V. ¿SE PUEDE TRANSFORMAR EL NÚCLEO DE UN ÁTOMO EN OTRO?
EFECTIVAMENTE, el núcleo de un átomo radiactivo, por ser inestable, se transforma, al decaer, en otro núcleo. Sin embargo, los átomos estables también pueden transformarse; esto se logra a través de las reacciones nucleares cuando los núcleos interactúan con otros núcleos, con partículas o con radiaciones de elevada energía. La primera reacción nuclear provocada por el hombre fue la transformación o transmutación de un elemento en otro: el sueño de los alquimistas.
EL SUEÑO DE LOS ALQUIMISTAS Y LA FÍSICA NUCLEAR
Durante la Edad Media el deseo de encontrar algún método de convertir un metal ordinario en oro era el estímulo principal de la investigación. Muchos alquimistas se esforzaron por encontrar la piedra filosofal, que, según suponían ellos, convertiría minerales y metales, como el mercurio y antimonio, en oro; querían encontrar la forma de transmutar un elemento en otro. Pero en el siglo XVII la alquimia entró en plena decadencia y ya en el siglo XVIII se transformó en la ciencia que ahora llamamos química. A finales del siglo pasado los científicos ya no pensaban en la transmutación de la materia y creían que los elementos químicos descubiertos eran definitivamente estables, que el mercurio y antimonio serían siempre mercurio y antimonio y el oro sería siempre oro. Nunca imaginaron que la transmutación de un elemento en otro volvería a ser un tema de actualidad.
Cuando se estableció que las propiedades químicas del átomo dependen del comportamiento del núcleo y se comprendieron los cambios y las transformaciones que acompañan a la radiactividad, muchos investigadores concibieron una idea verdaderamente fascinadora. Pensaron que el hombre podría, tal vez, alterar el núcleo de un átomo estable convirtiendo deliberadamente un elemento en otro distinto.
Una vez más aparece en esta historia ese famoso personaje ya bien conocido en las páginas de este libro, Ernest Rutherford. Este científico pensó que era posible que el núcleo de un átomo pudiera alterarse al ser bombardeado con partículas alfa, como las que emite la materia radiactiva. Bajo condiciones favorables, estas partículas debieron de pasar muy cerca del núcleo, en cuyo caso podrían o bien desarreglar su forma original, o bien, tal vez, combinarse con el mismo. Con esta idea bombardeó diversos gases con partículas alfa, y halló que en ocasiones una partícula alfa se combinaba con un núcleo de nitrógeno y que la combinación resultante emitía inmediatamente un protón y se transformaba finalmente en uno de los isótopos de oxígeno. Ésta fue la primera vez que se produjo deliberadamente la transmutación de un elemento químico estable en otro. Desde entonces, casi todos los elementos conocidos han sido transmutados por medio de bombardeo con diversas partículas. En esta forma, Rutherford llevó triunfalmente a cabo la primera reacción nuclear hecha por el hombre.
Esto es un auténtico ejemplo de transmutación, de conversión de un elemento en otro. En cierto modo, es la culminación de los viejos anhelos alquimistas, pero, desde luego, implica elementos y técnicas que los alquimistas desconocían por completo. Esta reacción ahora se puede expresar en forma taquigráfica:
queriendo decir con esto que el átomo de nitrógeno-14 al capturar una partícula alfa, forma un núcleo compuesto muy inestable que al buscar su estabilidad emite inmediatamente un protón transformándose así en un átomo de oxígeno-17.
Hoy en día, el mercurio puede transformarse de hecho en oro, mediante técnicas nucleares; pero el costo actual de esta transmutación sería tan elevado que el proceso resultaría un fracaso económico. Como muchos sueños, el de los alquimistas resultó finalmente no ser económicamente tan prometedor como parecía.
Ahora se conocen gran número de reacciones nucleares, entre ellas la reacción de captura de un neutrón. Los núcleos al capturar un neutrón forman primero un núcleo compuesto excitado que a su vez, por emisión de rayos gamma de muy elevada energía, decae a un estado menos excitado. Esta interacción se conoce con el nombre de reacción nuclear (n, g)
LA FISIÓN NUCLEAR: EL ROMPIMIENTO DEL NÚCLEO DEL ÁTOMO
Otra reacción nuclear sumamente importante en la serie de descubrimientos científicos es el rompimiento del núcleo del átomo. Para hablar de este fenómeno, situémonos en el ambiente científico de los años treinta. En 1934 ya se había descubierto la radiactividad artificial. Los científicos de esta época se pusieron a trabajar inmediatamente en producir nuevos núcleos en forma artificial. En particular en estas áreas se distinguieron tres grupos de investigadores encabezados por científicos notables: en Italia, Enrico Fermi; en Francia, los esposos Frédéric e Irène Joliot-Curie; en Alemania, Otto Hahn y su tía Lise Meitner.
Las primeras partículas utilizadas para bombardear los núcleos atómicos fueron las partículas alfa, que, por estar cargadas positivamente, eran rechazadas por los núcleos atómicos cargados también positivamente, ya que las cargas eléctricas del mismo signo se repelen entre sí.
El descubrimiento del neutrón abrió nuevas posibilidades; por no tener carga se aceptó con verdadero entusiasmo entre los investigadores nucleares, pues era el proyectil ideal para bombardear núcleos y producir reacciones nucleares, con la ventaja de poder dispararse hacia el núcleo cargado sin temor a ser repelido por las cargas presentes, lo cual era una de las dificultades que presentaba la partícula alfa cuando se utilizaba como proyectil. En otras palabras, la trayectoria del neutrón en general no se afecta por los electrones negativos del átomo, y no se desvía como una partícula cargada y sólo lo hace ocasionalmente a través de colisiones con los electrones de la corona. Sin embargo, cuando se acerca mucho al núcleo, el neutrón queda sujeto a las fuerzas muy intensas que existen entre los protones y neutrones en el núcleo.
El primero que investigó en detalle el bombardeo con neutrones fue Enrico Fermi
(Fig. 25). Comenzó su trabajo casi inmediatamente después de enterarse del descubrimiento
del neutrón. Él y sus colaboradores produjeron radiactividad en forma artificial,
bombardeando los núcleos de los átomos ya no con partículas alfa sino con neutrones.

Figura 25. Enrico Fermi (al centro) acompañado por Ernest Lawrence
e Isidor Rabi.
En esa forma produjeron nuevos núcleos de casi todos los elementos, muchos de ellos radiactivos, y descubrieron un gran número de isótopos radiactivos. En su primera publicación sobre estos trabajos, Fermi reconoció que 47 de los 68 elementos que examinó al ser irradiados con neutrones se activaron transformándose en isótopos radiactivos.
Fermi descubrió en esa época un fenómeno que estaba muy relacionado con estos experimentos. Halló que los neutrones eran particularmente eficaces para producir radiactividad si primero se hacían pasar a través de agua o parafina. Los átomos de estos compuestos absorbían parte de la energía de los neutrones y éstos reducían su velocidad al atravesar los materiales ricos en carbono e hidrógeno. De este modo, los neutrones eran frenados hasta que se movían sólo con la velocidad normal de las moléculas a la temperatura ambiente. Tales neutrones lentos permanecían en las proximidades de un núcleo determinado durante un tiempo más largo, y eran absorbidos con más probabilidad que los neutrones rápidos. Los neutrones lentos, así conseguidos, inducían más fácilmente la radiactividad al incidir sobre los elementos. Encontraron que en algunos casos la captura de un neutrón por un núcleo iba acompañada por la emisión de una partícula beta. Esta reacción producía un átomo cuya carga nuclear positiva había aumentado en una unidad y, por consiguiente, pertenecía en el próximo puesto más elevado en la tabla periódica.
Fascinados por estos resultados, Fermi y sus colaboradores concibieron la idea de hacer un ensayo parecido con uranio, el último elemento hasta entonces conocido en la tabla periódica. Así, bombardearon el uranio con neutrones, para ver si podían producir átomos más pesados que el uranio (elementos transuránicos), ya que en aquella época el uranio tenía el mayor número atómico de la tabla periódica, con 92 protones. Fermi y sus colaboradores pensaban que el núcleo del uranio-238 al capturar un neutrón aumentaría su masa en una unidad y al decaer por una o varias desintegraciones beta podría producir elementos de 93, 94 o 95 protones.
Sin embargo, mucho después se tendría que reconocer que lo que estaban observando no eran los elementos transuránicos, como pensaba Fermi. De lo que sí se dio cuenta Fermi es que al bombardear el uranio y torio con neutrones lentos las radiaciones emitidas eran muy intensas; advirtió, además, que en estos dos elementos el fenómeno de activación era complejo y que en vez de producir un isótopo nuevo se producía una mezcla de isótopos radiactivos.
El estudio de los efectos producidos por el bombardeo de uranio con neutrones resultó ser una tarea complejísima. Los resultados formaron un laberinto tan difícil e intrigante que se trabajó arduamente por varios años tratando de resolverlo.
Muchos laboratorios en esa época se dedicaron a buscar los elementos de más de 92 protones. Durante cuatro años, principalmente en laboratorios de Italia, Francia y Alemania, se bombardeaban los materiales con neutrones y se identificaban los productos radiactivos. Durante todo este tiempo se encontraron muchos isótopos radiactivos, pero los resultados obtenidos confundían cada vez más a los investigadores, pues como consecuencia de bombardear el uranio con neutrones se encontraban continuamente nuevos productos.
En esa época se multiplicaron las publicaciones sobre este tema, inclusive se consideró la posibilidad de que la creencia de Fermi respecto a haber obtenido elementos con 93, 94 o 95 protones era débil, y se hizo ver la posibilidad de que el uranio estallara y formara elementos más ligeros. ¡Cuánta razón tenían! Pero esta observación no fue tomada en cuenta. De haberse considerado, se hubieran evitado varios años de esfuerzo.
En el grupo francés también se analizaron estas posibilidades; los esposos Joliot-Curie y sus colaboradores se quedaron asombrados de encontrar como producto del bombardeo del uranio con neutrones un elemento como el lantano, el cual, como ellos sabían, solamente tiene 40 protones, mientras que el uranio tiene 92.
Cambiar el uranio en lantano significaba una disminución de... ¡52 protones! Sería como pensar que el átomo de uranio se hubiese partido aproximadamente por la mitad. Discutieron largamente este resultado y trataron de explicarlo como producido por el rompimiento del uranio irradiado en dos fracciones, pero finalmente desecharon esta hipótesis y publicaron únicamente que habían encontrado un elemento radiactivo, que se podría separar junto con el elemento lantano.
Las controversias y discusiones que tuvieron los Joliot-Curie con el grupo
alemán, particularmente con Lise Meitner, excelente radioquímica berlinesa,
y con su sobrino Otto Hahn (Fig. 26), fueron conocidas en todo el medio científico.
Los científicos alemanes no podían creer que el experimento realizado en Francia
al irradiar el uranio con neutrones pudiera dar lugar al lantano. Sin embargo,
para confirmar sus propios resultados, Otto Hahn con sus colaboradores repitieron
los experimentos en Alemania. Encontraron, por su parte, que el elemento radiactivo
separado se comportaba como el bario, pero al verificar la técnica utilizada
por el grupo encabezado por los esposos Joliot-Curie encontraron también, como
ellos, lantano en la mezcla.

Figura 26. Otto Hahn (1) y Lise Meitner acompañados por un grupo
de eminentes científicos.
El panorama científico en esa época era bastante confuso. Cada grupo científico obtenía gran número de isótopos radiactivos al bombardear el uranio con neutrones, pero nadie había podido dar una explicación correcta.
Fermi y sus colaboradores, en su búsqueda de elementos con un número mayor de protones que el uranio habían encontrado algo que nunca pudieron explicar correctamente. Por su parte los esposos Joliot-Curie y sus colaboradores se acercaron mucho a la verdad al pensar que el uranio podría dividirse en dos fracciones, pero no se atrevieron a definir y a apoyar su idea, que estaría de acuerdo con las predicciones hechas anteriormente. Por fin, en el año de 1939 Otto Hahn y sus colaboradores anunciaron la solución del problema.
Su mérito principal fue el de interpretar correctamente el fenómeno. Efectivamente, los científicos alemanes encontraron que cierto núcleo de uranio —el uranio-235, como después se supo— se rompía al ser bombardeado con neutrones lentos; es decir, se partía en dos fracciones que a su vez producían elementos más ligeros, por lo general radiactivos.
A este fenómeno se le llamó fisión nuclear, siendo los productos de fisión los elementos ligeros formados.
El artículo sobre la fisión nuclear del uranio, publicado por el grupo de Otto Hahn, llegó a manos de Frédéric Joliot unos diez días después. Es fácil imaginar la disilusión de los científicos franceses al saber que la idea que habían desechado era la respuesta a sus experimentos.
Como consecuencia del descubrimiento de la fisión nuclear se publicaron muchos artículos, principalmente en Alemania, Japón y Francia.
La noticia de este descubrimiento creó gran agitación entre los científicos, pues pensaban que un proceso nuclear de esta naturaleza liberaría inmensas cantidades de energía.
La agitación fue aún mayor cuando se dieron cuenta de que el proceso de la fisión del núcleo iba acompañada de la liberación de varios neutrones nuevos.
El grupo francés, en particular, se dedicó a investigar el recién descubierto fenómeno de la fisión nuclear. Frédéric Joliot en pocos días llegó a dos conclusiones de primordial importancia: que cada fisión nuclear debía liberar una cantidad de energía considerable y que junto oon los productos de fisión, tales como el bario o el lantano, con menos neutrones que el átomo de uranio original, debía emitirse uno o varios neutrones en cada fisión. Para realizar estas investigaciones Joliot formó un grupo de trabajo en el Colegio de Francia.
Los investigadores del Colegio de Francia compararon el conjunto de neutrones formado durante la fisión nuclear con el de la población humana, en que ciertos individuos tienen descendencia mientras otros no la tienen. Los neutrones que producen más fisiones son como los individuos que tienen descendientes, mientras que aquellos que no producen fisión y que sólo son absorbidos por la materia los compararon con los individuos que no tienen descendencia. Para que la población de neutrones en el material fisionable se mantenga constante, cada una de las fisiones debe dar origen por lo menos a una nueva fisión.
Joliot y sus colaboradores evaluaron la tasa de natalidad de los neutrones, es decir, el número de neutrones emitidos por cada fisión. Ahora se sabe que en cada fisión se liberan en promedio dos o tres neutrones. Sus resultados mostraron la posibilidad de que, usándose un material de número pequeño, como el hidrógeno, para frenar a los neutrones generados en la reacción de fisión a fin de volverlos lentos, pudieran producir más fisiones, y dar origen a más neutrones, y así sucesivamente, lo cual haría posible la generación de reacciones nucleares de fisión en cadena. Estos estudios mostraron la posibilidad de usar la fisión para producir energía.
De esta manera, el grupo formado por Joliot llegó a una nueva etapa en su trabajo: después de verificar el fenómeno de la fisión y la producción de neutrones, estudiaron la energía aprovechable producida por las reacciones de fisión nuclear en cadena. En esta nueva etapa, el grupo del Colegio de Francia competía en una carrera científica en la que participaban los países más poderosos de esa época. Después de muchos estudios llegaron a la conclusión de que podrían mantener una reacción en cadena en forma constante utilizando uranio enriquecido en uranio-235 o bien uranio natural. Se dieron cuenta de que para hacer funcionar un reactor nuclear con uranio natural era necesario contar con un material que les permitiera frenar los neutrones de la fisión hasta convertirlos en neutrones lentos, y consideraron que el agua pesada era el material adecuado.
Cada átomo de uranio fisionado provocaría la fisión de varios más (Fig. 27),
en una reacción nuclear en cadena, con un resultado semejante al de la reacción
química en cadena. Pero como las reacciones nucleares implicaban intercambios
energéticos mucho mayores que las reacciones químicas, los resultados de una
reacción nuclear en cadena serían mucho más formidables. Partiendo de unos cuantos
neutrones, con una insignificante energía, podrían liberarse reservas enormes
de energía.
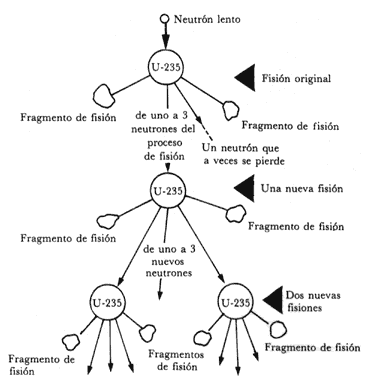
Figura 27. Diagrama de una reacción en cadena como resultado
de la fisión
de los átomos de uranio-235.
La enorme energía que se libera en el proceso de la fisión nuclear en cadena
es aprovechada hoy día en muchos países para producir energía eléctrica mediante
reactores nucleares, los cuales también se usan para otros propósitos, como
son la producción de isótopos radiactivos y la investigación científica (Figs.
28 y 29).

Figura 28. Exterior del Centro Nuclear de Salazar, Instituto Nacional de Investigaciones
Nucleares. (Fotografía: Roberto Campos.)
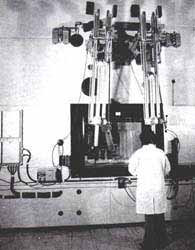
Figura 29. Interior del Centro Nuclear de Salazar, ININ.
La ciencia se ve enriquecida continuamente con descubrimientos que permiten desarrollar nuevas técnicas que son factores decisivos para llegar a conocer mejor la estructura de la materia.
Este es el caso del descubrimiento que hicieron Fermi y sus colaboradores al descubrir que era posible preparar isótopos radiactivos bombardeando elementos químicos con neutrones. Sin embargo, los isótopos formados, en muchos casos, siendo isótopos del mismo elemento irradiado, no podían ser separados y aislados utilizando técnicas químicas. Esto indujo a Szilard y a Chalmers a buscar la forma de separar un isótopo radiactivo de otros isótopos del mismo elemento utilizando técnicas químicas.
La separación de los isótopos de un mismo elemento
En 1934 Szilard y Chalmers bombardearon una solución de yoduro de etilo (I-etilo) con neutrones, propiciando así una reacción de captura de neutrón por el núcleo del yodo y observaron que una parte del yodo-128, formado por la reacción de captura de un neutrón por el núcleo del yodo-127, se encontraba en forma de yodo libre y no en la forma del yoduro de etilo original.
Este experimento demostró que las consecuencias de la reacción nuclear en el átomo de yodo son capaces de romper el enlace I-etilo. Este efecto, conocido después como "Szilard-Chalmers", proporcionó en esta forma una manera muy simple de separar isótopos de un mismo elemento, por vía química. En general dos formas químicas diferentes de un mismo elemento se pueden separar fácilmente por técnicas químicas; en este caso la técnica utilizada para separar el yodo y el yoduro de etilo fue la de extracción por solventes que se lleva a cabo por la agitación del producto bombardeado con neutrones en una mezcla de dos líquidos, uno acuoso y otro orgánico. En la fracción orgánica encontraron el yodo-128 separado completamente de su isótopo el yodo-127. Este ejemplo muestra la forma de separar dos isótopos de un mismo elemento por medio de una operación química muy sencilla, mientras que la mayoría de los métodos físicos para separar dos isótopos de un mismo elemento están basados en la diferencia de masa de ellos, que es en general una diferencia pequeña. Esto hace que el procedimiento sea costoso y que precise de instrumentos muy complejos.
Fermi y sus colaboradores explicaron el efecto Szilard-Chalmers como la consecuencia del retroceso del núcleo debido a la emisión del fotón en el proceso que conocemos como (n, g).
En general todas las transformaciones nucleares se acompañan de retrocesos nucleares más o menos intensos que pueden dar lugar a un cambio del sistema electrónico del átomo, causando de esta forma modificaciones químicas en la molécula en que se encuentra el núcleo transformado.
Si el átomo que sufre alguna de las transformaciones nucleares se encuentra formando parte de una molécula, la energía de retroceso del núcleo transformado puede romper el enlace químico y quedar todavía con una energía muy elevada; a menudo, esta energía cinética es tan alta, que el átomo energético no puede inicialmente formar combinaciones químicas. La energía se disipa por colisiones con otros átomos del medio; y finalmente, después de que se frena parcialmente, tienen gran capacidad de reaccionar con compuestos y radicales del Medio y formar por último un compuesto químico diferente al compuesto original del que partió.
La probabilidad de formación de nuevos núcleos por cualquiera de los procesos nucleares es, en la mayoría de los casos, muy pequeña: quizás uno de un millón de átomos pueda transformarse en otro núcleo; y en general es muy difícil detectarlo por los métodos analíticos tradicionales. Estos átomos nuevos, por lo general, son radiactivos; esto permite que se puedan detectar fácilmente por la radiación que emiten. En esta forma se puede estudiar su paso por la materia y su comportamiento.
Los efectos mencionados fueron usados en la práctica inmediatamente después de su descubrimiento; la primera aplicación fue en la separación de isótopos radiactivos de los demás isótopos de un elemento. Un ejemplo clásico está dado por la separación del radisótopo del cromo-50, que es uno de los isótopos del cromo que existen en la naturaleza; sometiendo este elemento a la acción de un flujo de neutrones se obtiene cromo-51.
Para que esta reacción nuclear produzca un cambio químico, es necesario que el cromo forme parte de un compuesto químico adecuado. En el cromato de potasio, el cromo es hexavalente, es decir, utiliza seis de sus electrones extranucelares. Al analizar el producto después de su irradiación con el cromo, parte del cromo-51 formado se encuentra en forma de cromo trivalente. Éste es un procedimiento sencillo para separar el isótopo de peso 51 de los otros isótopos del cromo, ya que la fracción del cromo-51 en forma trivalente se puede separar del cromo original por medio de técnicas químicas.
La separación química de isómeros nucleares
La misma técnica que se utiliza para separar isótopos se puede aplicar a la transición isomérica, y puede emplearse para separar isómeros nucleares. Los isómeros nucleares son aquellos núcleos que tienen masas y cargas idénticas, pero diferentes propiedades radiactivas.
El núcleo metaestable puede decaer por emisión de radiación gamma a su isómero en el estado básico; el estado básico es el de más baja energía del isómero nuclear. A menudo estos isómeros nucleares en el estado básico también son radiactivos.
Un ejemplo muy interesante está dado por la separación del isómero nuclear en el estado base del selenio-81b, de su correspondiente isómero nuclear metaestable, selenio-81m, y los otros isótopos del selenio. El selenio natural tiene varios isótopos, entre ellos el selenio-80. Las reacciones nucleares de captura de neutrones en los núcleos del selenio-80 producen los dos isómeros del selenio-81. Con la mezcla de isómeros nucleares del selenio, es necesario formar un compuesto adecuado como el selenato de potasio. El selenio-81 m, al emitir radiación y decaer así por transición isomérica a selenio 81b, rompe sus ligaduras y se estabiliza en la forma de selenio-81b tetravalente. Como el selenio tetravalente se puede separar del selenio hexavalente por técnicas químicas, este efecto permite también separar, por métodos químicos, los isómeros nucleares selenio-81b de los otros isótopos del selenio.