XI. VIRUS DE LA INMUNODEFICIENCIA HUMANA
POSIBLEMENTE ningún otro virus ha recibido tanta atención por
parte de los medios de comunicación y la opinión pública en general como el
llamado virus de la inmunodeficiencia humana (VIH o HIV).
La descripción, a principios de la década de los ochenta, de los primeros casos
del llamado síndrome de inmunodeficiencia adquirida (SIDA), padecimiento
que se caracteriza por una depresión progresiva de la inmunidad celular y que
con frecuencia tiene un desenlace fatal, provocó un gran interés por establecer
la causa o causas de esta enfermedad. El hecho de que los primeros casos de
SIDA se presentaron en jóvenes homosexuales con un alto índice
de promiscuidad sexual hizo sospechar que la enfermedad podía ser de carácter
infeccioso y transmisible a través del contacto sexual. Poco tiempo después
se estableció la presencia del SIDA en grupos de pacientes adictos
a las drogas por vía intravenosa (como la heroína), y también en algunos pacientes
que por diversas razones habían recibido transfusiones sanguíneas. Estos datos
reforzaron la idea de que el SIDA era infeccioso y algunos autores
sugirieron que podría ser causado por un virus desconocido.
A principios de 1983, investigadores del Instituto Pasteur de París, encabezados
por el doctor Luc Montagnier, reportaron el aislamiento de un nuevo tipo de
retrovirus a partir de un ganglio linfático extirpado a un paciente con SIDA.
Los investigadores franceses bautizaron como LAV (virus asociado a linfadenopatía)
a este nuevo retrovirus. Los mismos investigadores proporcionaron una muestra
de este retrovirus al grupo del doctor Robert Gallo en los Estados Unidos. El
grupo estadounidense contaba con reactivos y tecnología para mantener células
linfoides (linfocitos) en cultivo. Estas técnicas permitieron propagar al nuevo
retrovirus en cultivos de laboratorio. Sin embargo, los investigadores estadounidenses
identificaron al LAV como perteneciente al mismo grupo que el HTLV-I, previamente
descrito por el grupo de Gallo, y así, decidieron rebautizarlo como HTLV-III
(virus linfotrópico humano tipo III). Esta situación fue el origen de muchas
confusiones y de una prolongada disputa entre científicos y autoridades tanto
francesas como estadounidenses para adjudicarse el descubrimiento de este retrovirus,
al cual se le atribuyó la causalidad del SIDA con base en los resultados
de estudios epidemiológicos realizados en diversas partes del mundo, y fue finalmente
rebautizado como virus de la inmunodeficiencia humana (VIH) o Human Immunodeficiency
Virus (HIV).
Dichos estudios epidemiológicos demuestran una correlación entre la infección
por HIV y el subsecuente desarrollo del SIDA. Sin embargo, la epidemiología
del SIDA también demuestra que existe un largo periodo de latencia
que ha sido estimado entre 8 y 15 años, entre la infección primaria por HIV
y el desarrollo del SIDA.
Desde el punto de vista de su morfología y estructura genética básica, el HIV
pertenece al grupo de los retrovirus que se caracterizan por tener un genoma
constituido por ARN de cadena sencilla y se propagan por medio
de un intermediario intracelular (el provirus) formado por una molécula de ADN
de cadena doble que es sintetizada, por una enzima viral conocida como transcriptasa
inversa, a partir de la molécula de ARN genómico viral.
La organización de su genoma y su secuencia de nucleótidos indican que el HIV
pertenece a la subfamilia de los lentivirus, que esta constituida por retrovirus
que producen infecciones crónicas de evolución lenta en diversos animales, como
son el virus de la anemia equina infecciosa, el virus de la artritis-endefalitis
caprina, el virus visna-maedi que causa una enfermedad neurodegenerativa
en los borregos y el virus de la inmunodeficiencia del simio (SIV), que puede
causar en los macacos afectados un síndrome de inmunodeficiencia remotamente
parecido al SIDA.
La organización genómica de los lentivirus es mucho más compleja que la de
los retrovirus clásicos, como lo muestra la figura XI.1. Además de los tres
genes presentes en los retrovirus clásicos (genes denominados gag, pol
y env, mismos que codifican a las proteínas de la cápside, a la transcriptasa
inversa y funciones asociadas, y a las proteínas de la envoltura viral respectivamente),
el genoma del HIV contiene varios genes pequeños que codifican proteínas que
participan en forma importante en la regulación de la transcripción del genoma
viral. En particular, los productos de los genes tat y rev tienen
un papel muy importante como reguladores de la transcripción y el subsecuente
procesamiento y transporte de las diferentes especies de ARN mensajero
viral.
La figura XI.2 muestra el ciclo replicativo del HIV. Es importante mencionar que la integración del provirus dentro del genoma de la célula hospedera es un paso indispensable para la replicación de la mayoría de los retrovirus. Este proceso de integración sólo es posible en células activas que pasan cuando menos un ciclo completo de división celular. Sin embargo, existe evidencia de que el HIV es capaz de replicarse y permanecer estable incluso en células inactivas que no han pasado por una división celular.
La figura XI.3 muestra la estructura del virión de HIV. Estos viriones tienen
un diámetro de 100 a 120 nanómetros, son esféricos y poseen una envoltura constituida
por restos de la membrana de la célula hospedera que han sido modificados por
la inserción de dos tipos de proteínas virales: la gp120 que forma las púas
del virión y la gp4l que queda incluida en la envoltura viral. En en el interior
de la cápside viral se ubican dos copias del genoma viral, situación que es
común en todos los retrovirus. Este genoma está formado por una molécula de
ARN lineal de cadena sencilla que consta de 9400 nucleótidos. El
genoma viral se asocia con varias copias de dos proteínas virales: p7 y p9,
y la nucleocápside resultante es recubierta por varias copias de la proteína
viral p24 para formar la verdadera cápside o centro viral.
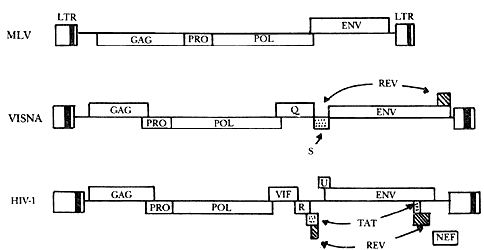
FIGURA XI.1. Organización del genoma proviral en retrovirus simples y retrovirus complejos. El esquema muestra la organización del genoma proviral de un común retrovirus simple: el virus de la leucemia murina (MLV), que muestra los genes gag, pol y env, flanqueados por las terminaciones largas repetidas (LTR) que constituyen las secuencias promotoras de la expresión de los genes virales y a su vez permiten la integración del genoma proviral (provirus) en el genoma de la célula hospedera. Los genomas de dos lentivirus: el virus Visna-Maedi y el HIV-1 muestran la presencia de nuevos genes que codifican proteínas regulatorias que controlan el proceso de transcripción y replicación de estos retrovirus complejos. Las siglas PRO denotan la posición de la secuencia que codifica a la proteasa viral cuya función consiste en el procesamiento de las proteínas virales estructurales, mismo que es necesario para permitir el ensamble de nuevas partículas virales.
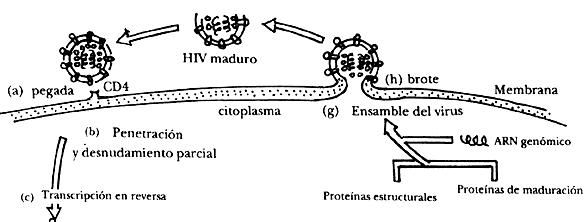
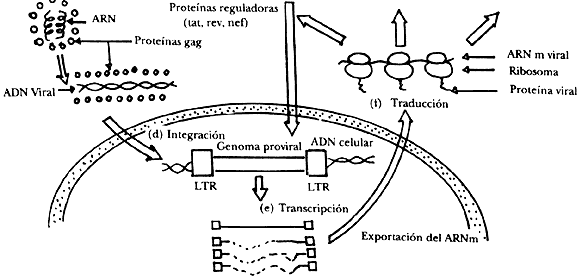
Figura XI.2. Replicación del HIV. a) la partícula viral se pega al
receptor CD4 presente en la membrana de ciertos tipos de linfocitos y células
inmunes. b) el virus penetra al interior de la célula y la envoltura viral,
constituida por lípidos, es removida para permitir la fusión del virión con
vacuolas citoplásmicas. c) en el corazón de la partícula viral ocurre el proceso
de transcripción en reversa mediado por la enzima transcriptasa inversa (RT)
viral. Este evento convierte al ARN viral original en una molécula
de ADN viral que constituye el provirus. d) el provirus es introducido
al núcleo celular y a continuación ocurre la integración del provirus al genoma
celular. e) el provirus integrado es transcrito por la enzima celular ARN
polimerasa II, los transcritos virales (ARN mensajeros) son exportados
al citoplasma. f) la traducción de algunos ARN mensajeros virales
conduce a la producción de proteínas virales regulatorias, mismas que estimulan
la síntesis de las llamadas proteínas de maduración viral y de las proteínas
estructurales del virión. g) la acumulación de proteínas estructurales en la
membrana celular permite el ensamble de nuevas partículas virales. h) la maduración
y brote de nuevas partículas virales ocurre entre 36 y 48 horas después del
inicio de la infección.
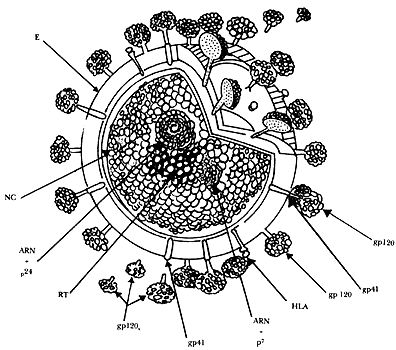
Figura XI.3. Estructura del virión de HIV.(E) envoltura formada por
una bicapa de lípidos derivada de la membrana de la célula hospedera. (gp120)
glicoproteína mayor de superficie con peso molecular de 120 000 daltones. (gp120s)
forma soluble de la gp120. (gp41) glicoproteína transmembranal con peso molecular
de 41 000 daltones. (HLA) antígeno de histocompatibilidad derivado de la membrana
de la célula hospedera. (NC) subunidades de la nucleocápside viral formada por
la proteína viral con peso de 17 000 daltones. (RT) moléculas de la enzima transcriptasa
inversa viral. (ARN + p24) ARN genómico viral rodeado
de múltiples copias de la proteína mayor del centro viral que pesa 24 000 daltones.
(ARN + p 7) ARN genómico viral cubierto por moléculas
de la proteína menor del centro viral con peso de 7 000 daltones.
A pesar de ser un virus con envoltura, el HIV es bastante resistente a la acción de solventes orgánicos como el alcohol, éter y cloroformo. También es muy resistente a la inactivación por agentes antisépticos y desinfectantes como el benzal.
Solamente algunos detergentes no iónicos como el TritonXl 00, el cloro activado y las temperaturas mayores a 60°C por varios minutos, son eficaces para inactivar al HIV La inusual resistencia del HIV a la inactivación por agentes fisicoquímicos es compensada por su baja infectividad, ya que el HIV infecta a sus células blanco con dificultad.
Con base en diferencias en la secuencia de nucleótidos se ha establecido que existen dos tipos fundamentales de HIV: el HIV-1 que corresponde al tipo más común y que se encuentra distribuido en todo el mundo, y el HIV-2 que fue aislado de pacientes que habitan en países centroafricanos. Hasta la fecha, la infección por HIV-2 sigue limitada a los países del África Central y es muy raro encontrarlo en otras partes del mundo. Sin embargo, la enzima transcriptasa inversa encargada de copiar el genoma viral, es una enzima que comete muchos errores de modo que introduce nucleótidos equivocados durante el proceso de copiado del genoma viral. La gran frecuencia con la que ocurren estas mutaciones (alrededor de 1 error por cada 1000 nucleótidos copiados), implica que existe una gran inestabilidad en la secuencia del genoma viral, de manera que a partir de un mismo paciente infectado con HIV se pueden aislar, en diferentes periodos de tiempo, cepas virales que han diferido entre sí debido a los cambios en la secuencia de nucleótidos del genoma viral. Esta gran viariabilidad del genoma del RIV se interpreta como una evidencia de que este virus está en proceso de lograr una adaptación evolutiva para establecer un equilibrio con su hospedero natural que en este caso, parece ser el hombre. Ha sido posible identificar la presencia del HIV en muestras congeladas de sangre o suero sanguíneo, procedentes de pacientes que fallecieron durante los años cincuenta. Pero todo parece indicar que el HIV constituye una especie viral muy reciente.
La evidencia disponible indica que el HIV sólo puede infectar en forma productiva y persistente al hombre y al chimpancé, y solamente se replica en cultivos de células humanas o de chimpancé, en particular de linfocitos. Sin embargo, chimpancés que han sido infectados con grandes dosis de HIV desde 1983, no han desarrollado ninguna enfermedad que sugiera inmunodeficiencia adquirida. Es un hecho que el HIV tiene predilección por infectar células que poseen el receptor CD4 en sus membranas, como son los linfocitos T auxiliares, los monocitos y los macrófagos. Sin embargo, se sabe que otros tipos de células que no son CD4+ también son infectables por HIV, pero todo indica que estas células no sufren efectos adversos como consecuencia de dicha infección.
Las principales vías de contagio por este virus son la sangre (y productos derivados de la sangre) y el contacto sexual. La eficacia del contagio por vía sanguínea depende de varios factores como son el número de partículas virales presentes en la sangre contaminada, el volumen de sangre aplicado y el estado inmunológico del individuo receptor. Hoy en día, la transmisión por vía sexual es la principal forma de contagio por HIV. Desafortunadamente, es frecuente la transmisión del HIV de la madre al producto, durante el embarazo o durante el periodo inmediato al nacimiento.
La evidencia de contagio por HIV se establece por medio de una prueba de ELISA específica (ELISA significa en inglés: enzyme linked inmuno sorbent assay), esta prueba permite detectar en el suero sanguíneo la presencia de anticuerpos específicos contra la proteína gp l2O del HIV. Un resultado positivo (seropositivo) se interpreta como evidencia de que la persona ha estado en contacto con el HIV.
Es una gran paradoja que la seropositividad anti-HIV sea interpretada como
factor de riesgo para la transmisión del propio HIV, ya que la presencia de
anticuerpos anti-HIV en el suero de los pacientes seropositivos no parece protegerlos
de desarrollar, tarde o temprano, el SIDA. Esto contrasta con lo
que ocurre en el caso de otros virus, ya que la seropositividad antipolio, anti-viruela
o anti-HBV es interpretada como evidencia de vacunación o inmunidad específica
contra estos virus. De hecho, las personas seropositivas a la polio, viruela
o HBV están protegidas contra la infección o reinfección por estos virus y,
a su vez, son incapaces de transmitirlos a otras personas. Sin embargo, en el
caso de las personas anti-HIV seropositivas se infiere que el virus está presente
y potencialmente activo, cuando menos como provirus, en el interior de las células
linfoides infectadas. Por esta razón, la opinión médica dominante considera
a las personas anti-HIV seropositivas como transmisores potenciales de la infección
por HIV, y esto a pesar de que en muchas personas anti-HIV seropositivas se
puede demostrar la presencia de anticuerpos capaces de neutralizar al HIV en
pruebas de laboratorio. Así, tomando en cuenta las graves repercusiones que
puede tener el diagnóstico de seropositividad anti-HIV, toda prueba de ELISA
positiva para HIV, debe ser confirmada por medio de una prueba mucho
más sensible y exacta que se conoce como Western Blot, ya que el ELISA
puede dar falsas reacciones positivas. La prueba del Western Blot permite
demostrar la existencia de anticuerpos específicos contra todas y cada una de
las proteínas estructurales del HIV. El Western Blot positivo confirma
la infección por HIV.
Las características clínicas del SIDA indican una profunda alteración
de los mecanismos de la inmunidad celular, por lo cual desde un principio se
llegó a sospechar que el HIV tenía como blanco a un órgano o tipo de célula
fundamental para la respuesta inmune celular. A fines de 1983, investigadores
de Francia e Inglaterra demostraron que el HIV tiene una gran predilección por
infectar linfocitos T auxiliares (o linfocitos CD4+), los cuales se caracterizan
por tener un receptor membranal denominado molécula CD4. Este receptor reconoce
una clase de proteínas conocidas como moléculas clase II del complejo mayor
de histocompatibilidad (MHC-clase II), las cuales están presentes en las membranas
de los linfocitos B, los macrófagos y de los linfocitos T activados. La interacción
entre el receptor CD4 y la molécula MHC-clase II es un cofactor en el proceso
de reconocimiento de antígenos específicos por parte de los linfocitos T auxiliares.
Dichos linfocitos CD4+ juegan un papel central como coordinadores y estimuladores
de otras células y actividades que participan en la respuesta inmune de tipo
específico.
Los mismos grupos de investigadores europeos demostraron que la molécula CD4 es el receptor de alta afinidad para el HIV, mismo que se fija a los linfocitos T auxiliares por medio de la interacción entre la glicoproteína viral 120 (gp 120), presente en la superficie de la envoltura del virus, y el receptor CD4. Por otra parte, estudios inmunológicos establecieron que en pacientes con SIDA avanzado existe una importante disminución en el número de linfocitos CD4+. Las primeras observaciones sobre la replicación y el comportamiento del HIV en cultivos celulares enriquecidos en linfocitos CD4+, sugirieron que el virus es citopático para este tipo de células.
Las observaciones anteriores fueron conjuntadas para establecer un modelo explicativo de la patogénesis del SIDA. Dicho modelo propone que el SIDA es consecuencia de la destrucción progresiva de linfocitos auxiliares CD4+ debida a la acción citopática del HIV y por esta razón, los pacientes con SIDA terminan sucumbiendo a infecciones oportunistas o a cierto tipo de tumores malignos que son consecuencia o manifestación de la disminución de la inmunidad celular, provocada por la pérdida de células CD4+. Un corolario que deriva de este modelo es que el SIDA es potencialmente curable mediante la acción de antivirales capaces de inhibir la replicación del HIV.
Sin embargo, múltiples observaciones acumuladas durante la última década sugieren que el modelo arriba mencionado dista de ser correcto, como lo demuestran las siguientes observaciones: 1) el número de linfocitos CD4+ que manifiestan infección productiva por HIV es muy reducido, siendo alrededor de 1/10 000 en la sangre periférica y 1/1000 en los ganglios linfáticos, este nivel de infección activa es mucho menor que la capacidad del sistema inmune pra reponer a las células perdidas como consecuencia de la infección. 2) en pacientes infectados por HIV que se encuentran en la llamada fase asintomática, la cual puede durar varios años, es posible detectar importantes alteraciones en los mecanismos de inmunidad celular aun cuando sus valores de linfocitos CD4+ circulantes se encuentran dentro de lo normal. 3) varias parasitosis profundas y otras infecciones virales provocan una importante disminución en la población de linfocitos CD4+, sin embargo, no producen una sintomatología similar al SIDA. 4) Nadie ha podido demostrar el efecto citopático del HIV in vivo. Por otra parte, diversas cepas de HIV aisladas a partir de pacientes con SIDA terminal no son citopáticas in vitro. 5) Es relativamente fácil aislar el HIV a partir de los linfocitos periféricos de pacientes recién infectados con HIV, los cuales sufren una enfermedad benigna parecida a la gripe o a la mononucleosis infecciosa, misma que desaparece en pocas semanas. Sin embargo, es muy difícil aislar el virus a partir de linfocitos periféricos de pacientes en fase asintomática y sólo en algunos pacientes con SIDA terminal se puede volver a aislar el virus con facilidad. Estas observaciones sugieren que la replicación del HIV en los linfocitos periféricos está muy reducida durante la larga fase asintomática. 6) agentes antivirales como la azidotimidina también conocida como zidovudina o AZT, inhiben en forma importante la replicación del HIV; sin embargo, no han servido para detener la caída de los linfocitos CD4+ ni el desarrollo del SIDA en pacientes asintomáticos tratados con estos compuestos por largo tiempo. 7) Son cada vez más frecuentes los reportes de personas que han estado infectadas con HIV por más de diez años y que sin embargo, se encuentran en buena salud a pesar de no haber seguido ningún tipo de tratamiento específico.
La falta de correlación entre los marcadores clásicos de actividad viral (como son la concentración de partículas virales infecciosas y los niveles de antígenos [proteínas] virales en el suero sanguíneo) y las manifestaciones clínicas del SIDA, ha motivado a los investigadores a establecer otros parámetros que les permitan evaluar la actividad de la infección por HIV durante el desarrollo del SIDA.
El HIV es un retrovirus y como tal, en forma de provirus debe integrarse al
genoma de la célula hospedera para poder replicarse y, eventualmente, producir
nuevas moléculas de ARN y proteínas virales que sirvan para ensamblar
nuevos vinones infectantes. Sin embargo, la mayor parte de los retrovirus clásicos
tienden a permanecer como provirus silenciosos dentro del genoma de sus células
hospederas y sólo muy de vez en cuando expresan su información genética con
el fin de producir nuevos componentes virales. De hecho, los retrovirus prefieren
propagarse en forma vertical o sea, cada vez que se replica el genoma de la
célula hospedera también es replicado el provirus integrado a dicho genoma,
de manera que las dos células hijas que resultan del proceso de división celular
contienen una copia del provirus retroviral integrado en sus respectivos genomas.
Esta estrategia equivale a una propagación pasiva del genoma viral. Por lo tanto,
una importan te cuestión consiste en establecer si el HIV se propaga principalmente
como un retrovirus clásico o si por el contrario, se propaga en forma horizontal
y activa: por medio de la producción de viriones infectantes capaces de salir
al medio externo para infectar nuevas células blanco.
Así, técnicas moleculares como la llamada hibridación de ácidos nucléicos in
situ y la amplificación de secuencias genómicas específicas por medio de
la reacción de polimerasa en cadena (PCR), permiten detectar la presencia de
ARN viral y del provirus integrado en el genoma de la célula hospedera.
Estas técnicas son muy sensibles y han permitido crear un nuevo parámetro virológico
que se conoce como "carga viral", que corresponde al porcentaje de células blanco
(células hospederas) que contienen información viral (como provirus o como ARN
viral), pero sin importar si dicha información viral está siendo utilizada para
producir nuevas partículas virales infectantes o solamente corresponde a una
infección latente en la cual no se expresa la información viral presente en
la célula hospedera.
Al parecer, en el caso de la infección por HIV, la carga viral se va incrementando gradualmente durante el curso de los años desde la infección inicial hasta la aparición del SIDA. Por otra parte, se ha podido establecer que dicha carga viral aumenta preferentemente en las células T auxiliares (CD4+) ubicadas en los tejidos linfoides como son: los ganglios linfáticos, el bazo y el tejido linfoide presente en la pared intestinal. También los macrófagos ubicados en estos tejidos muestran un aumento en la carga viral por HIV. Sin embargo, en los linfocitos CD4+ de la sangre periférica la carga viral por HIV es muy reducida ya que sólo en 1 de cada 10 000 linfocitos CD4+ es demostrable la presencia del provirus y de esta pequeña fracción de células infectadas sólo el 1% manifiesta una infección activa y la consecuente producción de nuevas partículas virales. Estos datos constituyen una gran paradoja, ya que resulta difícil explicar la gradual disminución de la población de linfocitos CD4+ como consecuencia de la infección activa por RW, puesto que el número de células que muestran infección activa es muy reducido y sobre todo, mucho menor que la capacidad del sistema inmune para reponer las células que pudieran haber sido destruidas como consecuencia de la infección por HIV.
Al momento de escribir estas notas (febrero de 1995), acaban de ser publicados
los resultados de dos estudios que pretenden haber resuelto la paradoja arriba
mencionada. Según estos estudios, consignados en la bibliografía al final de
este libro, el número de linfocitos CD4+ que son destruidos y repuestos diariamente
como consecuencia de la infección por HIV, es de alrededor de 10 9
(mil millones de células), este número es muy similiar a la carga viral promedio
(número total de linfocitos y otras células linfoides en los cuales se puede
detectar provirus o ARN viral, independientemente de que el provirus
este activo o no). Los resultados de estos estudios sugieren que durante el
largo curso de la infección por HIV que finalmente desemboca en el SIDA,
se encuentra sobreestimulada la capacidad del sistema inmune para reponer a
sus células perdidas o dañadas y que esta sobreestimulación, equivalente a 50
veces el promedio de recambio de células inmunes observado en individuos normales,
es consecuencia de una continua destrucción de linfocitos CD4+ que tiene lugar,
posiblemente, en los tejidos linfoides. Estas investigaciones sugieren que el
SIDA es consecuencia del eventual agotamiento del sistema inmune
que en un momento determinado ya no puede reponer el número de células que son
diariamente destruidas por la infección viral. Para llegar a estas conclusiones
fue necesario correlacionar datos de laboratorio y resultados de varios protocolos
de tratamiento con antivirales experimentales en grupos de pacientes con SIDA;
dichas correlaciones se establecieron por medio de métodos matemáticos que para
ser utilizados requieren de una serie de suposiciones y simplificaciones respecto
al comportamiento dinámico de las poblaciones virales y celulares que interactúan.
Puede ser que los resultados arriba mencionados sean una importante contribución para comprender la dinámica de la infección por HIV. Sin embargo, existen numerosas observaciones que hacen dudar que el HIV sea un virus citopático in vivo. Además, persiste la cuestión de por qué los chimpancés, que son la especie más cercana al hombre, pueden ser infectados en forma crónica y productiva por el HIV y, sin embargo, no desarrollan el SIDA. Si el HIV es verdaderamente citopático, resulta difícil explicar la resistencia de los chimpancés a la enfermedad, a menos que el sistema inmune del chimpancé tenga una capacidad de regeneración muy superior a la del hombre, lo cual es poco probable.
La evidencia disponible sugiere que el HIV dista de ser un virus que causa enfermedad por un mecanismo directamente citopático, como es el caso de los virus de la influenza o del Herpes simplex. Por lo tanto, las alteraciones en las funciones de los linfocitos CD4+, y la subsecuente disminución de los mismos deben ser provocadas por mecanismos que involucran al HIV de manera indirecta.
La inmunopatología es una disciplina que estudia la participación del sistema inmune en el desarrollo de diversas enfermedades; en algunos casos el sistema inmune pueder ser una de las causas de la enfermedad, en otros casos el sistema inmune pueder ser una víctima de la enfermedad y en otros más, el sistema inmune puede ser tanto causante como víctima de la enfermedad. Avances recientes en el conocimiento de la inmunopatología del SIDA, sugieren que el HIV puede ser una causa necesaria pero tal vez no suficiente para provocar el SIDA y, por lo tanto, se necesita de la acción de cofactores que también participan en el mecanismo o mecanismos que conducen a desarrollar el SIDA.
Como ya fue mencionado, la infección primaria por HIV puede ser asintomática o manifestarse como un síndrome gripal de resolución rápida. Posteriormente hay un largo periodo de latencia que dura varios años y que es asintomático, hasta que aparecen las primeras manifestaciones clínicas del SIDA que se presenta como una inflamación de varios grupos de ganglios linfáticos (linfadenopatía), acompañada de la pérdida de peso, diarrea persistente y posteriormente, se presentan una o varias infecciones oportunistas (causadas por microorganismos que tienen un bajo potencial patogénico) o la reactivación de antiguas infecciones latentes como la tuberculosis o el herpes. En algunos casos se desarrollan tumores malignos como el sarcoma de Kaposi o ciertos linfomas, y manifestaciones neurodegenerativas que terminan en la demencia.
Cualquiera de los procesos anteriores puede ser la causa del fallecimiento.
Sin embargo, desde que se describieron los primeros casos de SIDA, varios autores notaron una importante similitud entre las manifestaciones clínicas del SIDA y aquellas propias de ciertas enfermedades conocidas como enfermedades autoinmunes, las cuales se caracterizan porque el sistema inmune reconoce como extrañas a células y moléculas del propio organismo, por lo cual las ataca y produce enfermedad. En particular, existe un padecimiento de tipo autoinmune conocido como enfermedad del injerto contra el hospedero, cuyas manifestaciones clínicas son muy similares al SIDA; esta enfermedad es producida por células inmunocompetentes (linfocitos, macrófagos, etc.) que normalmente están presentes en el material o tejido transplantado. La enfermedad del injerto contra el hospedero puede ocurrir como consecuencia de la infusión de cualquier derivado de la sangre que pueda contener linfocitos viables, como es el caso en las transfusiones de sangre entre la madre y el feto, las transfusiones de sangre total con fines terapéuticos, las transfusiones de plasma sanguíneo o de paquetes de células sanguíneas. También se puede presentar esta enfermedad como consecuencia del transplante de timo o de hígado fetal y en los transplantes de médula ósea.
Cierto tipo de enfermedades como la anemia aplástica, las leucemias agudas, la inmunodeficiencia combinada congénita y las anemias resultantes de la exposición a radiaciones ionizantes o debidas al uso de agentes quimioterápicos en el tratamiento del cáncer; pueden ser tratadas por medio de transplantes de médula ósea, que es el tejido a partir del cual se originan las células sanguíneas que incluyen a los glóbulos rojos y los glóbulos blancos, entre los cuales se encuentran los linfocitos B. Para hacer un transplante de médula ósea primero se establece que el donador y el receptor del transplante son compatibles a nivel de sus antígenos de histocompatibilidad, esto evita que el tejido transplantado sea eventualmente reconocido como extraño y por lo tanto, rechazado por el sistema inmune del receptor. Sin embargo, en la médula ósea del donador existen células inmunocompetentes capaces de reconocer como extraños a los tejidos del receptor. A veces no es posible eliminar las células inmunocompetentes presentes en el tejido a ser transplantado y esto da como resultado que las células inmunes del tejido transplantado empiezan a reconocer como extrañas a las células y moléculas del organismo receptor del transplante. Dichas células inmunocompetentes se activan y atacan a los tejidos del receptor, provocando la enfermedad del injerto contra el hospedero, misma que puede ir desde una simple urticaria hasta una severa inmunodeficiencia, debida al ataque de las células inmunocompetentes del injerto sobre los tejidos linfoides del individuo receptor del transplante, y que se asocia con el desarrollo de infecciones oportunistas y lesiones en la piel, el hígado y el aparato digestivo.
En la actualidad se sabe que la proteína gpl20 del HIV tiene similitudes estructurales con un tipo de proteínas humanas conocidas como moléculas del complejo mayor de histocompatibilidad clase II (MHC-clase II). Dichas moléculas están presentes en la superficie de los linfocitos B, de los macrófagos y de los linfocitos T activados, y participan en la presentación de antígenos foráneos para que estos puedan ser reconocidos por el sistema inmune como extraños. La similitud entre gp 120 y MHC-clase II puede ser el origen de una grave confusión en la respuesta inmune, ya que anticuerpos y células T citotóxicas capaces de reconocer la presencia de gp l20 en la superficie de células infectadas por HIV, son también capaces de reconocer a las MHC-clase II presentes en la superficie de células inmunocompetentes normales, esto puede provocar que los componentes de la respuesta inmune dirigida contra HIV se comporten también como atacantes de las células normales que presentan MHC-clase II. Esto puede resultar en la destrucción de varios tipos de células inmunocompetentes entre las cuales se encuentran los linfocitos CD4+ activados que expresan la MHC-clase II en sus membranas.
La activación de los linfocitos T es condición necesaria para que expresen la molécula MHC-clase II en sus membranas. Por lo tanto, existe la posibilidad de que dicha activación dé como resultado que algunas poblaciones de linfocitos T activados se vuelvan blanco potencial de la respuesta inmune dirigida contra el HIV. Si tal es el caso, entonces deben existir mecanismos dirigidos a evitar la activación de estas células de manera que no puedan expresar la molécula MHC-clase II en sus membranas. Durante los últimos años se han acumulado observaciones que demuestran la presencia de abundantes linfocitos T supresores en pacientes infectados por HIV. Se ha sugerido que la función de estos linfocitos supresores consiste en evitar la activación de los linfocitos CD4+ para evitar que puedan ser blanco de un ataque por parte de la respuesta inmune contra HIV. Sin embargo, la supresión de la activación vuelve anérgicos a los linfocitos T auxiliares (CD4+), o sea, que no reaccionan ante agentes activadores como son los antígenos derivados de otros microorganismos patógenos. El resutado del estado anérgico es que los linfocitos auxiliares no pueden actuar como coordinadores y estimuladores de la respuesta inmune celular y por lo tanto, la persona afectada manifiesta importantes alteraciones en sus funciones inmunitarias a pesar de que todavía no se presenta una franca disminución en la población de linfocitos CD4+ auxiliares.
Los linfocitos T citotóxicos y los linfocitos T supresores se caracterizan por presentar en sus membranas un receptor conocido como CD8. Por otra parte, en personas normales la concentración de linfocitos CD4+ es de alrededor de 1 000 por milímetro cúbico de sangre. En la sangre de individuos normales la relación entre células CD4+ y CD8+ es de 2:1. Sin embargo, en los pacientes infectados por HIV esta relación está invertida con mucha frecuencia (CD4+/CD8+ 1:2) y este fenómeno ocurre mucho antes de la disminución de la población de linfocitos CD4+, misma que se observa en las etapas terminales del SIDA (en las cuales la población de linfocitos CD4+ es menor a 200 por milímetro cúbico). De hecho, la inversión del índice CD4+/CD8+ parece deberse a una proliferación excesiva de los linfocitos CD8+. En las etapas terminales del SIDA todas las poblaciones linfocitarias disminuyen en número; sin embargo, la proporción relativa CD4+/CD8+ permanece alterada, siendo estas últimas células las más numerosas en términos relativos. Como ya fue mencionado, pacientes infectados con HIV que están en fase asintomática muestran ya importantes alteraciones en las funciones de los linfocitos CD4+, y se sabe que grupos de estos linfocitos se encuentran en estado anérgico o sea, no reaccionan ante estímulos que normalmente activan a estos linfocitos. Dicho estado de anergía puede ser cancelado o reducido si se procede a separar a los linfocitos CD4+ de los linfocitos CD8+. Los linfocitos CD4+ purificados muestran una mejoría en sus reacciones cuando son ensayados in vitro, en ausencia de linfocitos CD8+. Esto sugiere que en pacientes infectados por HIV existe un estado inmunosupresor que bloquea la activación de los linfocitos CD4+. Diversas observaciones sugieren que los pacientes infectados por HIV que presentan un aumento temprano y excesivo en sus poblaciones de linfocitos CD8+, son candidatos a desarrollar el SIDA con mayor rapidez.
Los límites del presente libro no permiten continuar detallando otras importantes observaciones e hipótesis referentes a la inmunopatología del SIDA, tópico que está recibiendo cada vez mayor atención por parte de los investigadores. Todavía no se pueden hacer conclusiones definitivas acerca de los mecanismos causales del SIDA, y debemos estar preparados para futuras sorpresas al respecto. Existe una gran urgencia por conocer dichos mecanismos con el fin de lograr tratamientos eficaces para este padecimiento. Sin embargo, a pesar de la intensa investigación sobre este tema, todavía carecemos de respuestas verdaderas; pero un sano principio de la ciencia consiste en reconocer nuestras dudas, pues a partir de estas se puede llegar a comprender y aprender; mientras que la falsa sabiduría y las respuestas mal fundamentadas conducen a la confusión y al retraso del conocimiento.
PREVENCIÓN Y TRATAMIENTO DEL SIDA
Hasta el momento, los tratamientos con antivirales específicos como la azidotimidina (zidovudina) han dado pobres resultados en el tratamiento del SIDA y sólo se han logrado progresos en el manejo de las complicaciones clínicas del SIDA, utilizando medicamentos que disminuyen los síntomas y molestias asociadas con esas complicaciones. Existe una amplia variedad de agentes antivirales que están siendo evaluados respecto a su acción contra el HIV. Desafortunadamente, la mayoría de los antivirales probados hasta la fecha, inducen con rapidez la aparición de mutantes de HIV resistentes a dichos antivirales.
En cuanto al desarrollo de posibles vacunas específicas contra el HIV, cabe mencionar que la mayoría de los proyectos para el desarrollo de estas vacunas fueron iniciados con base en una apreciación incorrecta y apresurada de los mecanismos causales del SIDA. Hasta la fecha, la mayoría de dichas vacunas experimentales se dirige a estimular la producción de anticuerpos específicos contra componentes del HIV, por medio de la inoculación en animales (o de personas voluntarias) de proteínas o fragmentos de proteínas virales que actúen como antígenos que estimulen al sistema inmune para producir anticuerpos específicos contra estos componentes virales. Dichos anticuerpos podrían actuar neutralizando al virus, evitando así que este pueda infectar a las células del organismo vacunado.
Un importante obstáculo para el desarrollo de vacunas contra el HIV es que no se conoce ninguna especie animal que desarrolle SIDA como consecuencia de la infección por HIV; por lo tanto, no existe ningún modelo animal para probar directamente la capacidad protectora de dichas vacunas. Por esta razón se ha recurrido a métodos indirectos que permiten establecer la presencia de una respuesta inmune contra el HIV en chimpancés vacunados y también se ha recurrido a un sistema paralelo que consiste en desarrollar vacunas experimentales contra el llamado síndrome de inmunodeficiencia adquirida del simio, supuestamente causado por un virus parecido al HIV (SIV), con la esperanza de que los datos obtenidos en el modelo animal puedan orientar hacia el desarrollo de una vacuna efectiva en el humano.
Desafortunadamente, estos modelos de vacunación parecen no tomar en cuenta dos hechos fundamentales: la mayoría de los pacientes que desarrollan el SIDA tienen anticuerpos neutralizantes específicos contra el HIV y sin embargo no son protegidos contra la enfermedad. Por otra parte, existen importantes evidencias de que el principal modo de transmisión del HIV de un individuo infectado a un individuo receptor no es por medio de los viriones libres en el suero sanguíneo del transmisor, sino por la introducción de células infectadas en el interior del organismo receptor y el subsecuente contacto directo entre células infectadas y células no infectadas. En estas circunstancias, los anticuerpos neutralizantes no pueden actuar; ya que las partículas virales potencialmente infectantes no están libres sino protegidas en el interior de la célula infectada.
El posible desarrollo de una vacuna efectiva contra el HIV depende de un cambio radical en la manera como se entiende el concepto de vacuna, ya que las vacunas antivirales clásicas (como la de la viruela o la de la poliomielitis) están dirigidas a estimular la inmuniad humoral específica (inmunidad por anticuerpos) y hasta la fecha no ha sido desarrollada una vacuna efectiva contra ninguno de los virus cuyo control depende directamente de la inmunidad celular específica (aquélla mediada primordialmente por linfocitos T citotóxicos que atacan a las células infectadas por estos agentes).
En vista de lo anterior, las mejores medidas para reducir el riesgo de infección por HIV son: verificar que la sangre y derivados de sangre utilizados con fines médicos (para transfusiones, etc.) se encuentren libres de contaminación por HIV; evitar el uso de drogas intravenosas y otros procedimientos que impliquen el intercambio de materiales e instrumentos potencialmente contaminados con sangre o células infectadas; evitar la promiscuidad sexual y utilizar condones durante el acto sexual.