I.¿QUÉ SON LAS ARCILLAS?
A ESTA pregunta sencilla le podemos buscar una respuesta de acuerdo
con el pensamiento de Campoamor: " ... todo es según el color, del cristal con
que se mira". Es decir que si desde el punto de vista geológico las arcillas
son minerales naturales que se formaron hace varios millones de años y que reúnen
las características peculiares de composición y formación relacionadas con el
curso de la evolución de la Tierra, para el artista constituyen los materiales
plásticos o los pigmentos que le permiten expresar, mediante formas y composiciones
de color, un estado de alma o de conciencia que puede ser bello.
Desde un punto de vista utilitario las arcillas han sido los materiales preferidos por el hombre para la manufactura de utensilios que sirven en la cocción y el consumo de sus alimentos, de vasijas de barro para almacenar y añejar el vino, de piezas finas de porcelana, así como pisos de mosaico y embaldosados.
La época moderna ha incorporado a las arcillas en numerosos productos de uso cotidiano a través de las nuevas tecnologías de modo que, aunque no lo percibamos, las arcillas forman parte importante de nuestras vidas. Un ejemplo son los nuevos materiales poliméricos que incluyen en su composición las arcillas minerales con el fin de lograr superficies suaves al tacto y propiedades mecánicas mejoradas, como en los juguetes, en las partes de automóvil y en otros componentes que son, además, resistentes a la flama y al desgaste. Algunos productos de alta tecnología incorporan a las arcillas en alta proporción, como los convertidores catalíticos que se utilizan en el control de emisiones contaminantes de los vehículos de motor, o bien en el papel incombustible con que se provee a los astronautas desde el accidente del Challenger o en las revistas de alta calidad.
Existen otras aplicaciones masivas de las arcillas minerales: los lodos de perforación de los pozos petroleros, los moldes de fundición y los catalizadores empleados en la refinación del petróleo.
No faltan las aplicaciones en el campo farmacéutico y en los productos de belleza, ya que las arcillas forman parte importante de los talcos desodorantes, jabones y cremas, pastas de dientes, etc. Pero ¡dejemos esa lista interminable!, y volvamos a la pregunta original: ¿Qué son las arcillas?
El diccionario nos dice lo siguiente:
| Las arcillas son las rocas blandas que se hacen plásticas al contacto con el agua, siendo frágiles en seco, y con gran capacidad de absorción. |
La Enciclopedia las define así:
| La arcilla es un silicato de aluminio hidratado, en forma de roca plástica, impermeable al agua y bajo la acción del calor se deshidrata, endureciéndose mucho. |
Encontramos pues una serie de conceptos que van más allá de la noción de "tierrita" que teníamos originalmente. Por ejemplo, los sedimentos referidos en la definición anterior son aquellos minerales naturales que se han depositado en los lechos de lagos y mares por la acción de arrastre de los ríos. El material granuloso puede ser tan fino que podríamos poner un gránulo en la pata de una mosca ¡sin que se entere de que lo lleva! Con la ayuda de un microscopio óptico podríamos amplificar la imagen de uno de estos granos hasta llegar a unas dos mil veces, pudiendo observar así el objeto de cuatro micras con el tamaño de un grano de arroz. No obstante, la rugosidad y la estructura interna del grano no son observables a esos niveles de amplificación. Necesitaríamos de un instrumento más poderoso: el microscopio electrónico, con el que es posible alcanzar una amplificación de unos quince mil aumentos. Así, el grano que veíamos antes como un grano de arroz ahora se nos convierte en una hojuela con los bordes curvados hacia arriba, tal y como se muestra en la figura 1. Esta hojuela se asemeja a las placas de barro en un suelo secado, contraído y agrietado por el Sol. ¿No es así? Ahora bien, ¿qué pasa si observamos la hojuela con mayor amplificación? Veremos que, a medida que aumenta el tamaño de la hojuela, nos vamos concentrando más y más en una pequeña porción del material, tal y como se muestra en la figura 2, donde observamos el borde de la hojuela a 200 000 aumentos, es decir que ahora un centímetro de la figura 2 equivale a ¡la veinteava parte de una micra, o sea a cinco millonésimas partes de un centímetro!, así, vemos en la figura 2 que, a esta escala, el borde de la hojuela parece formado por una serie de láminas apiladas una encima de la otra, dispuestas como si fueran las hojas de un libro, o de un pastel ¡mil hojas!, ¿no es así?
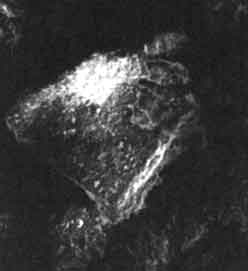
Figura 1. Hojuela de arcilla amplificada 15 000 veces.
Aún más, si ponemos en contacto a la arcilla con el agua, veríamos cómo las hojuelas se separan unas de otras, abriéndose, y si las secamos extrayendo el agua absorbida entonces observaríamos el efecto de contracción del espacio entre las láminas, ¡como si fuera un acordeón químico!
Se menciona en las definiciones precedentes que la arcilla es un silicoaluminato hidratado, es decir que desde el punto de vista químico está compuesta de silicio (Si), aluminio (Al), oxígeno (O) e hidrógeno (H). Por ello, nada más natural que comenzar nuestro tema echando una mirada a esa familia de minerales, los silicatos, que forman el árbol genealógico de las arcillas. Abrochemos pues nuestros cinturones y emprendamos la búsqueda de las características íntimas de las arcillas.

Figura 2. Borde de la hojuela amplificado 20 000 veces.
Aun con las técnicas modernas disponibles hoy en día, el conocimiento que tenemos
de la corteza terrestre es muy limitado, ya que sólo se ha explorado una pequeñísima
porción del casquete superficial, es decir aproximadamente los primeros cuatro
kilómetros a partir de la superficie, o sea el 0.062% del diámetro terrestre
(12 740 km). Sin embargo, mediante métodos indirectos, como los sismológicos,
se ha logrado poner en evidencia que la estructura interna de la Tierra, a semejanza
de una cebolla, está formada por capas que tienen una composición más o menos
definida: así, hacia el interior de la superficie encontramos la capa llamada
SIAL, situada entre los 40 y 100 km de profundidad, que es rica
en sílice (SiO2) y aluminio, es de tipo ácido y con una densidad
media de 2.7. Más hacia el interior hallaremos la capa denominada SIMA,
rica en hierro y magnesio pero con algunas porciones de sílice, aluminio y otros
elementos, de carácter básico, más caliente y fluida que la capa SIAL.
La capa SIMA es considerada la madre directa de todas las formaciones
minerales que afloraron a la superficie. Es decir, que es muy probable que las
primeras rocas superficiales se hayan formado por el enfriamiento y cristalización
posterior de las corrientes de magma provenientes de la capa SIMA,
acarreadas por las erupciones volcánicas y enfriadas en la superficie, dando
origen a las rocas básicas como los basaltos. En cambio, la afloración del material
fundido proveniente de la capa SIAL, a través de las hendiduras
y fallas, originó la formación de las rocas ígneas de carácter ácido: los granitos.
Las segregaciones del magma caliente, su migración y su compactación posteriores,
dieron origen a diversos minerales, como las cromitas, magnetitas, corindón,
sienitas, mármoles y cuarcitas, entre otros. Unos más resultaron de la presión
de los suelos al replegarse, como ocurrió con el grafito.
La acción de los vapores y de los gases calientes sobre las primeras rocas condujo a su alteración y a la consecuente formación de mezclas finas de minerales. Estas últimas permanecieron en forma de residuos o bien fueron transportadas y depositadas en los lechos de los ríos y en los fondos marinos. El arrastre y depósito de esas mezclas finas pudo efectuarse por vía fluvial, es decir, por acción de los ríos o bien por medio de los glaciares y los vientos. El resultado fue su depósito en los lechos lacustres y marinos, lo cual produjo los yacimientos más importantes.
Por lo anterior, es fácil aceptar que el 95% de la corteza terrestre está formada por silicatos. La corteza tiene una densidad media de 2.7, mientras que la densidad media de la Tierra es de 5.5, o sea que en el interior se concentran los elementos más pesados, hierro, níquel, etcétera.
Pero, ¿por qué son importantes los silicatos? A esta pregunta que el lector pudo haber formulado se le ha de buscar una respuesta que ya fue mencionada en la primera parte de esta obra: Los silicatos forman el árbol genealógico de las arcillas.
La familia de los silicatos comprende la mayoría de los minerales de la corteza terrestre, incluido el cuarzo y, como veremos, su composición y estructura están relacionados directamente con la historia geológica de la Tierra, es decir, que dependen de la naturaleza de la roca madre que les dio origen, así como del ambiente a que fueron sometidos durante la etapa de arrastre o deposición. Las arcillas son, pues, una rama de los silicatos y su formación obedeció a tres mecanismos principales: 1) por herencia, 2) por neoformación y 3) por transformación. El primer mecanismo indica que el material arcilloso fue derivado directamente de una roca madre y es este tipo de arcillas el que predomina en los sedimentos de lagos y mares.
Los otros dos mecanismos implicaron una reacción química entre varios componentes —o bien a partir de la arcilla original—, por lo que este tipo de formación requirió de mayor energía y de ciertas condiciones hidrotérmicas. Curiosamente, estos mecanismos están relacionados con la latitud en el planeta, de modo que encontramos que el primer mecanismo fue más común en las regiones árticas, mientras que la neoformación y la transformación resultaron dominantes en los trópicos húmedos. A las arcillas que se presentan en la naturaleza como una pasta suave se les llama "lodos", mientras que aquellas que tienen la apariencia de un sólido blancuzco se les denomina piedra lodosa o bien roca laminada (en inglés: shale). Es importante que a los depósitos de arcilla se les nombre arcillosos, a fin de distinguirlos de los depósitos arenosos y además plásticos, a fin de diferenciarlos de las rocas ígneas.
A continuación se presenta un glosario de los apelativos más comunes de algunas arcillas:
arcilla figulina: es aquella que contiene impurezas como la arena, la caliza y los óxidos de hierro.
arcilla refractaria: es rica en óxidos metálicos y tiene la propiedad de ser muy resistente al calor.
arcilla roja: esta clase la integra generalmente un depósito de tipo marino formado por los restos de materiales calcáreos y ferrígenos, polvo volcánico, restos de esponjas silíceas, dientes de tiburón, etc. El color rojizo proviene por lo común de sus componentes férricos. Se ha encontrado que estos depósitos son muy extensos, y cubren hasta el 60% de la superficie marina.
arcilla ferruginosa: contiene en su composición diferentes cantidades y tipos de óxido de hierro y puede ser de color amarillo, ocre e inclusive negra (tierras de Siena) debido al óxido de hierro hidratado, mientras que las arcillas rojas contienen, por lo general, un óxido conocido como hematita. Esta particularidad de las arcillas explica por qué en algunas regiones el barro es negro o rojizo, lo cual incide en los colores de la cerámica que se fabrica a partir de estos materiales. Recordemos en este punto al barro negro de Oaxaca, tan distinto de la cerámica ocre o rojiza de la zona central del valle de México.
arcilla magra y arcilla grasa: estos materiales contienen cierto grado de impurezas, lo que afecta sus propiedades plásticas, es decir, que a mayor contenido de impurezas se obtiene una pasta menos plástica (arcilla magra) al amasarla con agua.
arcilla de batán: llamadas también tierra de batán, debido al uso que tuvieron en el "batanado" de las telas y de las fibras vegetales como el algodón. Este proceso consistía en limpiar las fibras formadas en la máquina (batán) eliminando la materia grasa mediante la adición de arcilla, por lo general del tipo esmectita, cuyo nombre proviene del griego smektikós: "que limpia."
arcilla marga: es un material impermeable y frágil, con un contenido de caliza de entre 20 y 60%, aproximadamente.
arcillas de esquisto o pizarra: las constituyen formaciones antiguas que se presentan en forma de estratos o de plaquetas paralelas que se han dividido por la presión del suelo.
arcilla atapulgita: también conocida como tierra de Florida o floridrín, aunque algunas veces se la llamó tierra de Fuller. El último apelativo se empleó también para denominar a las sepiolitas. Actualmente la atapulgita es llamada paligorskita.
arcilla bentonita: nombre comercial de las arcillas tipo montmorillonita,
las que, tratadas con compuestos químicos aminados (p. ej. dodecilamonio)
se vuelven repelentes al agua —hidrofóbicas—, aunque mantienen gran
afinidad por las especies orgánicas, en particular los aceites, las grasas
y los colorantes o pigmentos naturales. El nombre bentonita proviene de Fort
Benton, Wyoming, EUA, donde W. C. Knight descubrió un enorme
yacimiento de este tipo de arcilla en 1896.
FORMACIONES ARCILLOSAS EN MÉXICO
Los trabajos de investigación realizados por Enciso (1968) y De Pablo (1990) indican que el territorio nacional estuvo sujeto a una gran actividad volcánica durante los periodos Oligoceno-Mioceno, lo cual provocó la formación de enormes depósitos de rocas vidriosas que a su vez fueron alteradas y dieron origen a la mayor parte de las arcillas que encontramos en México. Estas son, por lo regular, del tipo montmorillonita y sus formaciones más abundantes se localizan al norte del país, en el Estado de Durango, siendo las de Cuencamé, Velardeña, Pedriceña, Rodeo y Nazas las más conocidas y las que actualmente se encuentran en explotación.
También existen depósitos importantes en Puebla, en los límites de Tlaxcala y Puebla, en Chupaderos, Zacatecas, en Oaxaca, en Neutla, Guanajuato, en Huayacocotla, Veracruz y en numerosas formaciones menores localizadas en las antiguas zonas lacustres como el valle de México (Figura 3).
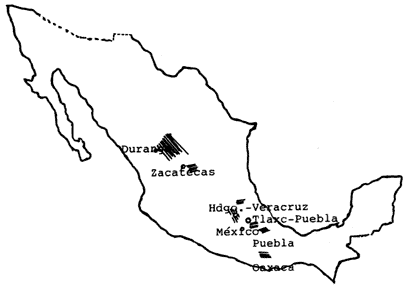
Figura 3. Depósitos arcillosos en México.
Sin duda la zona localizada en Durango es la más extensa y se sabe ahora, gracias a los trabajos de Enciso y De Pablo que esas arcillas fueron originadas por la alteración de las rocas piroplásticas depositadas previamente en el valle por medio de una nube ardiente. La subsecuente alteración de tales rocas ígneas y la deposición del material alterado en suelo seco dio origen al mineral arcilloso más rico en potasio, como el de la zona de Vizcarra, mientras que el mineral depositado en la zona lacustre (de origen marino aparentemente) se alteró y produjo las arcillas color verde y rosa típicas de la región de Cuencamé. Estas formaciones se encuentran a una altura de 1 340 m sobre el nivel del mar, en el valle de Cuencamé-La Lagunilla, que se extiende hasta Pedriceña y por el oeste hasta Rodeo y Nazas, donde la altura disminuye a 1 128 m. Esta zona contiene los depósitos más importantes de México, que representan un gran potencial económico. En su mayor parte la calidad de la arcilla es superior, del tipo montmorillonita expandible, y ocurre en concentraciones variables según la zona, es decir 85% en la región de Pedriceña, 50 a 70% en Nazas, un 50% en Las Cuevas y una porción variable en Cuencamé. En esta última se encuentran frentes de color blanco y rosa con espesores entre 2 y 6 m, mientras que la arcilla que se encuentra en contacto con el polvo alterado tiene sólo un espesor de 50 cm y su color es verde, cambiando luego a rosa y presentando frentes de hasta 4 y 8 m de espesor.
Las arcillas o lodos heredados de los continentes y depositados, neoformados o transformados, en los lechos marinos, lacustres, fluviales o estuarinos, han provocado cambios espectaculares en el planeta Tierra. Que digan si no es así la formación del petróleo, la de las moléculas orgánicas prebióticas que dieron origen a la vida y la de los suelos agrícolas, sin mencionar el surgimiento de las civilizaciones que hicieron uso del barro cocido en la manufactura de su cerámica.
En efecto, la mayor parte de las cimas de los yacimientos de petróleo de las
costas del Golfo de México (EUA-México) ocurren a la profundidad
en la que usualmente se produce la transformación de las arcillas tipo esmectita
(E) en las denominadas illitas (I). Ambas tienen la misma estructura
laminar, como se verá en detalle más adelante, excepto que las segundas no son
expandibles debido a las fuertes cargas electrostáticas que mantienen a las
hojas ligadas. Así, la transformación de la esmectita en illita pudo haber desempeñado
papel importante en la génesis del petróleo: al ser contenidas las moléculas
orgánicas en el interior del espacio interlaminar de la esmectita, aquellas
estaban "protegidas" de la oxidación y sujetas a un proceso de tipo catalítico
que pudo haberlas convertido en petróleo, tal y como ahora lo conocemos. Pero
es un hecho experimental que la sustitución del silicio (Si) por aluminio
en las hojas que componen el acordeón químico de la esmectita, origina
un exceso de carga electrostática negativa en las hojas, de tal magnitud a escala
molecular que provoca la deshidratación del potasio (K), el cual se encuentra
comúnmente en el espacio interlaminar de las arcillas. Luego, el agua así expulsada
pudo haber acarreado en su paso a los hidrocarburos formados en el interior
de las arcillas, mientras que la contracción subsecuente de las hojuelas de
arcilla deshidratada podría haber provocado un colapso en el material, dejando
hendiduras y poros por los que pudo migrar el fluido hacia los recipientes rocosos.
Por otro lado, la estructura laminar de las arcillas permite el almacenamiento de agua en el espacio interlaminar, formando así agregados lodosos difíciles de romper. La combinación de la arcilla con la materia orgánica del suelo y algunos óxidos minerales contribuye a la estabilidad estructural necesaria para resistir los efectos mecánicos destructivos. La porosidad interna de las hojuelas de arcilla y su carga electrostática asociada son adecuadas para la absorción de especies tales como los cationes de potasio (K+), magnesio (Mg++) y amonio (NH4+), los cuales son liberados bajo condiciones ácidas apropiadas, pudiendo ser absorbidos por las raíces de las plantas.
La acidez es provocada por una acumulación de iones de hidrógeno (H+) provenientes de compuestos químicos disueltos en el agua y acarreados por las lluvias; en ellos la concentración ácida llega a ser tal que algunos de los otros cationes atrapados por las arcillas, como los iones Al3+ se disuelven rápidamente en las soluciones, pasando a las raíces vegetales y provocando efectos tóxicos en las plantas. Es por ello que un suelo fértil debe estar balanceado en lo que a la acidez se refiere y el tratamiento en este caso consiste en la neutralización de la acidez mediante la agregación de compuestos alcalinos, como el carbonato de calcio. Luego tenemos que la combinación de acidez e intercambio iónico en las arcillas del terreno es importante en el desarrollo de los suelos agrícolas.
Éstos, en la actualidad, se encuentran expuestos a las contaminaciones por lluvia ácida proveniente de las zonas industriales y por los abonos químicos y plaguicidas, los cuales son absorbidos por las arcillas minerales provocando los efectos combinados de acidez e intercambio mencionados. En cualquier caso, las arcillas son las protagonistas en la formación de los suelos agrícolas y sus propiedades son determinantes para el crecimiento de los vegetales. Por otra parte, la mineralogía del suelo es resultado de diversos factores, el clima y el intemperismo, así tenemos que en las regiones tropicales predominan los caolines mezclados con óxidos minerales (oxisoles) y los suelos negros formados por esmectitas expandibles (vertisoles) combinadas. Si la acidez es baja (pH > 6) el suelo arcilloso tiende a ser rico en calcio, en cambio si la acidez es alta (pH < 6) el aluminio tiende a ser más abundante, lo que trae efectos tóxicos para la vegetación. Otros cationes, como el amonio, los nitratos y los fosfatos, también son retenidos por las arcillas del suelo e intercambiados bajo condiciones de humedad y acidez adecuadas, siendo realmente accesibles a las plantas y representando una fuente importante de nutrientes. La composición óptima del suelo debe incluir una fracción de arcilla compuesta de partículas menores a 2 micras, y una proporción mayor de sedimentos con tamaños de partícula entre 2 y 60 micras. Esta combinación parece incluir las mejores características para el cultivo y crecimiento de las raíces vegetales. Es claro, pues, que las arcillas son los componentes del suelo que provocan la mayor influencia en su productividad.
No menos importante ha sido la interacción de las arcillas con las moléculas orgánicas. Su afinidad por las bases orgánicas nucleicas, como la guanina, la citosina, etc., ha provocado interés creciente entre la comunidad científica que trata de atribuir un papel preponderante a los compuestos minerales de tipo laminar en la formación de las moléculas prebióticas. Más adelante, en el capítulo III, se ampliará esta idea con base en una mejor comprensión de la estructura de las arcillas y su posible relación con el origen de la vida en el planeta.
Otros usos de la interacción del barro (arcilla) con las moléculas orgánicas
lo encontramos en la manufactura de la cerámica en la antigüedad. Baste mencionar
el uso que los griegos daban a los pigmentos vegetales para la obtención de
la cerámica negra y roja, típica del arte de Micenas. Otros ejemplos más sorprendentes
los encontraremos en el curso de esta obra en la que estudiaremos la porcelana
china del periodo Sung (969-1279 d.c.), la llamada porcelana de "cáscara
de huevo" que, debido a su fineza y alta resistencia sorprendió al mundo occidental.
Su delicadeza era tal que ya en el siglo IX se hablaba de los vasos
de porcelana china translúcida, que dejaban ver los líquidos contenidos en su
interior. Se decía que las piezas de porcelana de esta clase trascendían a la
naturaleza humana. En cualquiera de los casos precedentes, la arcilla mineral
ha sido la protagonista y, gracias a su abundancia natural y accesibilidad,
el barro tradicional ha tenido un papel importante en el desarrollo de las primeras
civilizaciones. Desde muy temprano, el hombre observó que los objetos de barro
húmedo se contraen y endurecen al secarse por la acción del calor y que su resistencia
mecánica en esas condiciones es suficiente. Aunque estas propiedades son tan
familiares que hacen pensar en una serie de características simples, ha tomado
muchos años desentrañar los secretos que dieron origen a las propiedades mencionadas.
Ahora que se cuenta con instrumentos analíticos poderosos y con métodos de cálculo
avanzados, la sorpresa ha sido mayúscula al comprobarse que donde se esperaba
encontrar una estructura simple y rígida, se tiene un arreglo complejo y flexible.
Se ha venido encontrando que el horizonte llano presenta en realidad profundos
abismos y montañas en lo que se refiere a la física y la química de las arcillas
minerales. Un tema de investigación que parecía pertenecer al pasado se descubre
ahora como fuente inagotable de nuevos conocimientos y nuevas aplicaciones.
Todas estas características sólo hablan de la nobleza de un material y nos dan
la esperanza de que con el polvo se han de construir y transformar grandes cosas
para beneficio del hombre.
EL ÁRBOL GENEALÓGICO: LOS SILICATOS
No fue sino hasta el año de 1912 cuando, gracias a los físicos W. L. Bragg y M. Laue, que descubrieron las propiedades de los rayos X, fue posible desentrañar la estructura interna de los minerales. Estos son compuestos cristalinos, es decir, que a escala molecular están formados por planos y caras muy bien definidos, los cuales tienen la propiedad de dispersar los rayos X y producir así patrones de interferencia, los cuales nos proporcionan información muy valiosa sobre los arreglos cristalinos de las sustancias minerales.
Después, con el microscopio electrónico, desarrollado por primera vez por E. Ruska en 1931, fue posible observar directamente los cristales minerales, su forma y su geometría.
Mediante las técnicas apuntadas, se sabe que los silicatos están formados por cristales regulares y, si vamos a una escala más pequeña, veríamos que estos cristales tienen a su vez una unidad básica: el tetraedro (en, griego "cuatro caras"), tal y como se ilustra en la figura 4. Este es el tabique elemental con que podemos construir los edificios moleculares que forman a los silicatos, ¡interesante!, ¿no es así? Veamos más de cerca cómo se piensa que esto ocurre.
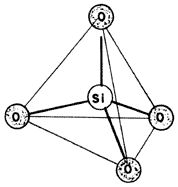
Figura 4 (a). El tetraedro elemental o la pirámide triangular.
El tetraedro de la figura 4 está compuesto por un átomo central de silicio (Si) y cuatro átomos de oxigeno en las esquinas (O).
Si cada átomo de silicio tiene cuatro cargas eléctricas positivas, mientras que cada átomo de oxígeno tiene dos cargas negativas, es necesario que cada uno de los átomos de oxígeno use una de sus cargas para atraer a una de las cargas del silicio, quedando así saturado el átomo central (Si), mientras que las esquinas todavía tienen una carga negativa para enlazarse a otro átomo con carga positiva. Cuando esto último ocurre, entonces tenemos que se puede formar una cadena de tetraedros, mediante los enlaces del tipo: ..-.O-Si-O-Si-O-Si-O-...
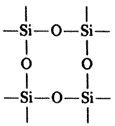
Similarmente, mediante este mecanismo podemos formar cadenas verticales que se unen a las cadenas horizontales para formar redes, de la manera siguiente: si seguimos armando este "Mecano", podemos superponer una red encima de otra, a manera de formar arreglos tridimensionales. También podemos sustituir uno de los átomos de silicio por otro, por ejemplo de aluminio (Al), con lo cual el arreglo quedaría desbalanceado, ya que el aluminio sólo tiene tres cargas eléctricas positivas en vez de cuatro, dejando una carga negativa "extra" en uno de los átomos de oxígeno, por ejemplo:
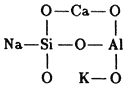
Como se observa en este esquema, la carga negativa desbalanceada puede ser satisfecha por un catión positivo, por ejemplo el sodio (Na) o el potasio (K), con lo cual se logra nuevamente una estructura neutra.
Existen dos reglas básicas que nos dicen cómo unir dos o más tetraedros (Reglas de Pauling):
1) La suma de las cargas negativas debe ser igual a la suma de las cargas positivas, de manera que la estructura sea eléctricamente neutra.
2) Todos los elementos con carga positiva (cationes) pueden enlazarse o rodearse de elementos cargados negativamente, coordinándose con ellos de modo que los arreglos coordinados dependen únicamente de los tamaños entre el catión (+) y el anión (-) respectivo.
Existe una tercera regla conocida como Regla de Lowenstein: No es válido enlazar dos tetraedros que tengan un átomo central de aluminio cada uno. Esto nos indica que dos tetraedros de aluminio sólo pueden enlazarse mediante otro tetraedro intermedio a base de silicio.
Siguiendo estas sencillas reglas podemos armar el mecano de manera que un tetraedro (1T) pueda unirse a otro para formar un arreglo tipo 2T (dos tetraedros) o bien 3T, ..., etc. Así, en la figura 5 (a) se reúnen todas las posibles combinaciones de tetraedros que dan origen a una serie de vistosas geometrías, en forma de cadena simple, doble, redes de motivos hexagonales, etc. Lo más sorprendente es que cada uno de estos arreglos es típico de alguno de los silicatos minerales más conocidos. Así vemos que el mineral circón está compuesto de tetraedros aislados (1T), mientras que los piroxenos por cadenas simples de un número infinito de miembros (nT). En particular, las redes de tetraedros que se extienden a lo largo y a lo ancho, formando hojas completas, constituyen el grupo de filosilicatos, o estructuras laminares, del que forman parte las arcillas.
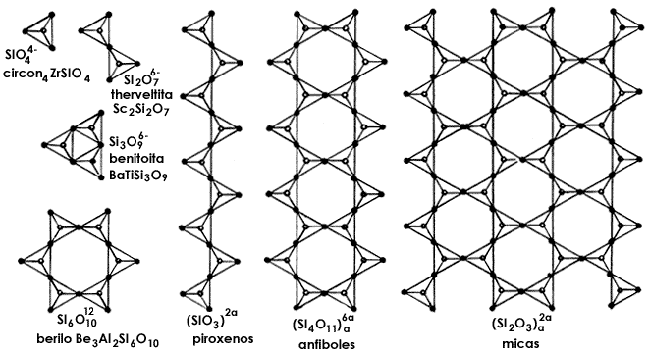
Figura 5(a). La estructura de los silicatos, o el mecano
Una propiedad extraordinaria de estas estructuras es su posibilidad de ser capaces de sustituir al átomo de silicio (Si), situado en el centro de los tetraedros (Figura 4), por otro de menor carga como el aluminio (A13+), generando así una deficiencia de carga positiva, o un exceso de carga negativa en el tetraedro, la cual necesita atraer a otros cationes para compensarse, por ejemplo Na, K, Ca, ... , etc. Este es el mecanismo que permite a los silicatos tener propiedades superficiales únicas de acidez e intercambio iónico, tan importantes que a ellas se deben las propiedades catalíticas de las arcillas. Esto es un ejemplo típico de lo que ocurre a menudo en la química, es decir, que los arreglos cristalinos, las sustituciones, etc., representan aspectos físicos, que ocurren a escala molecular, estableciendo o modificando las propiedades químicas de los materiales: fundamento de las propiedades químicas de las sustancias es la física que ocurre a escala molecular.
LA ESTRUCTURA DE LAS ARCILLAS: ¡QUIÉN ES QUIÉN!
Hemos visto cómo la unión de varios tetraedros nos genera hojas que se extienden a lo largo y a lo ancho, dando origen a las estructuras laminares. Veamos de cerca qué ocurre al unir los vértices para formar anillos tipo 6T (seis tetraedros), como se muestra en la figura 5 (b). Las puntas de los tetraedros se encuentran a la misma altura, formando un plano, de igual manera ocurre con los átomos de silicio situados en el centro de los tetraedros y con los de oxígeno situados en las bases. La articulación de esos tres planos nos conduce pues a la formación de una hoja tetraédrica (tipo T).
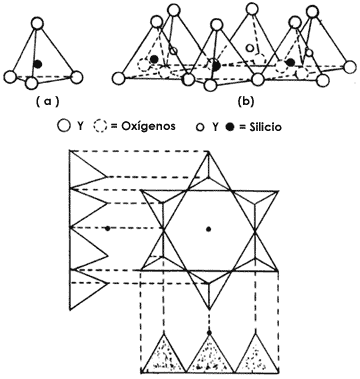
Figura 5 (b). El anillo de seis tetraedros.
Siguiendo esta secuencia, podemos ahora unir dos hojas para formar una lámina tetraédrica, tal y como se ilustra en la figura 6. En ésta se observa que las dos hojas se encuentran invertidas, una con respecto a la otra, compartiendo uno de los vértices.
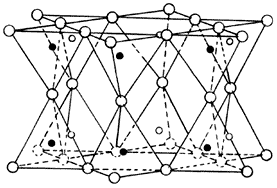
Figura 6. Una lámina de tetraedros (T).
Similarmente, existen otros cuerpos poligonales que podemos unir entre sí para formar cadenas, tal y como ocurre con el octaedro (octa, ocho; edros, cara), representado en la figura 7, formación típica de los compuestos de aluminio, por ejemplo Al (OH)6, o del magnesio. Este arreglo es una hoja octaédrica (tipo O).
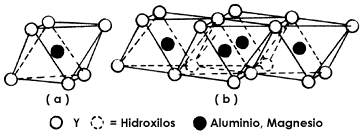
Figura 7. Una hoja de octaedros (O).
Ahora bien, la unión de una hoja del tipo T, con otra del tipo O, genera una lámina T- O, o lámina 1:1, tal y como se ilustra en la figura 8. La coincidencia, sin embargo, no es perfecta cuando se trata de hojas T formadas por silicio-oxígeno y de hojas tipo O formadas por aluminio-oxígeno-oxhidrilo, lo cual crea un efecto de esfuerzo entre las hojas que es de gran importancia para algunas de las aplicaciones de las arcillas que presentan este tipo de láminas (T-O), por ejemplo el caolín.
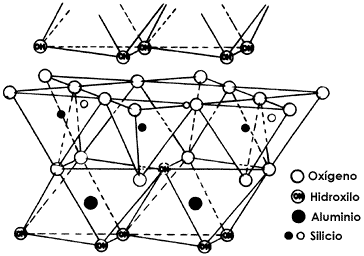
Figura 8. Una lámina T-O.
Ahora terminamos la secuencia agregando una tercera hoja tipo T a la lámina T-O mencionada arriba y el resultado se ilustra en la figura 9, que muestra la lámina T-O-T, o, como algunos lectores perspicaces la llaman: la estructura de sandwich, debido a que dos hojas tipo T se asemejan a los panes del sandwich, mientras que el jamón correspondería a la hoja tipo O. Esta lámina tiene pues dos hojas T y una hoja O, o sea la lámina es del tipo 2:1.
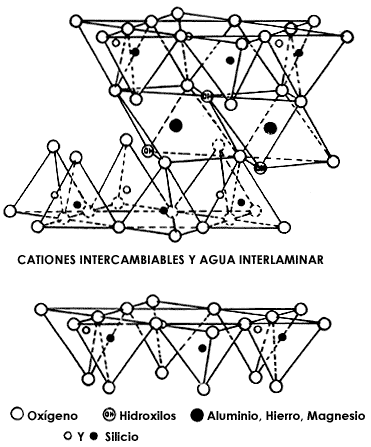
Figura 9. Una lámina T-O-T.
Hasta aquí termina el juego del mecano, ya que la lámina T-O-T es la más completa y no acepta una nueva adición, debido a la saturación de los enlaces. Una cosa es clara en este punto: las estructuras de sandwich son nada menos que ¡la parte esencial de las arcillas! Por si hubiese alguna duda al respecto, pasaremos ahora a ilustrar la importancia de las estructuras formadas por las láminas tipo 1:1 y aquellas formadas por las láminas tipo 2:1.
El nombre caolín proviene de la voz china Kau-Ling, nombre del cerro de una
región situada al norte de China de donde se extraía esta arcilla desde el siglo
VIII d.C., para la fabricación de la porcelana. La unidad fundamental
de la estructura del caolín es la lámina T-O, o sea la lámina 1:1, una
hoja de tetraedros de silicio-oxígeno unida a otra hoja de octaedros de aluminio-oxígeno-OH.
La sustitución del silicio por otro elemento, como el aluminio, o bien la sustitución
del aluminio en la hoja tipo O por otro elemento de menor carga, por
ejemplo el magnesio, causa un cambio químico en el material pero mantiene esencialmente
la misma estructura. Estas sustituciones dan origen a la familia de los caolines
(Figura 10).
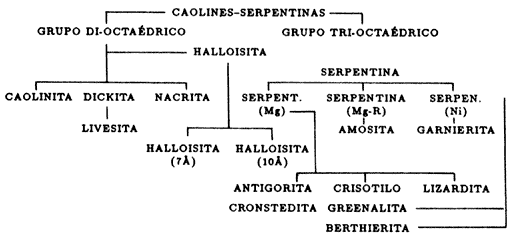
Figura 10. El árbol de los caolines.
La primera rama comprende a aquellos minerales derivados de la caolinita que guardan la misma composición química por cada unidad estructural:
éstos son la nacrita, dickita, anauxita, halloisita y el alofano, los cuales difieren entre si sólo por su arreglo laminar. Imaginemos un paquete de naipes en el que todas las cartas se encuentran ordenadas perfectamente: ésta es la estructura de la nacrita (Figura 11). En este caso el paquete de cartas puede llegar a ser muy alto debido a que la estructura ordenada es más estable.
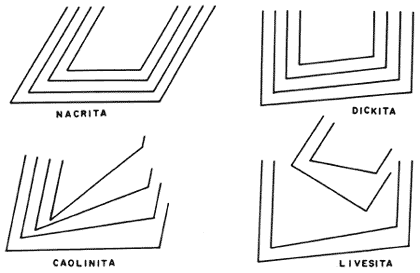
Figura 11. La baraja de los caolines.
En cambio, la dickita está dispuesta de tal manera que el paquete de naipes se abre más de un lado que del otro, entre 6 y 7 grados, mientras que la caolinita se abre hasta 15 grados.
Existe un mineral asociado (livesita) que presenta una abertura a un lado que es siempre regular, mientras que la carta siguiente se abre de forma irregular hacia el otro lado, dando origen a una estructura laminar muy desordenada y poco estable.
El otro grupo de caolines es igualmente importante y comprende el mismo tipo de estructura laminar, pero con una sustitución del aluminio de la hoja tipo O por otro catión, por ejemplo el hierro (Fe2+, Fe3+) o el magnesio (Mg2+). Sin embargo, al sustituir el aluminio por el magnesio se contraen ligeramente las dimensiones de la hoja tipo O, originando una pequeña distorsión en la lámina T-O, la cual permite acomodar el esfuerzo pero ocasiona que la forma externa de los cristales de este tipo sea fibrosa o corrugada, tal es el caso de los asbestos (crisotilo) y la antigorita, respectivamente.
Una última observación: en las estructuras de estos derivados del caolín se ve que sus hojas se ensamblan naturalmente unas sobre otras, como las cartas de una baraja, con las variaciones mencionadas arriba, de modo que entre una hoja y otra hay un enlace muy débil, del tipo Van Der Waals, creando un espacio interlaminar que guarda propiedades muy interesantes, como veremos más adelante.
La familia de las esmectitas está formada por todas aquellas arcillas que presentan una estructura de ¡sandwich!, es decir, que está constituida por dos hojas de tipo T y por otra intermedia de tipo O. La fórmula estructural típica de estas arcillas es la siguiente:
|
Al2
|
Si4
|
O10
|
(OH)2
|
|
hoja
|
hoja
|
||
|
octaédrica
|
tetraédrica
|
Esta estructura es eléctricamente neutra debido a que todas las posiciones en la hoja T se encuentran ocupadas por átomos de silicio, mientras, que todas las posiciones de la capa O contienen aluminio. Ésta es la fórmula típica de la pirofilita. Sin embargo, tal y como se muestra en la figura 12, existen numerosas ramas en el árbol de las arcillas, las cuales presentan la misma estructura de sandwich, excepto que algunas veces el aluminio sustituye al silicio parcialmente en la capa T, o bien el magnesio o el hierro sustituyen al aluminio en la capa O, e inclusive el flúor (F) pudiera sustituir al oxígeno de la capa O. Luego, estas diferencias de composición química hacen que las propiedades de cada arcilla mineral sean distintas.
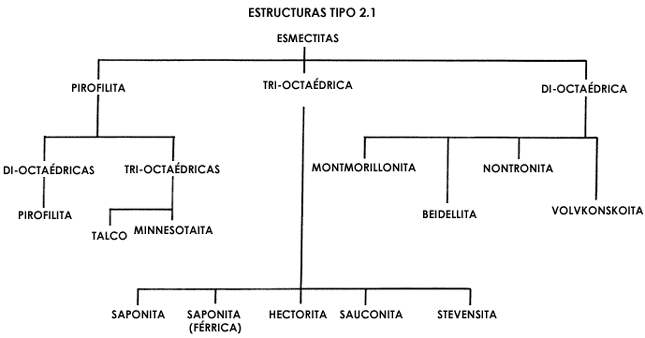
Figura 12. El árbol de las esmectitas.
Entre todas las esmectitas, la rama de las arcillas di-octaédricas presenta propiedades muy interesantes, derivadas por supuesto de su estructura laminar, de su espacio interlaminar y de la carga residual. La figura 13 ilustra la composición de las láminas T-O-T para todas las arcillas del tipo esmectita, es decir, las láminas tipo 2:1. Entre ellas destaca la montmorillonita, cuyo nombre se deriva del francés Montmorillon, lugar de Francia en que se encontró esta arcilla típica en 1874. La composición química de una arcilla esmectita, tipo montmorillonita, es la siguiente:
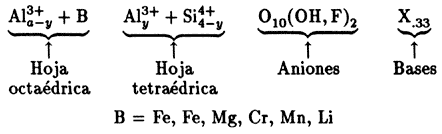
Como se observa en esta fórmula estructural, la hoja tetraédrica está compuesta sólo de silicio y aluminio mientras que la hoja octaédrica contiene aluminio y una variedad de cationes (B). Esto ilustra perfectamente la gran variedad de arcillas tipo esmectita que se pueden conseguir simplemente cambiando el catión de la hoja octaédrica y manteniendo ocupada la hoja T con Si y Al (Figura 13), para cada caso. Por supuesto, la sustitución de aluminio (O) y silicio (T) por un catión de menor carga eléctrica, por ejemplo Mg, origina una deficiencia de carga eléctrica que es responsable de algunas de las propiedades superficiales más importantes de las arcillas: la capacidad de intercambio, la absorción de moléculas polares como el agua, así como de otros compuestos orgánicos, por ejemplo las aminas, las cuales al introducirse en el espacio interlaminar causan el hinchamiento de la estructura laminar de las arcillas.
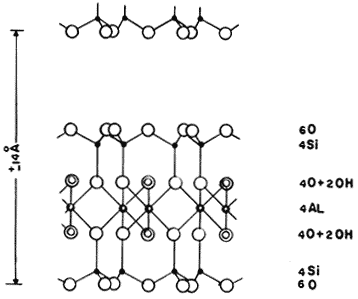
Figura 13. La composición de la lámina de T-O-T.
Debido a su avidez por el agua y las moléculas orgánicas las montmorillonitas encuentran aplicaciones muy variadas que van desde la extracción de esencias naturales hasta la fabricación de catalizadores para procesar los hidrocarburos derivados del petróleo. Los mecanismos que intervienen a escala molecular para llevar a cabo estas reacciones serán explicados en los capítulos siguientes, por ahora sólo mencionaremos que: la estructura de ¡sandwich! y el grado de sustitución catiónica determinan en gran medida las propiedades de las arcillas.
Más aún, la sustitución de cationes se lleva a cabo mediante mecanismos muy sencillos. La figura 14 muestra la fórmula estructural de las arcillas tipo esmectita, en donde podemos apreciar las sustituciones que se realizan en las hojas de cada uno de los minerales.
|
|
||
|
Mineral
|
Carga
|
Composición
|
|
(octa) (tetra) O10 (OH)2
|
||
|
|
||
|
Pirofilita
|
( E = 0 )
|
Al2 Si4 O10 (OH)2
|
|
Talco
|
"
|
Mg3 Si4 O10 (OH)2
|
|
Minnesotaita
|
"
|
(Fe, Mg)3 Si4 O10 (OH)2
|
|
Saponita
|
( E+ = 0.33 )
|
Mg3 (Si3.6, Al.33)
O10 (OH)2 nH2O
|
|
Saponita férrica
|
"
|
(Fe2+, Mg)3 (Si3.6,
Al.33) O10 (OH)2 nH2O
|
|
Hectorita
|
"
|
(Mg2.6, Li.33) Si4
O10 (OH)2 nH2O
|
|
Sauconita
|
"
|
(Mg, Zn)3 (Si3.6, Al.33)
O10 (OH)2 nH2O
|
|
Stevensita
|
( 2E+ = 2x )
|
Mg3-x Si4 O10
(OH)2
|
|
Montmorillonita
|
( E+ = 0.33 )
|
(Al1.67, Mg.33) Si4
O10 (OH)2 nH2O
|
|
Beidellita
|
"
|
Al2 (Si3.6, Al.33)
O10 (OH)2 nH2O
|
|
Nontronita
|
"
|
Fe23+ (Si3.6, Al.33)
O10 (OH)2 nH2O
|
|
Volkonskoita
|
"
|
(Al, Fe3+, Cr)2 (Si, Al)4
O10 (OH)2 nH2O
|
|
|
||
|
Figura 14. Arcillas esmectitas del grupo 2:1. Fórmula química. |
||
Existe otra familia de arcillas que se asemeja a la de las montmorillonitas: las vermiculitas, que tienen la misma estructura de sandwich, pero que pueden presentar un grado de sustitución mayor en la hoja octaédrica, originando una carga residual mayor que las montmorillonitas y, por eso mismo, la atracción entre las láminas es mayor también, por lo que la estructura no es tan expansible.
Las micas son los minerales clasificados como arcillas que tienen la misma estructura que las esmectitas, excepto que el grado de sustitución y la naturaleza de los cationes que se alojan entre láminas, por ejemplo el potasio, hacen que la carga residual sea muy alta. En estas condiciones, las láminas se fijan unas a otras haciendo que su estructura no sea expansible, ni sus cationes interlaminares intercambiables. La familia de las micas se ilustra en la figura 15 y la fórmula estructural en la figura 16.
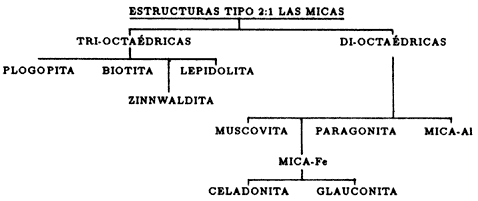
Figura 15. El árbol de las micas.
|
|
||
|
Mineral
|
Carga
|
Fórmula
|
|
|
||
|
Plogopita
|
( E+ = 1 )
|
KMg3 (Si3Al) O10
(OH)2
|
|
Biotita
|
"
|
K (Mg, Fe2+, Fe3+, Mn)3
(Si3Al) O10 (OH)2
|
|
Lepidolita
|
"
|
K (Al, Li)3 (Si, Al)4 O10
(OH)2
|
|
Sinnwaldita
|
"
|
K (Al, Li, Fe2+, Fe3+ )3
(Si, Al)4 O10 (OH)2
|
|
Muscovita
|
"
|
KAl2 (Si3Al) O10
(OH)2
|
|
Paragonita
|
"
|
NaAl2 (Si3Al) O10
(OH)2
|
|
Mica-Al
|
( E+ = 1 )
|
Kx (Al, Mg)2 (Si, Al)4
O10 (OH)2 NH2O
|
|
Mica-Fe
|
( E+ = 1 )
|
KMgFe3+Si4 O10 (OH)2
|
|
Celadonita
|
||
|
Mica-Fe (Glauconita)
|
K (R1.33+ R.672+)
(Si3.6 Al.33) O10 (OH)2
|
|
|
|
||
|
Figura 16. Micas, fórmula química y formas estructurales. |
||
El lector recordará la facilidad con la que la mica común se parte a lo largo de las hojas que la componen, pero, ¡qué difícil es partirla en la dirección perpendicular! ¿no es así? Esto ilustra perfectamente la constitución laminar de tales minerales. Además, conociendo la estructura podemos explicarnos fácilmente por qué las micas son buenos alsiantes térmicos, por ejemplo en las planchas eléctricas y en las conexiones: debido al espacio interlaminar, el cual no es un buen conductor térmico o eléctrico (las hojas se encuentran "desconectadas" unas de otras, lo que impide el paso del fluido térmico o eléctrico).
En contraste con la montmorillonita, la cual tiene una deficiencia de carga localizada en el centro de los octaedros, la carga residual de las micas está localizada en la hoja tetraédrica, es decir, en la superficie misma de las hojas, originando un amarre fuerte de los cationes interlaminares con las hojas, por lo que la estructura no es fácilmente expansible. Entre las micas más conocidas se encuentran la muscovita, cuyo nombre deriva del "vidrio de Moscú", con el que se fabricaban antiguamente las ventanas de las casas de esa ciudad.
En resumen, las arcillas expansibles son las esmectitas, las vermiculitas y las haloisitas, que derivan esta propiedad de la concentración de carga interlaminar, por ejemplo de 0.33 unidades por cada celda unitaria, mientras que ésta es igual a 0.86 en las vermiculitas y 1.0 en las muscovitas.
La figura 17 muestra los distintos espesores que se obtienen con las distintas arcillas al intercalarse una o dos capas de agua en el espacio interlaminar:
|
|
||
| a) Pirofilita | · cationes octaédricos | |
| b) Mica | o cationes intercambiables | |
| c) Esmectita | w capas de moléculas | |
| d) Vermiculita | ||
| e) Clorita | · OH | |
| f) Caolinita-serpentina | K ion de potasio | |
| g) Haloisita (10A) | ||
|
|
||
Una cosa queda clara: los edificios moleculares que constituyen a las arcillas y el grado de sustitución logrado, permiten obtener una serie de propiedades de interés en diversos campos de aplicación. No sólo esto es cierto cuando interviene la mano del hombre al tratar de modificar el espacio interlaminar (Figura 17), sino que el proceso de modificación a través del intercambio con otras especies químicas ocurre naturalmente, lo que conduce a una variación constante de la naturaleza de la arcilla que se traduce en variaciones de la fertilidad del suelo, permeabilidad, etc. Estas modificaciones del edificio molecular son susceptibles de estudiarse experimentalmente en el laboratorio y para ello es necesario introducir, ya sea un catión, ya sea una especie química distinta, en el interior del espacio interlaminar, lo cual será el tema que abordaremos enseguida.
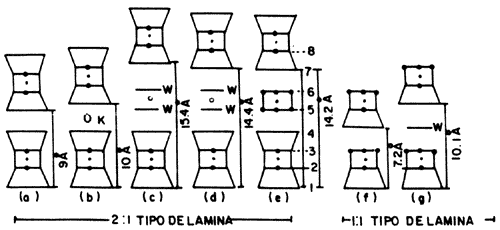
Figura 17. El espesor de las arcillas expandidas.