Corresponde a la sesi�n de GA 5.7 �OX�GENO, OX�GENO!
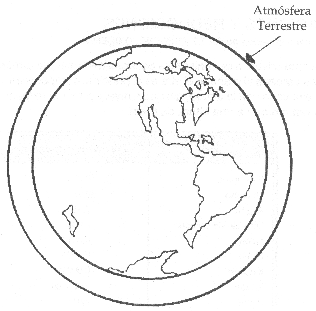
La Tierra est� envuelta por una masa gaseosa denominada atm�sfera, y en su parte m�s cercana al planeta, el aire es el principal componente. La composici�n del aire var�a con la altitud, as� que a nivel del mar el ox�geno ser� mucho m�s abundante que a una altura de 6 km.
| Gas | Porcentaje en volumen |
| Nitr�geno | 78.08 |
| Ox�geno | 20.95 |
| Arg�n | 0.91 |
| Di�xido de carbono | 0.033 |
| Ne�n | 0.0018 |
| Helio | 0.0005 |
| Kript�n | 0.00011 |
| Xen�n | 0.000009 |
| Agua | 0.01 |
| Hidr�geno | 0.01 |
Composici�n del aire a nivel del mar.
Todos estos gases son indispensables para la vida en nuestro planeta. Por ejemplo, el ox�geno y el di�xido de carbono son necesarios para los organismos aut�trofos y los heter�trofos.
El aire puede separarse en sus componentes mediante procesos de destilaci�n fraccionada. El nitr�geno y el ox�geno pueden almacenarse en matraces Dewar.
La mayor�a de los minerales contiene ox�geno, entre ellos se encuentran los �xidos, sulfatos y carbonos. Por otro lado, el agua es un compuesto constituido por ox�geno e hidr�geno. Tambi�n es un elemento esencial en el funcionamiento y conformaci�n de los seres vivos.
As� que, en la atm�sfera, la corteza terrestre y la hidrosfera, el ox�geno es el elemento m�s abundante.

El ox�geno es el elemento m�s abundante en la atm�sfera, la hidr�sfera y la corteza terrestre.
Existen 3 is�topos del ox�geno en la naturaleza: 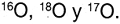
De forma natural, el ox�geno es producido por los seres aut�trofos a partir de una reacci�n qu�mica conocida como fotos�ntesis, realizada por cianobacterias, algas y plantas.
Artificialmente, se puede producir por hidr�lisis (rompimiento de la mol�cula de agua) como se observa en la reacci�n siguiente:
El ox�geno puro se usa en la industria del acero, en la producci�n de per�xidos, en los tratamientos biol�gico y qu�mico de las aguas residuales, en medicina, en los viajes espaciales y en los submarinos, entre otras actividades.
Se conocen cuatro iones del ox�geno: super�xido 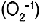 , per�xido
, per�xido 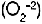 , �xido
, �xido 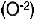 y oz�nido
y oz�nido 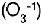 .
.
La existencia de estos iones permite que haya tanta variedad de compuestos del ox�geno, como son:
 El per�xido de hidr�geno o agua oxigenada, que se utiliza como as�ptico y antis�ptico.
El per�xido de hidr�geno o agua oxigenada, que se utiliza como as�ptico y antis�ptico.
 El ozono es muy importante, ya que forma una capa en la atm�sfera que filtra los rayos solares e impide, principalmente, la penetraci�n de los rayos ultravioleta que producen c�ncer en la piel.
El ozono es muy importante, ya que forma una capa en la atm�sfera que filtra los rayos solares e impide, principalmente, la penetraci�n de los rayos ultravioleta que producen c�ncer en la piel.
 Al unirse con un �tomo de carbono, el ion super�x�do forma el
Al unirse con un �tomo de carbono, el ion super�x�do forma el 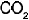 ., gas importante en la fotos�ntesis y en la regulaci�n de la temperatura atmosf�rica.
., gas importante en la fotos�ntesis y en la regulaci�n de la temperatura atmosf�rica.
 Puede haber �xidos met�licos, tambi�n llamados �xidos b�sicos, y anh�dridos conocidos como �xidos �cidos. Ejemplo de �xidos met�licos son: el �xido de calcio (CaO) y el �xido de potasio
Puede haber �xidos met�licos, tambi�n llamados �xidos b�sicos, y anh�dridos conocidos como �xidos �cidos. Ejemplo de �xidos met�licos son: el �xido de calcio (CaO) y el �xido de potasio 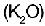 .
.
Ejemplo de anh�dridos son: anh�drido hipocloroso 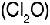 y anh�drido sulfuroso
y anh�drido sulfuroso 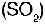
La denominaci�n de �xidos b�sicos y �xidos �cidos no es muy utilizada, ya que algunos elementos pueden formar tanto �xidos b�sicos como �cidos, y ciertos �xidos no se combinan con el agua.
Al n�mero de oxidaci�n de un elemento tambi�n se le llama valencia.
El n�mero de oxidaci�n de un elemento es un entero, y se asigna mediante las siguientes reglas:
 El n�mero de oxidaci�n de todos los elementos en su estado libre es cero.
El n�mero de oxidaci�n de todos los elementos en su estado libre es cero.
 El n�mero de oxidaci�n del ox�geno combinado es -2, excepto en los per�xidos y super�xidos, en que es -1.
El n�mero de oxidaci�n del ox�geno combinado es -2, excepto en los per�xidos y super�xidos, en que es -1.
 El n�mero de oxidaci�n del hidr�geno combinado es +1, excepto en los hidruros, en que es -1.
El n�mero de oxidaci�n del hidr�geno combinado es +1, excepto en los hidruros, en que es -1.
 Los elementos del grupo IA, combinados, tienen n�mero de oxidaci�n de +1; los del grupo IIA, de +2, y los del grupo VIlA de -1.
Los elementos del grupo IA, combinados, tienen n�mero de oxidaci�n de +1; los del grupo IIA, de +2, y los del grupo VIlA de -1.
La oxidaci�n es la p�rdida de electrones en un �tomo y la reducci�n es la ganancia de electrones en un �tomo.
Cuando un �tomo reacciona con otro, uno se oxida y el otro se reduce, por ello, estas reacciones se conocen como de oxidaci�n - reducci�n o redox.
Para separar el metal del mineral se utilizan oxidaciones y reducciones.
La metalurgia es el conjunto de procedimientos utilizados para extraer los metales a partir de sus menas. Las menas son compuestos naturales en los que existe tal concentraci�n de un metal que su explotaci�n resulta provechosa.
La tostaci�n es un proceso qu�mico metal�rgico que se utiliza cuando el mineral es un sulfuro, ejemplo:
La calcinaci�n se utiliza cuando el mineral es un carbonato, ejemplo:
Despu�s de la tostaci�n y calcinaci�n, los �xidos se someten a reducci�n, ejemplo:
Uno de los efectos de la oxidaci�n, que causa grandes p�rdidas materiales y econ�micas, es la corrosi�n que se produce cuando un metal es da�ado por alguna sustancia que produce un �xido, como por ejemplo: agua, aire, di�xido de carbono, di�xido de azufre, di�xido de nitr�geno o alg�n electr�lito disuelto, ya sea en agua o en la humedad ambiental
Otras sustancias corrosivas que son muy utilizadas en los hogares son los detergentes, �stas contienen fosfatos 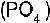 , lo cual aumenta su acci�n oxidante o corrosiva.
, lo cual aumenta su acci�n oxidante o corrosiva.
Un ejemplo claro para observar a simple vista los efectos del fen�meno de oxidaci�n es el de la corrosi�n de las estructuras met�licas.
La manera m�s sencilla de evitar la corrosi�n consiste en mantener la superficie met�lica libre de humedad, oxigeno y di�xido de carbono, entre otros factores, mediante una capa protectora de pintura o de grasa. Tambi�n se puede prevenir mediante el galvanizado, que consiste en recubrir un objeto de hierro con una capa de zinc.
![[ Índice Conceptos Básicos ]](toc.gif)
![[ Previo ]](prevsec.gif)
![[ Nivel Superior ]](parntsec.gif)
![[ Siguiente ]](nextsec.gif)