I. BOSQUEJO HISTÓRICO
HOY en día es común pensar que en el complejo proceso de creación, asimilación y aplicación del conocimiento científico, la tecnología es la última etapa que emana de la investigación científica. Si bien es cierto que existe una complicada interrelación entre la ciencia y la tecnología, al grado que es difícil pensar que ésta última sea ajena al quehacer científico, no siempre fue así. Cierto es que por ejemplo las comunicaciones, alámbricas e inalámbricas, surgen de la comprensión del comportamiento del campo electromagnético a través de los estudios de Faraday, Maxwell y Hertz en la segunda mitad del siglo pasado. Así, una tecnología emanó de los resultados de la investigación científica. Pero en el caso de los dispositivos que transforman energía y en particular energía térmica en trabajo mecánico, la situación fue completamente la opuesta. Estos últimos dispositivos, que ahora llamaremos máquinas térmicas se desarrollaron desde su forma más incipiente, en el siglo XVIII, hasta prácticamente la forma en que las conocemos hoy en día, lo que ocurrió ya hacia mediados del siglo XIX, sin que hubiese existido la menor comprensión sobre las causas teóricas, esto es, la explicación científica de su funcionamiento. Hagamos pues un poco de historia.
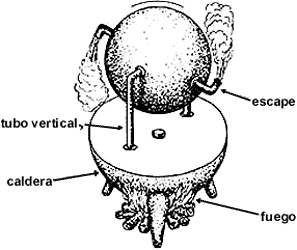
La primera máquina térmica de que tenemos evidencia escrita fue descubierta
por Hero de Alejandría ( ~ 130 a.C.) y llamada la aeolipila. Es
una turbina de vapor primitiva que consiste de un globo hueco soportado por
un pivote de manera que pueda girar alrededor de un par de muñones, uno de ellos
hueco. Por dicho muñón se puede inyectar vapor de agua, el cual escapa del globo
hacia el exterior por dos tubos doblados y orientados tangencialmente en direcciones
opuestas y colocados en los extremos del diámetro perpendicular al eje del globo.
Al ser expelido el vapor, el globo reacciona a esta fuerza y gira alrededor
de su eje.
En la misma obra de Hero se describe también el primer prototipo de una máquina de presión, que después fue motivo de varios estudios por Matthesuis en Alemania en l57l, de Caus en Francia en 1615 y en Italia por Ramelli en 1588, della Porta en 1601 y Branca en 1629. Posteriormente, en 1663, Edward Somerset, el segundo marqués de Worcester, en su obra Un siglo de invenciones describe un método para elevar un volumen de agua usando vapor. Su descripción es obscura y carece de dibujos; y subsiste la duda de si construyó o no la máquina. No fue sino hasta los años de 1698 a 1725 cuando la idea de Somerset fue puesta en práctica y utilizada para satisfacer diversas necesidades. En 1698 Thomas Savery obtuvo una patente para una máquina utilizada para elevar cantidades considerables de agua. Su funcionamiento consistía esencialmente en inyectar vapor a un recipiente lleno de agua hasta vaciar su contenido por un tubo vertical a través de una válvula de seguridad. Cuando el recipiente se vacía cesa el suministro de vapor y el vapor contenido se condensa por medio de un chorro de agua fría que cae sobre las paredes exteriores de dicho recipiente y que proviene de una cisterna colocada en su parte superior. Esto produce un vacío y permite que otro tubo, controlado por otra válvula de seguridad, aspire agua del pozo distribuidor a cualquiera que sea la fuente. Entre tanto, una operación paralela se lleva a cabo en otro recipiente semejante al primero. El vapor se suministra de un horno que consiste de una caldera principal que tiene una alimentación continua de agua caliente la cual proviene de otro horno que calienta agua fría por el fuego encendido en su hoguera. Los niveles de agua en las calderas se controlan por sendas válvulas de presión.
Esta máquina, que puede considerarse como la primera máquina de vapor, encontró un uso considerable en la extracción de agua de las minas de carbón y en la distribución de agua para casas habitación y pequeñas comunidades. Esta máquina fue subsecuentemente modificada de diversas maneras, todas ellas destinadas a mejorar la cantidad de agua y la altura a que ésta podía elevarse, ya que estas características estaban limitadas por la presión que podían soportar las calderas. Ya en 1690 Denis Papin había sugerido que la condensación de vapor se debería usar para producir un vacío debajo de un pistón que previamente se había elevado por la acción del vapor. Ésta fue la primera versión de una máquina de vapor usando un cilindro y un pistón. En 1705 Thomas Newcomen y John Cawley, su asistente, mejoraron la operación del pistón al forzar su caída por acción de la presión atmosférica. Al hacerlo producía trabajo mecánico sobre una bomba que introducía el agua por bombear. Después de varios ajustes técnicos estas máquinas fueron producidas en gran tamaño y en serie por John Smeaton hasta que en 1770 fueron superadas por las innovaciones debidas a James Watt. (Figs. 1)
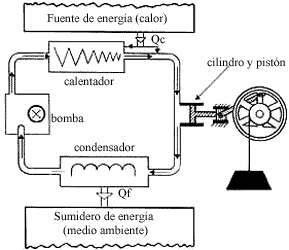
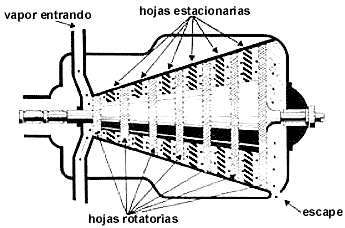
Figura 1a. Figura esquemática de una máquina o planta de vapor. El agua
es bombeada a un calentador donde hierve y se evapora al aumentar la presión
del cilindro para empujar al pistón hasta enfriarse a la temperatura y presión
del condensador en el cual condensa y vuelve a ser bombeada para completar el
ciclo.
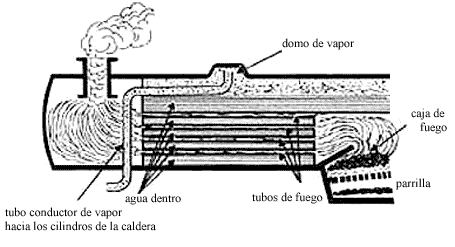
Figura 1b. Diagrama simplificado de una locomotora de vapor mostrando el principio básico utilizado.
En 1763 este notable fabricante de instrumentos escocés, al reparar una de
las máquinas de Newcomen se sorprendió de ver el enorme desperdicio de vapor
que ocurría durante el proceso de calentamiento y enfriamiento del cilindro,
dentro del cual operaba el pistón. El remedio, en sus propias palabras, consistiría
en mantener al cilindro tan caliente como el vapor de entrada. Después de seis
años sus experimentos lo llevaron a patentar, en 1769, una máquina que superaba
a las de su antecesor por su mayor rapidez en la carrera del pistón y por ser
mucho más económica en cuanto al consumo de combustible, sin embargo estaba
reducida al bombeo y adolecía de otras limitaciones técnicas. La forma en que
estas limitaciones fueron superadas queda fuera de contexto, pero vale la pena
subrayar que el propio Watt en 1781 ideó la forma de usar la máquina para hacer
girar un eje y por lo tanto, abrir sus aplicaciones a muchos otros usos además
del bombeo. En manos de inventores notables como Trevitchik y Woolf en Inglaterra,
Evans en los EUA , Cugnot en Francia y otros, esta máquina llegó
a un estado de perfección tal que en 1829 George Stephenson fue el primero en
adaptarla a una locomotora esencialmente en la misma forma usada por las más
pesadas locomotoras actuales. También, en 1802 fue usada por vez primera por
W. Symington para navegar el remolque Charlotte Dundas. Posteriormente,
en 1807, el norteamericano Robert Fulton hizo navegar un barco en el río Hudson
con máquinas de vapor diseñadas por Boulton y Watt.
Entre esos años y las postrimerías del siglo pasado, con mejoras en el diseño y la construcción, la máquina de vapor se transformó en la máquina habitual para la navegación marina lográndose alcanzar presiones de vapor muy altas y velocidades de pistón considerables. Con la invención de la turbina de vapor la navegación marina adquirió su máximo grado de desarrollo, sólo superado posteriormente por el advenimiento de los combustibles nucleares. En la turbina de vapor, desarrollada por Parsons en 1884 y perfeccionada por Laval en 1889, la presión del vapor se utiliza para poner directamente al fluido en movimiento y no al pistón.
En todo este proceso de invenciones e innovaciones los inventores difícilmente tuvieron una teoría, como la electromagnética en el caso de la radio, que les guiara en su camino. Los termómetros producto de la obra de Gabriel Fahrenheit en 1717, eran reproducibles con un alto grado de precisión y surgieron de la necesidad de subsistir con un instrumento más preciso las sensaciones de frío y caliente que al tacto son difíciles de cuantificar. De hecho, mucho antes de su construcción, científicos como Leonardo da Vinci, Galileo y otros sabían que al contacto con un tercer cuerpo, usualmente el aire, dos o más cuerpos en contacto con él "se mezclaban de una manera apropiada" hasta alcanzar una misma "condición". De ahí la palabra temperatura que proviene del latín temperare que significa "mezclar apropiadamente" o templar. Pero para nadie era claro qué mecanismo estaba implícito en ese mezclado.
En 1620, sir Francis Bacon en su célebre obra Novum Organum propuso un método para estudiar e interpretar la naturaleza y eligió la naturaleza del calor para ilustrarlo. El método consiste de tres pasos: el primero, listar todas las "instancias asociadas a la ‘naturaleza’" que se desea investigar; el segundo es una revisión crítica de la lista y el tercero un proceso de inducción para formular la interpretación fundamental del fenómeno. Aplicada al calor es ilustrativo, pues pone de relieve las ideas que al respecto prevalecían en ese entonces: la forma o verdadera definición de calor es como sigue: calor es un movimiento, expansivo, restringido y actuando en su contienda sobre las partículas más pequeñas de los cuerpos.
Aunque se realizaron muchos esfuerzos para explicar los procesos que se pensaban
ocurrían al experimentar con la ayuda de termómetros, fue Joseph Black un médico
y químico escocés, quien a mediados del siglo XVIII aclaró la distinción
entre calor y temperatura. En sus Lecciones sobre los elementos de la química,
publicada póstumamente en 1803 y editada por su alumno y colega John Robison,
Black distingue con toda precisión la diferencia entre calor y temperatura e
introduce por primera vez los conceptos de calor específico y calor latente.
De esta obra vale la pena citar al pie de la letra:
En términos contemporáneos no sólo apunta Black al hecho de que calor y temperatura
son dos conceptos estrictamente diferentes, sino que además apunta al bien conocido
hecho de que los calores específicos de substancias diferentes, son diferentes.
De sus experimentos al mezclar agua y mercurio a diferentes temperaturas iniciales
cita:
Se pone de manifiesto que la cantidad de calor
requerida para hacer 2 volúmenes de agua más caliente, digamos por 25
grados, es suficiente para hacer a 3 volúmenes de mercurio más calientes
por el mismo número de grados. Esto es, el mercurio tiene una menor capacidad
para el calor1
(si se me permite usar la expresión) que el agua... |
Sobre los calores latentes sus observaciones fueron no menos agudas. Citamos: "La opinión que me he formado de una observación minuciosa de los hechos y fenómenos es como sigue: Cuando el hielo u otra sustancia sólida se funde, soy de la opinión que recibe una cantidad de calor mayor que la perceptible a través del termómetro inmediatamente después de la fusión... Este calor debe agregarse para darle la forma de un líquido; cuando congelamos un líquido, este emite una gran cantidad de calor... En los procesos ordinarios de la congelación del agua, la extracción y surgimiento de calor latente, si se me permite usar el término, se lleva a cabo por etapas diminutas... que muchos pueden encontrarse difíciles de comprender..."
Pero hasta el momento nada se ha dicho sobre la naturaleza misma del calor.
En 1783 el famoso químico Henry Cavendish al referirse al frío generado por
la fusión del hielo y el calor producido por la congelación de agua observó:
El texto de Cavendish no sólo arroja luz sobre las controversias existentes en aquella época acerca de la naturaleza del calor, sino que además exhibe claramente la idea que el gran Newton tenía sobre el calor, muy cercana a la interpretación moderna basada en la teoría molecular de la materia. ¿Y Black mismo? Aunque mucho se dice que él nunca sostuvo con convicción una teoría específica sobre el calor , sus escritos muestran que estaba consciente de la polémica acerca de la naturaleza del calor. Dicha polémica originada desde el tiempo de los griegos y suscrita por Robert Boyle en su obra Ensayos sobre efluvios sugería que el calor era una substancia material que se comportaba como un fluido elástico, sutil, que llenaba todos los cuerpos y cuya densidad aumentaba con la temperatura.
Este fluido se concebía como formado partículas que se repelen entre sí pero son atraídas a las partículas de materia ordinaria. Cada partícula de materia está entonces rodeada de una atmósfera de calórico de manera que dos partículas materiales se repelen entre sí a cortas distancias, aunque a distancias grandes la atmósfera se atenúa y predomina la fuerza atractiva de la gravedad; así existe un punto de equilibrio intermedio en el cual la fuerza neta es cero. Si la temperatura aumenta y se agrega fluido a la sustancia, el punto de equilibrio se desplaza hacia el exterior aumentando la distancia promedio entre las partículas y produciendo así una expansión del cuerpo. Bajo una compresión el fluido se comprime y aparece en la superficie como calor emitido. Esta teoría aunque opuesta al concepto de movimiento propuesto por Bacon y sostenido por Newton y otros filósofos ingleses, llegó a tener una aceptación general al grado que en 1787 el célebre químico Lavoisier y otros científicos franceses, al hacer una revisión de la terminología química, llamaron a este fluido el "calórico".
Antes de volver a nuestra pregunta inicial acerca de la teoría inexistente sobre el funcionamiento de las máquinas térmicas conviene mencionar algunas anécdotas adicionales.
De acuerdo con la teoría de Black cuando un cuerpo se licúa o se congela (solidifica) el calor latente emitido o absorbido resultaba de la combinación de una cantidad definida del calórico con cada partícula material de la sustancia en cuestión. Al concebir al calor como el calórico surgió de manera natural la pregunta acerca de como medir su peso. Esta cuestión fue abordada por Benjamin Thomson, más tarde el conde Rumford, en 1798 y en 1799 por el notable químico H. Davy. Después de una serie de experimentos que más tarde se reconocieron como una evidencia clara para desechar la existencia del calórico, concluyeron que el peso de dicho fluido nunca podría determinarse.
En su época, estos experimentos no se estimaron como objeciones serias a la teoría del calórico porque sus ejecutantes, Davy y Rumford, no propusieron una teoría alternativa coherente; no explicaron cómo si el calor es movimiento de partículas (moléculas) puede transferirse de una substancia a otra. Por otra parte, el calor radiante se usaba en todas sus manifestaciones como un fuerte apoyo a la teoría del calórico: como el calor podía atravesar el vacío sin provocar ningún movimiento de materia, debía ser una substancia y no una propiedad de la materia.
No obstante estas controversias, no existía evidencia conclusiva y contundente
para descartar la teoría del calórico, hasta que a fines del siglo XVIII
el conde Rumford, que fungía entonces como superintendente del arsenal
de Münich, percibió una cantidad de calor muy considerable que se producía al
horadar un cañón y el calor aún mas intenso de las astillas metálicas que se
producían en dicha operación. Citando su propio texto publicado en 1798:
Inspirado en estas ideas, Rumford decidió llevar a cabo varios experimentos para responder a estas cuestiones. Construyó un cilindro de bronce que pudiera ajustarse a un taladro de acero filoso. Este taladro se forzaba en contra de la parte inferior del cilindro y al cilindro se le hacía girar sobre su eje por medio de una máquina taladradora operada con caballos. En su experimento más espectacular todo el cilindro y el taladro se ponían dentro de una caja hermética llena con agua inicialmente a una temperatura normal (18º C) y la máquina se ponía en movimiento. El cilindro se hacia girar a 32 vueltas por minuto. Al poco tiempo de operar. Rumford percibió un calentamiento del cilindro y del agua. Citando. "Al cabo de una hora encontré, introduciendo un termómetro en el agua, que su temperatura había aumentado no menos de 9º C y al cabo de dos horas con 20 minutos era de 94º C, y a las dos horas y media ¡el agua hervía! Sería difícil describir la sorpresa y aturdimiento reflejado en el semblante de los espectadores al ver una cantidad de agua fría, calentarse y hervir, sin nunca haber encendido un fuego."
De estos experimentos, Rumford concluyó que la fuente generada por la fricción es inagotable y señaló que cualquier cosa que uno o varios cuerpos puedan generar sin límite alguno no puede ser substancia material.
Por consiguiente, de los experimentos realizados es difícil, si no imposible, identificar al calor generado con otra cosa que no sea el movimiento. Aunque el efecto de estos experimentos fue debilitar seriamente las bases en que se sustentaba la teoría del calórico, tuvieron que pasar otros cincuenta años antes de que estos puntos de vista fueran totalmente aceptados.
La discusión anterior exhibe con cierto detalle el escenario en que evolucionó la tecnología de las máquinas térmicas, en la medida, como dijimos antes, de tener a la mano una teoría que guiara su desarrollo. En efecto, tal teoría, hasta 1840 no existió y la evolución de la tecnología fue casi empírica.
La primera persona que planteó la interrogante esencial del problema, a saber,
conocer el principio o los principios que rigen el funcionamiento de estas máquinas,
fue el brillante ingeniero francés N. Sadi Carnot (1796-1832). En 1824 publicó
su famosa memoria Reflexiones sobre la potencia motriz del calor y sobre
las máquinas apropiadas para desarrollar esta potencia, en donde se dedicó
a razonar sobre la pregunta general de cómo producir trabajo mecánico (potencia
motriz) a partir de fuentes que producen calor. Citamos de su obra:
Es realmente a partir de estas ideas de las cuales surgió toda la teoría moderna
de las máquinas térmicas y, como veremos más adelante, se llegó a la formulación
del no siempre muy claro segundo principio de la termostática. Pero volvamos
con Carnot para comprende mejor sus ideas concebidas todavía durante la época
en que la teoría del calórico era, inclusive para él mismo, muy aceptada. El
punto clave consiste en reconocer que una máquina térmica (o de vapor ) requiere
de una diferencia de temperaturas para poder operar. Citamos:
En otras palabras, cuando la máquina opera entre dos cuerpos y extrae de calor
del más caliente, cede una cantidad de calor al cuerpo más frío hasta igualar
las temperaturas de ambos, esto es, hasta restaurar el equilibrio térmico. Más
aún, señala que cuando la restauración del equilibrio ocurre sin producir trabajo,
éste debe considerarse como una pérdida real (Fig. 2). En el lenguaje más moderno
diríamos que a diferencias de temperatura entre dos o más cuerpos tienden a
desaparecer espontáneamente al fluir el calor de los más calientes a los más
fríos sin producir trabajo útil.
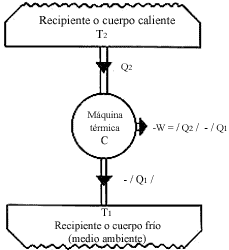
Figura 2. Una máquina térmica extrae / Q2 / unidades de calor de
una fuente a temperatura T2 y desecha una cantidad menor - / Q1
/ a la fuente fría. Ésta, usualmente el medio ambiente, se encuentra a una temperatura
T1 menor que T2. Por la conservación de la energía, el
trabajo neto realizado por la máquina, si ésta es ideal (no hay fricción) es
- W = / Q2 / - / Q1 /
De aquí entonces se le ocurre a Carnot pensar que una máquina térmica eficiente
debe diseñarse de manera que no existan flujos de calor desaprovechables durante
su operación. Para ello se le ocurre idear un proceso cíclico en el cual sólo
aparecen la fuente térmica de la cual la máquina extrae calor para operar y
la fuente fría a la cual se le suministra el calor no aprovechable. Citamos:
1) Ponemos en contacto al cuerpo A con el aire encerrado en el espacio abcd a través de una de sus caras, ab digamos, que suponemos conduce calor fácilmente. A través de este contacto el aire alcanza la misma temperatura que la del cuerpo A; cd es la posición presente del pistón.
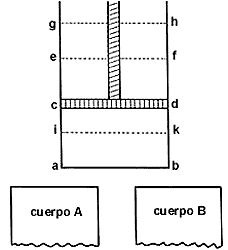
Figura 3. Diagrama de la Máquina de Carnot (según Carnot)
2) El pistón se eleva gradualmente hasta tomar la posición ef. Se mantiene el contacto con el cuerpo A y el aire, el cual por lo tanto se mantiene a una temperatura constante durante la expansión. El cuerpo A suministrará calor necesario para mantener dicha temperatura constante.
3) El cuerpo A se retira de manera que el aire no esté ya en contacto con cualquier cuerpo que pueda suministrar calor: el pistón, sin embargo, continúa moviéndose y pasa de la posición ef hasta la posición gh. El gas se expande sin recibir calor y su temperatura disminuye. Imaginemos que disminuye en esta forma hasta que alcanza un valor igual a la temperatura del cuerpo B. En este punto el pistón se para y ocupa la posición gh.
4) El aire se pone en contacto con el cuerpo B; se comprime por el regreso del pistón a medida que se mueve de la posición gh a la posición cd. No obstante, el aire se mantiene a una temperatura constante por su contacto con el cuerpo B al cual le cede su calor.
5) Se retira el cuerpo B y continuamos la compresión del aire el cual, ahora aislado, aumenta su temperatura. La compresión se continúa hasta que el aire alcance la temperatura del cuerpo A. Durante este proceso el pistón pasa de la posición cd a la posición ik.
6) El aire se pone de nuevo en contacto con el cuerpo A; el pistón regresa de la posición ik a la posición ef; la temperatura permanece constante.
7) La operación descrita en 3) se repite y sucesivamente 4,5,6,3,4,5,6,3,4,5,... y así sucesivamente.
Sobre este proceso cíclico Carnot hace ver que la substancia operante (el aire)
realiza una cantidad de trabajo neta y además que este trabajo se produce de
la manera más ventajosa posible. Los dos procesos 3 y 5 en que el aire está
aislado cambian su temperatura sin remover o ceder calor. En esta forma el aire
siempre se pone a la temperatura deseada, la del cuerpo A y B respectivamente,
antes de ponerlo en contacto con ellos; se elimina pues cualquier flujo
de calor espurio entre cuerpos a diferentes temperaturas. También, hace notar
que la secuencia de operaciones arriba descrita puede llevarse a cabo en el
sentido opuesto, lo cual implica que al terminar el paso 6) se llevan a cabo
las operaciones en el orden 5), 4), 3), 6), 5), 4), etc. En este caso el resultado
es el de consumir una cierta cantidad de trabajo igual a la producida
en el ciclo inicial y regresar todo el calor del cuerpo B al cuerpo A.
Finalmente, Carnot demuestra que no puede concebirse una máquina térmica más
eficiente operando entre dos temperaturas prescritas que la suya y anuncia una
de sus proposiciones fundamentales:
Así se veían los procesos subyacentes a las máquinas térmicas, incluyendo las
de vapor durante la tercera década del siglo XIX. El porqué no
tuvo mayor impacto el trabajo de Carnot, que contiene el reconocimiento claro
entre la equivalencia entre calor y trabajo así como la imposibilidad de construir
una máquina de movimiento perpetuo, principio ahora conocido como la segunda
ley de la termodinámica, fue debido a que sus colegas franceses lo ignoraron
por completo. Sólo Emile Clapeyron, un colega de Carnot de la École Polytéchnique,
publicó un escrito en 1834 mencionando su trabajo. Fue sólo en Alemania y en
Inglaterra que sus ideas fueron apreciadas e incorporadas en la teoría moderna
del calor, y fueron la fuente esencial de donde emanaron las leyes de la termostática.
NOTAS
1 El término calor específico fue introducido en 1781 por el físico sueco J. C. Wilcke.