V. ¿SE PUEDE LUCHAR CONTRA LA CORROSIÓN? EL CONTROL DE LA CORROSIÓN
BÁSICAMENTE todos los métodos que existen para lograr controlar la corrosión de los materiales metálicos, son intentos para interferir con el mecanismo de corrosión, de tal manera que se pueda hacer que éste sea lo más ineficiente posible. Por ejemplo, disminuyendo el flujo de electrones entre los componentes metálicos de la celda de corrosión por el aumento de la resistencia eléctrica del metal, de alguna manera disminuiría la corriente de corrosión y, por tanto, la velocidad de corrosión. Esto no es practicable generalmente, pero disminuir el flujo de corriente en el componente electrolítico de la celda de corrosión produciría el mismo efecto, y esto sí es practicable.
Dado que para que exista un proceso de corrosión, debe formarse una pila o celda de corrosión y, por tanto, un ánodo, un cátodo, un conductor metálico y una solución conductora, además de una diferencia de potencial entre los electrodos o zonas anódicas y catódicas, la eliminación de alguno de los componentes esenciales de la mencionada pila, podría llegar a detener el proceso.
En la práctica, existen tres maneras de lograr lo anterior y por tanto de luchar contra la corrosión:
1) Aislamiento eléctrico del material. Esto puede lograrse mediante el empleo de pinturas o resinas, depósitos metálicos de espesor suficiente o por aplicación de recubrimientos diversos.
De esta forma, se puede lograr aislar el metal del contacto directo con el medio agresivo (agua, suelo y atmósfera por lo general).
2) Cambiando el sentido de la corriente en la pila de corrosión.
Conectando eléctricamente, por ejemplo, el acero con un metal más activo (cinc o magnesio) podemos llegar a suprimir la corrosión del acero, ya que dejará de actuar como ánodo y pasará a comportarse como cátodo, dejando el papel de ánodo al metal más activo (cinc o magnesio).
Este es el principio de la protección Catódica.
3) Polarización del mecanismo electroquímico.
Esto se puede lograr bien eliminando el oxígeno disuelto, bien mediante la adición en el medio agresivo de ciertas sustancias llamadas inhibidores, las cuales pueden llegar a polarizar uno de los electrodos de la pila de corrosión y por lo tanto, llegar a detener o cuanto menos disminuir sus efectos. En la práctica, lo anterior conlleva una modificación del entorno o medio ambiente, al cual está expuesto el metal.
Veamos con un poco más de detalle, en qué consisten cada una de las tres maneras propuestas de luchar contra la corrosión.
Estos recubrimientos se utilizan para aislar el metal del medio agresivo. Veamos en primer lugar aquellos recubrimientos metálicos y no-metálicos que se pueden aplicar al metal por proteger, sin una modificación notable de la superficie metálica.
Recubrimientos no-metálicos: Podemos incluir dentro de éstos las pinturas, barnices, lacas, resinas naturales o sintéticas. Grasas, ceras, aceites, empleados durante el almacenamiento o transporte de materiales metálicos ya manufacturados y que proporcionan una protección temporal.
Recubrimientos orgánicos de materiales plásticos: Esmaltes vitrificados resistentes a la intemperie, al calor y a los ácidos.
Recubrimientos metálicos: Pueden lograrse recubrimientos metálicos mediante la electrodeposición de metales como el níquel, cinc, cobre, cadmio, estaño, cromo, etcétera.
Inmersión en metales fundidos: Cinc (galvanización en caliente), aluminio (aluminizado), etc.
Proyección del metal fundido mediante una pistola atomizadora. Metalizaciones al cinc, aluminio, estaño, plomo, etc.
Reducción química (sin paso de corriente): electroles. Por ese procedimiento se pueden lograr depósitos de níquel, cobre, paladio, etc. Recubrimientos formados por modificación química de la superficie del metal. Los llamados recubrimientos de conversión consisten en el tratamiento de la superficie del metal con la consiguiente modificación de la misma. Entre las modificaciones químicas de la superficie del metal podemos distinguir tres tipos principales:
Recubrimientos de fosfato: El fosfatado se aplica principalmente al acero, pero también puede realizarse sobre cinc y cadmio. Consiste en tratar al acero en una solución diluida de fosfato de hierro, cinc o manganeso en ácido fosfórico diluido. Los recubrimientos de fosfato proporcionan una protección limitada, pero en cambio resultan ser una base excelente para la pintura posterior.
Recubrimiento de cromato. Se pueden efectuar sobre el aluminio y sus aleaciones, magnesio y sus aleaciones, cadmio y cinc. Por lo general, confieren un alto grado de resistencia a la corrosión y son una buena preparación para la aplicación posterior de pintura.
Recubrimientos producidos por anodizado. El anodizado es un proceso electrolítico en el cual el metal a tratar se hace anódico en un electrolito conveniente, con el objeto de producir una capa de óxido en su superficie. Este proceso se aplica a varios metales no-ferrosos, pero principalmente al aluminio y a sus aleaciones. Proporciona una buena protección y también resulta un buen tratamiento previo para la pintura posterior.
Podemos incluir también entre los recubrimientos con modificación de la superficie del metal los procesos de cementación. En este proceso, se convierte la superficie externa de la porción metálica que se quiere proteger, en una aleación de alta resistencia a la corrosión. El proceso consiste en calentar la superficie metálica en contacto con polvo de cinc (sherardizado), polvo de aluminio (calorizado) o un compuesto gaseoso de cromo (cromizado). Se obtienen capas de un considerable espesor.
Propiedades físicas de los recubrimientos metálicos
Refiriéndonos al caso del acero como el material de más amplia utilización, la selección de un determinado recubrimiento metálico se puede efectuar y justificar sobre la base de una de las siguientes propiedades físicas, cuando se trata de proteger de una manera eficaz y económica la superficie del acero en condiciones determinadas:
- Impermeabilidad, esto es, que el recubrimiento sea continuo y de espesor suficiente, lo cual permitirá aislar la superficie del acero de los agentes agresivos.
- Resistencia mecánica de los metales utilizados en los recubrimientos, para garantizar una buena resistencia a los choques, rozamientos ligeros o accidentales, etc.
-Posibilidad de proporcionar superficies pulidas o mates, capaces de conferir a los objetos un acabado con fines decorativos.
Para obtener buenos resultados con los recubrimientos metálicos, hay que tener en cuenta una serie de operaciones que deben llevarse a cabo con anterioridad a la aplicación del recubrimiento.
Estado de la superficie a proteger. Preparación de la superficie
La limpieza y puesta a punto de la superficie del acero antes de la aplicación de un recubrimiento metálico, son operaciones indispensables, sea cual sea el procedimiento de aplicación escogido. De la calidad de la preparación de la superficie dependerá la adherencia y, en consecuencia, la eficacia de la capa protectora.
Según el estado actual de la superficie por proteger, más o menos oxidada, se puede seleccionar el procedimiento mecánico de limpieza más adecuado, desde el granallado, chorreado de arena, pasando por una limpieza química o electroquímica, como los baños ácidos, con corriente eléctrica o sin ella.
La selección de un recubrimiento está en función de las dimensiones de los objetos y de la extensión de la superficie que se quiere recubrir.
Los procedimientos que se aplican en recintos como hornos, cubas electrolíticas o crisoles, sólo pueden utilizarse para aquellas piezas cuyas dimensiones no están limitadas por su capacidad. Esto es válido para la galvanización, electrólisis, tratamientos térmicos. Por el contrario, la metalización con pistola permite efectuar recubrimientos metálicos independientemente de las dimensiones de la pieza, en razón de la movilidad del equipo.
Por ejemplo, si se trata de hacer un recubrimiento de cinc o cadmio sobre unos tornillos, la operación se puede realizar mediante una electrólisis. Para proteger un bote de acero con un recubrimiento de cinc, se puede recurrir a la galvanización en caliente. En fin, si se trata de proteger una obra de arte o la puerta de una esclusa, se debe de recurrir al cinc proyectado por una pistola de metalización.
Tanto la naturaleza como el espesor del metal protector son función de muchos parámetros, entre los cuales uno de los más importantes es el precio. Asimismo, es muy importante conocer con la mayor precisión posible el medio ambiente al cual va a estar sometida la pieza. En lo que cierne a los medios naturales, debe conocerse si es posible si se trata de una atmósfera exterior (y en este caso es de mucha ayuda conocer el tipo de atmósfera: rural, urbana, industrial, marina, etc.) o interior (climatizada, con calefacción, etc.).
Para los entornos diferentes a los naturales, es preciso conocer la mayor información posible sobre la composición química del medio, impurezas eventuales, estado físico, temperatura, etc. Por ejemplo, los recubrimientos de cinc aguantan el contacto con soluciones de pH comprendido entre 6 y 11; los recubrimientos de estaño son convenientes en contacto con ciertos productos alimenticios, etc.
Los procedimientos más comúnmente empleados en la práctica para obtener recubrimientos metálicos sobre el acero son:
- metalización por proyección con pistola
- tratamientos termoquímicos de difusión
Los procedimientos de aplicación son de suma importancia en cuanto a la eficacia de la protección contra la corrosión, pues tanto el espesor, porosidad, como la naturaleza misma de las capas obtenidas son función del procedimiento de aplicación. Así, por ejemplo, los recubrimientos electrolíticos que tienen espesores de algunos micrones, se reservan generalmente para su utilización en medio poco agresivo. En cambio, los recubrimientos obtenidos por inmersión en un metal fundido tienen espesores mayores.
Los recubrimientos obtenidos mediante proyección permiten obtener espesores más grandes y perfectamente controlables. Se utilizan especialmente en condiciones severas de corrosión.
El placado del acero permite asociar a la calidad mecánica del soporte, la resistencia a la corrosión del recubrimiento.
La selección entre los diferentes procedimientos de aplicación de los recubrimientos metálicos se realiza, pues, siguiendo criterios tales como: el espesor de protección, dimensión de las piezas, agresividad del medio, duración prevista, etc. Muy brevemente vamos a describir cada uno de los procedimientos citados.
Inmersión en un metal en fusión
Después de una adecuada preparación superficial (un decapado ácido por ejemplo), las piezas de acero se sumergen momentáneamente en un baño de un metal en fusión. Esta operación puede realizarse para una sola pieza o para un conjunto, o también en continuo para productos siderúrgicos como tuberías láminas, trefilados, etc. Tal técnica se utiliza habitualmente para los recubrimientos de cinc (galvanización en caliente), aluminio (aluminizado), estaño y plomo.
Después del enfriamiento, las piezas ya recubiertas pueden someterse a un tratamiento complementario de pasivación en ciertos casos.
Metalización por proyección con pistola
Esta técnica consiste en proyectar sobre la superficie del acero, ya preparada en unas condiciones especiales (por chorreado con arena o granallado), un metal en estado de fusión por medio de una pistola.
El espesor del recubrimiento se puede controlar fácilmente por el operador y puede variar según la naturaleza del metal proyectado y el resultado que se espera obtener. La mayoría de los metales o aleaciones pueden aplicarse de esta manera: cinc, aluminio, acero inoxidable, estaño, plomo, níquel, cobre, etc.
Después de una cuidadosa preparación superficial que incluye un decapado ácido, seguido de neutralización y lavado, las piezas por tratar se sumergen en soluciones que contienen sales de los metales a depositar. Las piezas se colocan en posición catódica, conectadas al polo negativo de un generador. Bajo la acción de la corriente eléctrica proporcionada por el generador, el acero se recubre del metal contenido en el baño o bien puede ser suministrado por un ánodo soluble del metal en cuestión.
Los metales corrientemente depositados por vía electroquímica son: cromo cobre, níquel, cinc, cadmio y estaño. Los depósitos obtenidos son por lo general de espesor pequeño (2 a 30 micrones).
Tratamientos termoquímicos de difusión
Los tratamientos termoquímicos de difusión, también conocidos como cementación, consisten en colocar las piezas de acero a tratar en una mezcla de polvo metálico y de enlazante (cemento) en un recinto a alta temperatura. El metal protector (recubrimiento) se difunde superficialmente en el metal base y forma una capa eficaz contra la corrosión. Los metales corrientemente aplicados por este método son el cinc (sherardización) y el aluminio.
Después de un tratamiento superficial especial, la lámina del metal para aplicar y el metal base se someten a un proceso de colaminación en caliente, obteniéndose al final lámina de acero recubierta del metal aplicado. Este proceso puede efectuarse sobre una o las dos caras de la lámina del acero. El acero inoxidable, níquel, monel y el cobre se aplican comúnmente por esta técnica.
La corrosión suele ser un fenómeno electroquímico por lo que se puede intentar combatirlo conectando el metal que se quiere proteger a otro metal menos noble, según la serie galvánica, que actuará entonces como ánodo de sacrificio (también llamado galvánico) o bien conectándolo al polo negativo de una fuente exterior de corriente continua.
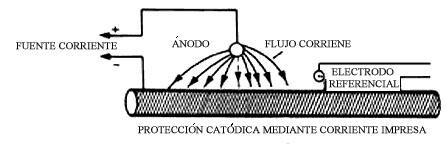
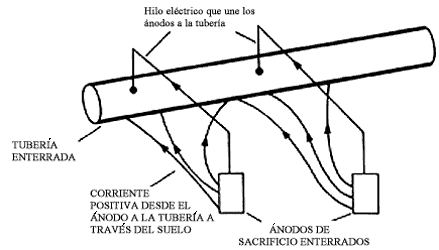
Figura 23. Protección catódica mediante ánodos de sacrificio.
El primer caso constituye la protección catódica con ánodos galvánicos o de
sacrificio y el segundo la protección catódica con corriente impresa. La protección
catódica constituye sin duda, el más importante de todos los métodos empleados
para prevenir la corrosión de estructuras metálicas enterradas en el suelo o
sumergidas en medios acuosos.
Tanto el acero como el cobre, plomo y bronce son algunos de los metales que pueden ser protegidos de la corrosión por este método. Las aplicaciones incluyen barcos, tuberías, tanques de almacenamiento, puentes, etc. La protección se logra aplicando una corriente externa a partir de un rectificador que suministra corriente continua de bajo voltaje. El terminal positivo de la fuente de corriente se conecta a un ánodo auxiliar (grafito por ejemplo) localizado a una determinada distancia de la estructura a proteger y el terminal negativo se conecta a la estructura metálica.
En la práctica, la corriente necesaria para proteger una estructura desnuda suele ser demasiado grande como para ser rentable económicamente. La estructura entonces, se recubre con algún revestimiento para proporcionarle protección frente al medio agresivo, reservándose la protección catódica para proteger la estructura sólo en aquellos puntos en que no pueda lograrlo el revestimiento.
Una estructura también puede protegerse contra la corrosión mediante un ánodo galvánico o de sacrificio. Si el electrodo auxiliar es de un metal más activo que el metal que se quiere proteger, actuará de ánodo en la celda de corrosión. En este caso, la estructura actuará como cátodo y quedará protegida por el "sacrificio" del ánodo que se corroerá.
Este otro método de proteger catódicamente una estructura se utiliza cuando resulta inconveniente una fuente externa de corriente. Esencialmente, el ánodo de sacrificio (de magnesio, aleaciones base de magnesio, cinc y aluminio) suministra la energía eléctrica necesaria para la protección de la estructura.
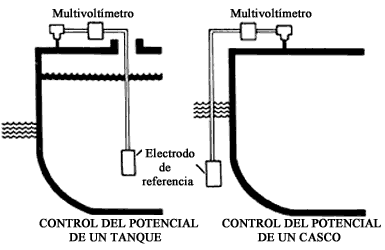
En un montaje de protección catódica conviene comprobar periódicamente la buena
marcha del sistema de protección, lo cual se realiza con ayuda de un electrodo
de referencia y un milivoltímetro. Los electrodos de referencia más empleados
son el de plata/cloruro de plata (Ag/AgCl) y el de cobre/sulfato de cobre
(Cu/CuSO4)
Los esquemas de la figura muestran como hacerlo en el caso de control del casco de un barco o de una cisterna de un petrolero.
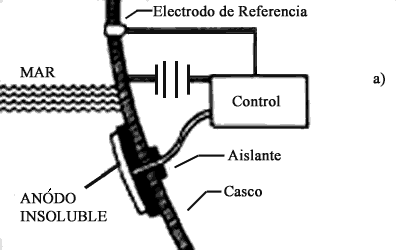
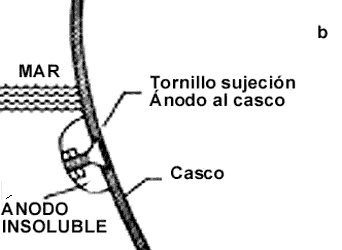
Figura 25. Protección catódica del casco de un barco.
a) Mediante corriente impresa, b) mediante ánodos de sacrificio.
Aplicaciones prácticas de la protección catódica
Protección catódica de depósitos de agua dulce. Los depósitos de agua potable, tanto industriales como domésticos, también se pueden proteger de la corrosión mediante protección catódica. En este caso se prefiere el sistema de ánodos galvánicos o de sacrificio. En la figura 26 se ilustra la protección de un tanque de agua potable con ayuda de un ánodo de sacrificio.
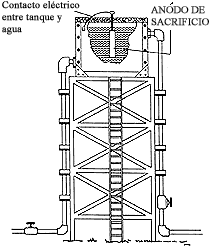
Figura 26. Esquema de protección catódica con ánodo de sacrificio de un tanque
de agua.
Protección catódica de tuberías enterradas. Quizá uno de los casos donde es
más empleada la protección catódica es en las tuberías enterradas. Los miles
y miles de kilómetros de tuberías enterradas que se utilizan para transportar
agua o petróleo están protegidos por lo general mediante tratamiento catódico,
además de determinados revestimientos, cuando el caso lo requiere. Básicamente,
se determina la resistencia del suelo para identificar aquellos lugares en los
cuales, cuando tal resistencia es baja es indicio de posibilidad de corrosión.
En la figura se representa el esquema de un montaje de protección catódica de una tubería con ánodos de sacrificio, comúnmente empleado en la práctica. Se citan estos ejemplos, como algunas de las aplicaciones más frecuentes de la protección catódica. Ahora bien, su campo es mucho más amplio ya que, en general, por este procedimiento se pueden proteger los metales que están en contacto con medios conductores agresivos.
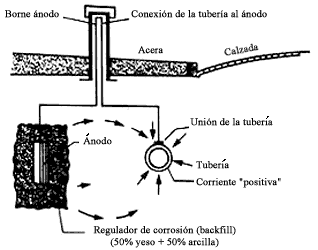
Figura 27. Protección de una tubería enterrada con ánodo de sacrificio.
3. LOS INHIBIDORES DE LA CORROSIÓN
Los inhibidores son sustancias químicas que protegen al metal contra el ataque electroquímico de soluciones agresivas. Son usados ampliamente por la industria para modificar el comportamiento de las aguas, a efectos de un mejor control de la corrosión.
El principio del funcionamiento de los inhibidores es formar en la superficie misma de los electrodos de la pila causante de la corrosión, sea un compuesto insoluble, sea la fijación de una determinada materia orgánica, con el objeto de polarizar la pila de corrosión.
El comportamiento de los inhibidores puede ser muchas veces peligroso, ya que en función de la concentración o de las circunstancias, pueden jugar tanto el papel de inhibidores como de estimuladores de la corrosión.
Los hay de dos tipos, aunque a veces se utiliza una combinación de ambos: —inhibidores anódicos— hidróxido sódico, carbonato, silicato y barato de sodio, ciertos fosfatos, cromato sódico, nitrito y benzoato de sodio, etc; —inhibidores catódicos— sulfato de cinc, sulfato de magnesio, bicarbonato de calcio, etc.
La disolución del acero en aguas de pH neutro tiene lugar en ánodos asociados con defectos en la capa superficial del óxido formado sobre el acero. En cambio, la reacción catódica puede ocurrir en cualquier lugar de la superficie. La combinación de ánodos muy pequeños y una gran superficie catódica, conduce a la llamada corrosión localizada (picaduras). Los inhibidores anódicos actúan formando un compuesto insoluble (óxido férrico), el cual precipita en los lugares anódicos, evitando la reacción anódica y por tanto, inhibiendo todavía más la corrosión.
Los inhibidores catódicos, en cambio, actúan sobre toda la superficie y son menos eficaces. Reducen la corrosión mediante la formación de una capa o película de alta resistencia eléctrica sobre la superficie, la cual funciona como una barrera para la corriente de corrosión.
Uno de los principales problemas de los inhibidores anódicos es que tienen que estar presentes en una concentración suficiente, con el objeto de asegurar que cualquier posible defecto en la película de óxido será cubierto, ya que, de lo contrario puede ocurrir una corrosión por picaduras (localizada) muy intensa. Este riesgo se puede minimizar utilizando los llamados sistemas de inhibidores de efecto sinergético, los cuales, básicamente, son mezclas de inhibidores anódicos y catódicos. El constituyente catódico disminuye la velocidad de corrosión y así permite al constituyente anódico "sellar" la capa de óxido con una concentración mucho menor que si estuviera actuando solo. Actualmente, los sistemas de inhibidores que se están empleando para el control de la corrosión de aguas son de este tipo, por ejemplo, el sistema cromato/polifosfato de cinc. En los medios ácidos, los cuales disuelven la película superficial protectora de óxido formada sobre el acero, los inhibidores anteriores, obviamente, no tienen efecto. En este caso se emplean los llamados inhibidores de adsorción específica —moléculas orgánicas— que aislan el metal del medio ácido, protegiendo la superficie por adsorción. Algunos inhibidores de adsorción actúan predominantemente sobre la reacción anódica, mientras otros lo hacen sobre la catódica.
Hay que tener muy presente cuando se emplean estos inhibidores que los procesos de adsorción, muy a menudo son muy específicos y están afectados por muchos factores, como la temperatura, la velocidad de flujo del medio y las impurezas presentes en la superficie metálica. Todos estos factores deben ser evaluados cuidadosamente, antes de recomendar el uso de un inhibidor de adsorción.
El empleo de los inhibidores de la corrosión, entra dentro del control de ésta por modificación del medio ambiente. Los ambientes más comunes asociados con la corrosión son de tres tipos: aguas, la atmósfera y los suelos.
En el caso del agua hay que tener en cuenta todos los aspectos de la composición de ésta. Todas las aguas que están en contacto con metales, tanto en los procesos industriales como de otra naturaleza, provienen sea del agua de mar, sea del agua de lluvia. Por tanto, puede haber una gran variación en su composición química.
El principal método de tratamiento de aguas para control de la corrosión es la eliminación del oxígeno disuelto, junto con la adición de inhibidores. La presencia de oxígeno disuelto en el agua acelera la reacción catódica y, consecuentemente, la velocidad de corrosión aumenta en proporción a la cantidad de oxígeno disponible en el cátodo.
La eliminación tanto del oxígeno disuelto como del anhídrido carbónico (CO2) de las aguas, antes de su uso, constituye un camino importante para el control de la corrosión no sólo del hierro y acero, sino también del cobre, bronce, cinc y plomo. El oxígeno puede ser eliminado por medios físicos de-aireación o químicos-de activación.
La de-aireación se puede llevar a cabo subiendo la temperatura, bajando la presión o purgando el agua por paso de un gas inerte.
La de-activación química se realiza por tratamiento del agua con hidrazina o sulfito sódico.
Por lo que se refiere a la atmósfera hay que tener en cuenta que la corrosión depende fundamentalmente de dos factores: la presencia de contaminantes (partículas sólidas en suspensión, impurezas gaseosas como el anhídrido sulfuroso, SO2) y el contenido de humedad del aire.
La humedad relativa es muy importante al considerar los problemas relacionados con la corrosión atmosférica. El hierro libre de óxido no desarrolla la herrumbre en aquellas atmósferas cuya humedad relativa es del 70% o menor. En general, para cualquier metal que se pueda corroer en la atmósfera, hay un valor crítico de la humedad relativa, por debajo del cual no se corroe. Este valor crítico de la humedad está determinado grandemente por la naturaleza higroscópica de algún contaminante sólido que pueda estar presente y por la del producto o productos de corrosión formados. De aquí la gran influencia ejercida por los contaminantes atmosféricos.
Los métodos de control más efectivos para minimizar la corrosión atmosférica tendrían que ver con la modificación de la atmósfera, eliminando los contaminantes, particularmente el SO2. Esto no puede realizarse en el exterior y debe recurrirse a la protección de las estructuras y equipos sometidos a la intemperie, por alguno de los métodos citados anteriormente (pinturas, recubrimientos metálicos, etc.).
La corrosión en los suelos se parece en muchos aspectos a la corrosión por las aguas. En ambos casos, el electrolito contiene sustancias disueltas que alteran su comportamiento. La corrosión de un suelo puede cambiar de un área a otra por simple cambio de composición. Los principales factores que determinan cuándo un suelo es susceptible de ser agresivo con respecto a una estructura metálica enterrada son: la humedad, el acceso de oxígeno (aireación), conductividad eléctrica (la cual está influenciada por la presencia de sales disueltas) y el pH del suelo. No hay que olvidar que muchos problemas de corrosión de metales enterrados provienen de las llamadas corrientes eléctricas parásitas o vagabundas, producidas por ejemplo por los trenes eléctricos.
Como ya se ha indicado, el método más utilizado para prevenir la corrosión de metales o estructuras enterradas es la protección catódica, junto con un adecuado revestimiento (tela asfáltica por ejemplo).
Selección de materiales en medios agresivos
El control de la corrosión es sólo uno de los muchos factores que intervienen en la selección de un material. El ingeniero de materiales al efectuar una determinada selección debe tener en cuenta una serie de factores, como propiedades físicas y mecánicas del material, resistencia a la corrosión, disponibilidad, facilidad de trabajo, etc., además de los aspectos económicos, antes que pensar en el material en sí mismo. La selección debería realizarse en base al material más económico, pero que reuniera la combinación de propiedades necesarias para el uso que se le va a dar.
Las consideraciones económicas son muy importantes, así como el tiempo de vida esperado para el equipo e instalación. No se trata, por ejemplo, de esperar un material más barato, si el costo de la demora puede llegar a ser mayor que el de un material más caro, pero del que se tiene una disponibilidad inmediata. Tampoco se trata de seleccionar un material muy resistente a la corrosión, y por lo general muy caro, que supere largamente la duración prevista para el equipo. Lo mismo puede aplicarse en el caso de los recubrimientos.
Tanto el diseño como el mantenimiento planificado deben ser tenidos muy en cuenta a la hora de realizar la selección de un material con miras a un buen control de la corrosión.
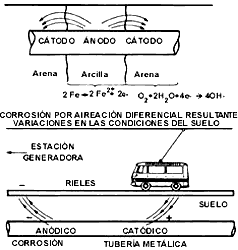
Figura 28. Corrosión de una tubería enterrada causada por corrientes eléctricas
parásitas producidas por un tranvía.
El control de la corrosión debe realizarse, siempre que sea posible, desde la etapa misma del diseño del componente o de la planta. Evitar dentro de las limitaciones del propio diseño la formación de huecos o cavidades en los cuales pueda quedar atrapada el agua, eliminar el contacto directo de metales disímiles (pares galvánicos), así como proporcionar un acceso fácil para un posterior y planificado mantenimiento por pintura durante el servicio, por ejemplo, constituyen alguna de las normas de buena práctica que ayudarán a un mejor control de la corrosión.
Tipos de materiales disponibles
Ya que la corrosión es un proceso electroquímico, un camino evidente para evitarla es el empleo de materiales químicamente resistentes. Plásticos, cerámicas, vidrios, gomas, asbesto y cemento entran dentro de esta categoría. El problema es que en muchos casos no tienen o no reúnen aquellas otras propiedades —diferentes a la resistencia a la corrosión— como para satisfacer los requerimientos de servicio.
Los metales difieren mucho en cuanto a su resistencia a la corrosión. Por ejemplo, los metales nobles como el platino y el oro son inherentemente resistentes a muchos medios agresivos; el cromo y el titanio tienen una buena resistencia a la corrosión; el acero, el cinc y el magnesio se corroen fácilmente. La resistencia a la corrosión "intrínseca" de un metal depende de muchos factores, incluyendo su posición en la serie galvánica, así como la adherencia y compacidad de la película formada en su superficie en contacto con el aire o el medio de servicio. Con una película de óxido protectora, el material se comporta como un metal noble, en el supuesto de que exista suficiente oxígeno en el medio como para reparar los defectos en la película, a medida que se formen.
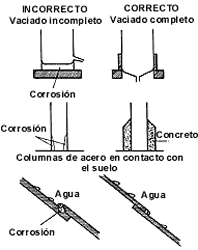
Figura 29. Diseños "geométricos" que pueden contribuir a evitar la corrosión.
El objetivo en último término, consiste en seleccionar el material más económico compatible con las demandas y especificaciones de la aplicación en particular.
Aparte de la resistencia a la corrosión, la selección obvia para muchas aplicaciones es un acero al carbono. El acero tiene una resistencia "intrínseca" a la corrosión pequeña, pero aleándolo se tiene el medio de combinar lo económico del acero con la intrínsicamente alta resistencia a la corrosión de metales relativamente costosos, como el cromo.
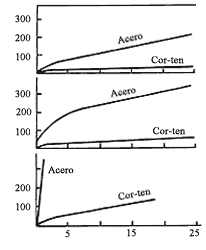
Figura 30. Efecto de pequeñas adiciones de aleantes en la resistencia del acero a la corrosión atmosférica. El acero Cor-ten (acero patinable) contiene 2-3% de aleantes, particularmente cobre, cromo, fósforo.
Añadiendo cuanto menos un 0.2% de cobre a un acero al carbono se aumenta considerablemente su resistencia a la corrosión atmosférica, transformando la herrumbre en un producto más compacto y adherente.
El cromo, aluminio, titanio, silicio, tungsteno y molibdeno forman películas de óxidos protectores y sus aleaciones están similarmente protegidas.
El níquel también forma aleaciones con una buena resistencia a la corrosión en medios ácidos, incluso cuando el contenido de oxígeno del medio es bajo.
Veamos algunos de los tipos más comunes de aleaciones resistentes a la corrosión utilizados en la práctica.
Existen tres tipos principales. Los aceros inoxidables martensítico y ferrítico contienen entre un 11 y un 18% de cromo. El acero inoxidable austenítico contiene aproximadamente entre un 16 a 27% de cromo y de un 8 a 22% de níquel. La resistencia más elevada a la corrosión se logra con el acero inoxidable austenítico.
Los aceros inoxidables mejoran sus características de resistencia a la corrosión en medios oxidantes o de buena aireación, que aseguran el mantenimiento de su película protectora superficial, pero están sujetos a corrosión por picaduras, por hendiduras y corrosión bajo tensión en ciertos medios específicos, y son resistentes a la corrosión atmosférica, ácido nítrico, algunas concentraciones de ácido sulfúrico y muchos ácidos orgánicos.
El cobre es resistente en agua de mar, agua corriente fría o caliente, ácidos deareados y no-oxidantes y al ataque atmosférico.
Ciertos elementos aleantes mejoran sus propiedades físicas y mecánicas y también su resistencia a la corrosión. De aquí la utilización de los bronces de aluminio y de las aleaciones cobre-níquel para los tubos de los condensadores. Los bronces de aluminio también se emplean para la construcción de los cuerpos de las bombas y de las hélices de los barcos.
El aluminio ofrece una buena resistencia a la corrosión atmosférica y a muchos otros medios agresivos, como por ejemplo: ácido acético, ácido nítrico ácidos grasos, atmósferas sulfurosas, etc. Se fabrican aleaciones de aluminio con pequeñas adiciones de otros metales, principalmente con el objeto de mejorar sus propiedades mecánicas y físicas las aleaciones aluminio —magnesio y aluminio— manganeso son las que presentan una mayor resistencia a la corrosión, seguidas por las aleaciones de aluminio—magnesio—silicio y aluminio—silicio. En cambio las aleaciones de aluminio que contienen cobre son las que presentan menor resistencia a la corrosión.
El níquel es resistente a los álcalis en frío y caliente, ácidos orgánicos y ácidos inorgánicos no oxidantes diluidos, así como a la atmósfera. La adición de cobre mejora su resistencia a la corrosión en los medios reductores y en el agua de mar.
El cromo aumenta su resistencia a la corrosión en los medios oxidantes. La presencia de molibdeno como aleante también aumenta la resistencia en condiciones reductoras. La adición de cobre y molibdeno mejora la resistencia a la corrosión tanto en medios reductores como oxidantes.
El titanio y sus aleaciones tienen una gran resistencia a la corrosión en agua de mar y en atmósferas industriales, de tal manera que no necesitan protección. También se pueden utilizar con buenas garantías en las plantas químicas.