XIII. APLICACIÓN A LÍQUIDOS
COMO se vio en capítulos anteriores el estado cristalino se caracteriza por tener un alto grado de orden interno. Este se da debido a la repetición prácticamente idéntica del arreglo de los átomos del cristal. Esta repetición ocurre a lo largo de distancias macroscópicas, del orden de centímetros o aun de metros. Esto significa que, desde el punto de vista microscópico, hay orden a largo alcance. Este concepto implica lo siguiente: la celda unitaria, o sea el "ladrillo" básico con el que se construye el cristal, se repite muchos miles de millones de veces a lo largo de toda la sustancia.
Una consecuencia del orden a largo alcance que existe en un cristal es que si movemos un extremo del cristal, casi instantáneamente se mueve su otro extremo. Se dice que hay una correlación de largo alcance. Lo anterior significa que el átomo de un extremo, el que recibió nuestro movimiento, está íntimamente ligado con el átomo que se encuentra en el otro extremo del cristal, de manera tal que al mover el primero, el segundo a pesar de encontrarse muy lejos de él también "siente" la acción que aplicamos nosotros al cristal. Estos dos átomos no son independientes. Uno de ellos será afectado por lo que haga el otro.
El orden que muestra una sustancia cristalina no existe en los líquidos, los gases, los vidrios y otra clases de sustancias amorfas. Nos dedicaremos primero a hablar de algunas características de los líquidos.
Se han realizado experimentos en los cuales se hace incidir sobre un líquido un haz de rayos X o de neutrones. Resulta que el líquido sí difracta estas radiaciones. En cierta forma lo que ocurre es algo análogo a lo mostrado en la figura 15, donde se ve la difracción de luz por una rejilla en dos dimensiones en la cual las rendijas no están ordenadas. En este caso sí hay difracción.
El patrón de difracción que produce un líquido es muy distinto al producido
por un cristal. De un análisis muy detallado de estos patrones de difracción
se ha podido inferir que el líquido es una sustancia que tiene cierto orden.
En efecto, resulta que en la cercanía (hablando en términos microscópicos) de
un átomo hay cierta estructura, que a medida que se va uno alejando de él se
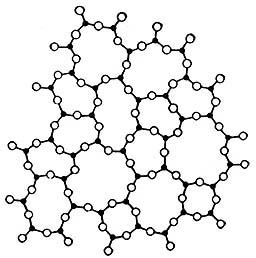
va perdiendo (véase la Figura 28 ). Esto quiere decir que en un líquido existe
únicamente orden a corto alcance. Este alcance corresponde sólo a distancias
de unos cuantos angstrom.
Cuando hablamos de orden a largo alcance nos referimos a la existencia de regularidad a través de distancias macroscópicas, digamos del orden de centímetros. Recuérdese que un centímetro es igual a cien millones de angstrom. Cuando decimos que hay orden de corto alcance, éste solamente se extiende a lo largo de distancias de unos cuantos angstrom (10-8 cm), o sea que es un orden microscópico.
Debido a que en un líquido no hay orden a largo alcance, entonces tampoco hay seguridad de que a cierta distancia de un átomo esté colocado otro átomo, como ocurre en un cristal. A causa de ello solamente se puede describir la estructura de un líquido en términos de la probabilidad de encontrar un átomo a cierta distancia de otro. Esta probabilidad queda dada por una cantidad que se llama la función de correlación de posiciones. La correlación es una medida del grado de dependencia de un átomo con otro colocado a cierta distancia. Esta cantidad es tal que si su valor es distinto a uno, entonces hay correlación entre dos átomos, es decir, en este caso los átomos no son independientes uno del otro. Si su valor es igual a uno, entonces los dos átomos son independientes, es decir, no están correlacionados.
Por medio de la espectrometría de neutrones se ha podido encontrar la función
de correlación en diferentes líquidos. En la figura 29 se muestra, por ejemplo,
la función de correlación de posiciones para el argón líquido a una temperatura
de -125°C,1 como función de la distancia entre dos átomos.
El argón, aun en el estado líquido, no se agrupa en moléculas por lo que únicamente
se encuentra con un solo átomo.
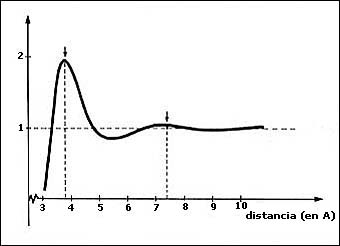
Figura 29. Función de correlación de posiciones del argón líquido a -125°C.
Los picos muestran una estructura a corto alcance.
Nos damos cuenta de que esta gráfica tiene varios picos: el primero está centrado a la distancia de 3.8 Å y el segundo a 7.4 Å. A medida que la distancia entre los átomos aumenta, después del segundo pico, la correlación oscila muy levemente y se acerca paulatinamente al valor uno. Estos resultados significan que, efectivamente, hay una correlación de corto alcance. A una distancia de 3.8 Å de cualquier átomo del líquido hay una probabilidad muy alta de que haya otro átomo. Hay también una probabilidad menor, de que haya otro átomo a una distancia de 7.4 Å del primer átomo mencionado. Este hecho es, por decirlo así, una herencia de la estructura cristalina que tiene la sustancia cuando, habiendo solidificado, forma un cristal. Sin embargo, al aumentar la distancia entre los átomos ya casi no hay probabilidad de encontrar otro átomo a una distancia mayor. De hecho, para distancias de 8 Å o mayores, como se ve en la gráfica, los átomos son prácticamente independientes. Es decir, ya no hay ni siquiera restos de algún orden en la sustancia. El orden en el argón líquido es entonces de corto alcance ya que se mantiene solamente hasta distancias de alrededor de 8 Å, que es una distancia microscópica.
Otro ejemplo interesante es la función de correlación de posiciones para el
agua a una temperatura de 20°C, que se muestra en la figura 30. A diferencia
del caso anterior en que tratamos un líquido de un solo átomo, ahora tenemos
un líquido compuesto de moléculas, H2O. La gráfica muestra
dos picos muy intensos a las distancias de 1 Å y de 2.9 Å.
Asimismo, hay otros dos picos leves a las distancias de 4.5 Å y
de 7 Å. Veamos lo que significan estos picos.
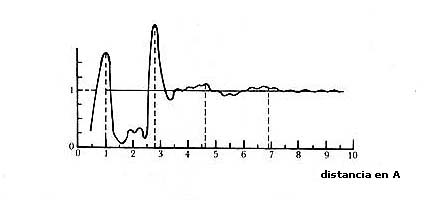
Figura 30. Función de correlación de posiciones de agua a 20°C. El primer
pico da la distancia entre los átomos de oxígeno y de hidrógeno dentro de la
molécula. Los otros picos muestran estructura microscópica entre las moléculas
de agua.
El pico en 1 Å representa la distancia que hay entre cada átomo de hidrógeno y el de oxígeno en la molécula de agua. Es decir, es la distancia dentro de la molécula.
El pico a la distancia de 2.9 Å representa la distancia entre dos moléculas de agua. Este segundo pico implica que hay un orden de corto alcance. Los otros dos picos a distancias mayores indican un remanente de la estructura del agua cristalina, o sea del hielo. Por lo tanto, se puede decir que el agua en cuestión tiene una estructura como sigue: alrededor de una molécula hay tres capas de moléculas y cualquier molécula situada a distancias mayores de 8 Å es independiente, es decir, a distancias de 8 Å se tiene ya un líquido sin estructura.
Una sustancia muy interesante es el vidrio. Se ha estudiado su estructura microscópica y resulta que el vidrio no es un cristal. Esto quiere decir que no tiene una estructura microscópica ordenada y repetitiva. Su estructura es amorfa y muy parecida a la que tienen los líquidos. Se ha obtenido experimentalmente la función de correlación para vidrios y resulta sorprendentemente parecida a la de los líquidos. Se puede decir que el vidrio es un líquido que se ha "congelado" y que sus moléculas no tuvieron tiempo suficiente para ordenarse y formar un cristal. De hecho, se le puede también describir como un líquido que tiene una viscosidad extremadamente alta por lo que no puede fluir como lo hace un líquido común y corriente.
Lo anterior significa que no todas las sustancias sólidas son cristales. Existen también sólidos que son amorfos. Sus átomos o moléculas no forman una estructura regular, ordenada o repetitiva de largo alcance.
NOTAS
1 A la temperatura ambiente, digamos 20°C, y la presión de la atmósfera, el argón no es líquido sino gaseoso.