II.SÍNTESIS DE UNA ZEOLITA
CÓMO HACER ZEOLITAS |
POR ahora sabemos lo que es una zeolita, o sea que estamos en
condiciones de definirla y de probar si un compuesto es o no es una zeolita.
Lo hicimos paso a paso con los polvos contenidos en aquella pequeña botella.
Aunque ya sabemos reconocer zeolitas aún no estamos en condiciones de prepararlas
¡una cosa es saber y otra hacer!
Este capítulo se consagrará por entero al "hacer". Sentaremos las bases para preparar zeolitas y, para ser consistentes, lo centraremos en la obtención de zeolitas faujasitas. Desde luego, en una primera parte observaremos cómo se forman las zeolitas en la naturaleza para duplicar estos procesos en el laboratorio. Así, seguiremos los pasos de los primeros investigadores que, imitando los fenómenos naturales consiguieron sintetizar zeolitas. Desgraciadamente, la mayor parte de sus trabajos se ha tenido que descartar debido a análisis insuficientes de los compuestos resultantes.
LAS ZEOLITAS Y SU ÁRBOL GENEALÓGICO |
¿Cómo se forman las zeolitas y de dónde provienen? Queremos saber en qué condiciones y a partir de qué compuestos se consigue, en la naturaleza, la síntesis de las zeolitas. Aunque ahora no sea una clasificación lo que buscamos sino una evolución en el tiempo, digamos que una "historia", nuevamente nos vemos obligados a recurrir a la geología.
El experimento más sencillo sería observar en el laboratorio los procesos naturales, o sea, cristalizar muy lentamente una gran cantidad de roca fundida cuya composición promedio fuese próxima a la de la litosfera. Aunque este experimento es difícilmente realizable los geólogos aseguran, basándose en los fenómenos volcánicos, que la secuencia de cristales depositados sería clara. A medida que la lava fluida, homogénea y a muy alta temperatura, se enfriase aparecerían primero cristales sin silicatos (o sea, sin átomos de silicio, Si) como los cristales de magnetita (Fe3O4). Luego se detectaría la formación de ortosilicatos, por ejemplo el olivino (Mg2SiO4 con contenido variable de Fe2SiO4) y secuencialmente vendrían los metasilicatos y los feldespatos que son los minerales más corrientes en la corteza terrestre. Un ejemplo es la ortoclasa (K Al Si3O8 con pequeño contenido de Na y Ca), el cuarzo (SiO2) como mineral primario y mezclas de minerales como el granito (que está compuesto por cuarzo, feldespato y mica). En condiciones particulares, estos últimos sólidos darían origen a las arcillas, las zeolitas y a la larga a alúminas como la bauxita.
Cuando el enfriamiento fuese tal que la lava cristalizase suficientemente como para dar un magma basáltico rico en álcalis sería probable que se formasen zeolitas por medios acuosos salinos y alcalinos (Cuadro 2). La "zeolitización" también se provoca mediante una caída súbita de la temperatura en una lava basáltica.
CUADRO 2. Formación de zeolitas en la naturaleza.
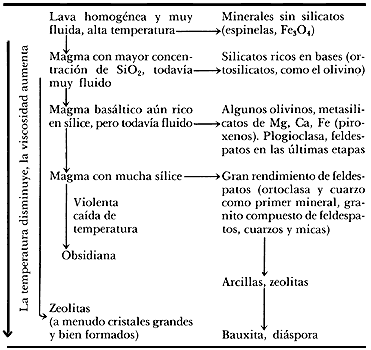
Hay que recordar aquí que a tan altas temperaturas se pueden generar enormes presiones que, a su vez, pueden acelerar los procesos de cristalización. Cuando la presión alcanza valores extremos es probable que ocurran explosiones, ése fue el caso del monte Pelée, en la isla de Martinica.
Un ejemplo clásico de zeolitas formadas naturalmente son las zeolitas presentes en las rocas volcánicas de Sicilia, que incluyen la analcima, la chabasita y su variante, la herschelita, la epistilbita, la gmelinita, la gonnardita, la mesolita y la thomsonita. Los cristales de zeolita suelen crecer bien, lo cual es típico de las reacciones hidrotérmicas en soluciones* de rocas ricas en álcalis, como por ejemplo, los basaltos. Las zeolitas debidas a alteraciones hidrotérmicas de corrientes de lava basáltica en regiones geotérmicas existen en muchas partes del mundo, por ejemplo, en los baños romanos de Plombières (Francia) o en el parque de Yellowstone (EUA). Se trata entonces de zeolitas de origen volcánico.
Por otro lado, como lo discutimos anteriormente (Cuadro 2), las zeolitas también pueden provenir de sedimentos. En este caso se caracterizan por ser aglomerados de cristales de muy pequeñas dimensiones y a menudo con caras cristalinas mal desarrolladas. De todas las zeolitas de origen sedimentario, por ahora, es la clinoptilolita la que parece ser la más abundante. Son este tipo de formaciones las que han dado los grandes depósitos de interés tecnológico.
¿Y EN MÉXICO? |
Siendo México un país en donde hay numerosas zonas volcánicas, es de esperarse que haya zeolitas naturales. Sin embargo, no es sino hasta 1973 cuando F.F. Mumpton publica en la revista American Mineralogist, 28,287 (1973) un artículo que titula "First Reported Occurrence of Zeolites in Sedimentary Rocks of Mexico" (Primer informe sobre la presencia de zeolitas en rocas sedimentarias de México). De ese trabajo transcribimos los siguientes párrafos pues preferimos que sea el mismo Mumpton quien describa el descubrimiento:
Durante las primeras etapas de la exploración para encontrar zeolitas
en este país [se refiere a EUA] (1958-1962), la similitud geológica
de las regiones volcánicas y piroclásticas entre el norte de México y el
sur de Arizona y California sugería que deberían existir yacimientos de
zeolitas al sur de la frontera; sin embargo, no se hizo ningún esfuerzo
por probar esta posibilidad, y hasta la fecha no se ha informado de minerales
zeolíticos en las rocas sedimentarias de México. |
Durante el verano de 1972 el autor examinó una serie de sedimentos piroclásticos
del valle del río Atoyac, alrededor de 15 km al noroeste de Oaxaca, en el sur
de México. Aunque límites de tiempo impidieron una exploración extensiva del
área, se recogieron varias muestras de un prominente yacimiento verde, situado
como a unos 100 m al este de la supercarretera 190, a 3 km al norte del pueblo
de Etla. Exámenes subsecuentes por difracción de rayos X*
de estas muestras indicaron que el yacimiento está constituido casi únicamente
por zeolitas, mordenita y clinoptilolita. Esta identificación confirma lo que
se cree ser el primer descubrimiento de zeolitas minerales en rocas sedimentarias
de México.
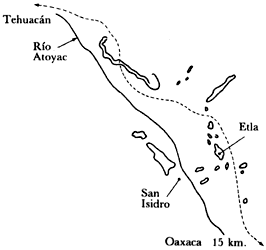
Figura 12. Yacimientos de zeolitas en la zona de Etla, Oaxaca (1978).
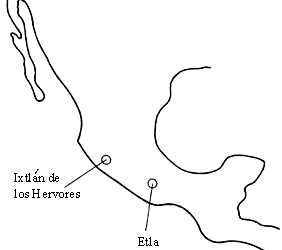
Figura 13. Yacimientos de zeolitas en la República Mexicana.
Mumpton describe el yacimiento y hace notar que este tipo de piedra se usa en Oaxaca
| [...]en los edificios, los muros, los cimientos y otras estructuras desde tiempos de los mayas, y predominan en los famosos edificios arqueológicos de Mitla y Monte Albán. Fue la presencia de tal material en los muros de la catedral central en Oaxaca lo que llamó la atención del autor y propició la exploración de campo subsecuente. |
En la figura 12 presentamos la geografía de la zona. Este mismo yacimiento es el que Liberto de Pablo incluye en el mapa que reproducimos, simplificado, de su sobretiro "The clay deposits of Mexico" (Yacimientos de arcillas en México), trabajo presentado en la Conferencia Internacional de Arcillas en 1978. Cinco años después del hallazgo de Mumpton ya figura, no sólo el yacimiento de Etla, sino que también el de Ixtlán de los Hervores (Figura 13). Y en 1987 se han reportado dos nuevos yacimientos, esta vez en el estado de Sonora, uno rico en clinoptilolita en el municipio de Rayón y el otro conteniendo erionita en el municipio de Agua Prieta.
SÍNTESIS DE UNA ZEOLITA |
Los antecedentes geológicos (Cuadro 2), sugieren que las zeolitas se generan a partir de un magma basáltico rico en SiO2 cuando disminuye la temperatura. También se forman si este magma se pone en contacto con soluciones salinas y alcalinas. Experimentemos, entonces.
Nuestro objetivo va a ser destruir la estructura de los materiales iniciales, separar los tetraedros de silicio y los octaedros de aluminio y volverlos a cristalizar. De hecho, esta cristalización sólo es un nuevo arreglo de los octaedros de aluminio y los tetraedros de silicio que constituyen los compuestos iniciales. Si los tetraedros de Si y octaedros de Al estaban ordenados en cierta forma, ahora queremos "soltarlos" y volverlos a "fijar". Es como jugar al Meccano.
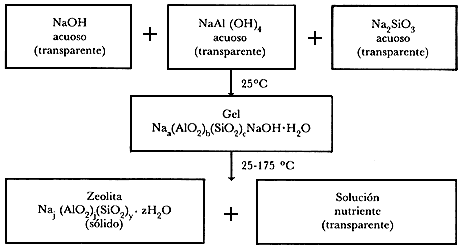
Iniciemos la síntesis a partir de tres soluciones acuosas: sosa (NaOH), NaAl (OH)4 y Na2SiO3. Son soluciones típicas, transparentes y fluidas; las partículas de soluto están distribuidas homogéneamente en el disolvente. Mezclamos sin problemas el NaOH con el aluminato de sodio. Sin embargo, a medida que se va añadiendo la solución de silicato a la mezcla de aluminato y sosa, muy lentamente, a goteo, se nota que la solución resultante se vuelve turbia; ahora el líquido es gelatinoso y viscoso. Se ha formado un gel*...
La estructura del gel se debe a una reacción* en la cual se forman moléculas grandes a partir de muchas moléculas pequeñas (en química se habla de una polimerización*). La composición y la estructura del gel polimerizado hidratado están controladas por el tamaño y la estructura de las especies que se polimerizan. Diferencias en la composición química y el peso molecular* de las especies iniciales en las soluciones silicato conducen a diferencias en las estructuras del gel y por lo tanto a diferencias mayores en las fases zeolitícas producidas.
Los geles típicos se preparan a partir de aluminato de sodio, silicato de sodio
e hidróxido de sodio porque todos son solubles. Durante la cristalización del
gel, los iones de sodio y los componentes aluminato y silicato se acomodan paulatinamente
y tienden a la estructura ordenada de un cristal, lo cual se debe a la depolimerización
del gel debido a los iones hidroxilos (OH) presentes en la mezcla
reactiva.
CUADRO 3. Síntesis de una zeolita.
 |
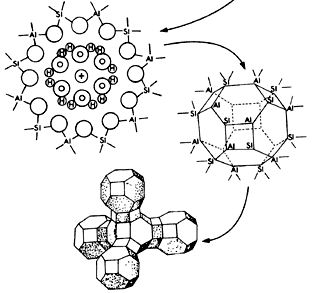 |
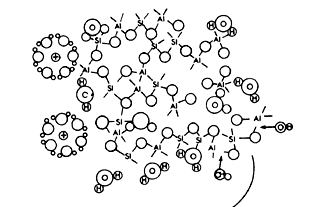
Figura 14. Síntesis de una zeolita; mecanismo de cristalización.
Viene entonces la formación de núcleos, que son pequeños cristales que a su vez sirven de base para que se formen los cristales grandes de zeolita. Estos núcleos, como en cualquier proceso de este tipo, crecen durante el periodo de cristalización. Como en los geles supersaturados se forma un gran número de núcleos cristalinos, el producto final consiste en un polvo finamente dividido en pequeños cristales usualmente de sólo unas cuantas micras.
La naturaleza de la zeolita obtenida queda determinada por las condiciones de la síntesis, o sea las concentraciones de los reactivos, el pH, el tiempo, la temperatura y la naturaleza, y la concentración de los promotores* que se introduzcan. Muchas de las fases formadas no son fases en equilibrio, son metaestables, que con el tiempo se convierten en otras fases más estables, así se trate de zeolitas o minerales. Las reacciones químicas que describen la síntesis de la zeolita están dadas en el cuadro 3 y en la figura 14.
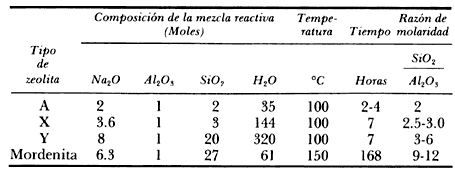
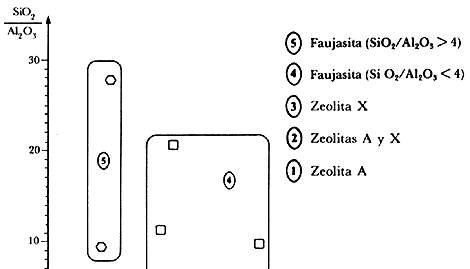
La zeolita resultante se debe separar en el momento apropiado y lavar cuidadosamente hasta eliminar de la estructura porosa los productos que no hayan reaccionado. En el cuadro 4 resumimos las condiciones típicas para sintetizar algunas zeolitas importantes. En la figura 15, dependiendo de la razón de molaridad inicial Na2O/SiO2 y SiO2/Al2O3, se predice el tipo de zeolita que se obtiene. Estos resultados son válidos siempre y cuando se trabaje con sales solubles y rangos de temperatura de cristalización entre 85 y 100°C, lo cual no siempre es el caso.
CUADRO 4. Condiciones típicas para sintetizar algunas zeolitas.
 |
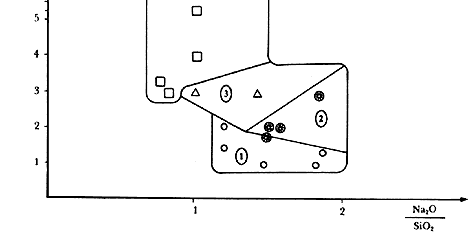 |
Figura 15. Tipos de zeolitas sintetizadas según la proporción de óxidos.
Más aún, también se pueden sintetizar zeolitas a partir de minerales, los caolines*
en particular, cuya composición, en lo que toca al contenido de Si y Al, es
muy próxima a la de algunas zeolitas. Esta alternativa de obtención resulta
interesante para nuestro país ya que las sales de aluminio se tienen que importar.
Para que la síntesis sea eficaz hay que destruir por completo la red del caolín
antes de preparar el gel. De allí que todas las patentes o artículos que tratan
el tema propongan un tratamiento térmico extremo, preliminar a la disolución
del caolín. Por ejemplo, si se desea obtener zeolita A o faujasita a partir
de caolín proveniente de la región de Huayacocotla, Veracruz, hay que calcinarlo
entre 750 y 1 000 °C. En el cuadro 5 presentamos los resultados obtenidos:
se comprueba que dependiendo de la temperatura de calcinación se obtiene una
u otra zeolita y que las relaciones de la figura 15 no son válidas en este caso.
CUADRO 5. Dependencia entre el tipo de zeolita obtenida y la temperatura de calcinación del caolín

No queremos cerrar este capítulo sin mencionar que fue R.M. Barrer, en Inglaterra, el primero en sintetizar, por el procedimiento que hemos descrito, las contrapartes sintéticas de zeolitas; tales como la mordenita, analcima, etc. En 1953, R.M. Milton y colaboradores en EUA prepararon zeolitas cristalinas sintéticas mediante procesos de baja temperatura que fueron altamente exitosos y que no sólo reprodujeron zeolitas naturales (faujasita, chabasita), sino que generaron muchas especies nuevas de zeolitas, como es el caso de la zeolita A.
ZEOLITAS SOBRE PEDIDO |
Hemos hablado de tetraedros que se juntan esquina con esquina hasta formar esa red porosa llamada zeolita, red en la cual se encuentran cavidades, ventanas y túneles y en donde se pueden alojar iones como el sodio (Na), el potasio (K) o el calcio (Ca) y en donde cabe un número variable de moléculas de agua. Esos tetraedros son las unidades fundamentales de la estructura, los hay con un átomo de silicio en el centro o bien con un aluminio.
Sin embargo, no parece ser de mayor trascendencia que los tetraedros sean de silicio o de aluminio siempre y cuando se respete el equilibrio de cargas, o sea que las cargas libres debidas a la presencia del Al se neutralicen con otros iones. Se nos ocurre entonces sintetizar zeolitas a partir de tetraedros en cuyo centro sea otro el átomo. Para que este experimento resulte hay que proponer átomos equivalentes al Si o al Al, o sea que ocupen el lugar del Si o del Al sin alterar demasiado la estructura.
Un caso claro es el del galio (Ga) que por su estructura electrónica puede equipararse con el aluminio. Es más, se tiene el antecedente de que existen galias, así como alúminas. La preparación es análoga a la de las zeolitas con aluminio, la diferencia estriba en que las sales iniciales son de silicio y galio. La zeolita resultante difiere de la que contiene aluminio porque el parámetro de la red ya no es el mismo. En este tema no parece haber límite y día a día se reportan síntesis originales de sólidos con estructura zeolítica a partir de Be, Cr, Fe, B, Zn, Ge, V, Ti, P, etcétera.
Es más, obsérvese con cuidado la figura 14, donde se ilustra cómo, cuando el
gel cristaliza, existen grandes cadenas flexibles de tetraedros que se organizan
alrededor de cationes y moléculas de agua. Son estos conglomerados, de sodios
por ejemplo, rodeados de moléculas de agua, los que sirven de molde para las
cavidades de las faujasitas. Una vez formados los pequeños núcleos de zeolita,
el crecimiento de los cristales es rápido.
(a)  (b)
(b) 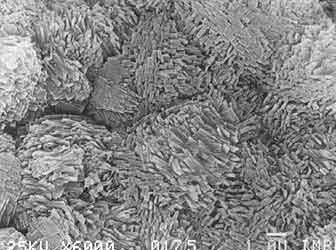
Figura 16. Efecto del sembrado en una zeolita ZSM-5. (a) Zeolita ZSM-5 observada mediante el microscopio electrónico de barrido. (b) Zeolita ZSM-5 obtenida mediante la técnica del sembrado (X 6000).
En los procesos industriales, en los que el tiempo es una variable importante, conviene propiciar la cristalización mezclándole al gel un poco de zeolita cristalina. Así no hay que esperar a que se formen los núcleos de zeolita sino que de inmediato se pasa a la fase de crecimiento de los cristales. Este artificio se conoce como sembrado y es común en la síntesis de cristales diferentes de las zeolitas. Además de facilitar la síntesis de zeolitas A o X de alta pureza, la cantidad y el tipo de semilla determina el tamaño de cristal y el estado de agregación.
Naturalmente, como también ocurre en otros procesos de cristalización, estos factores se controlan mediante distintas variables tales como la agitación, temperatura y composición de los reactivos. Se ha probado que el control de la síntesis mediante el sembrado es una de las técnicas de más valor. Las micrografías de la figura 16 ilustran el cambio en el tamaño de cristal de una zeolita ZSM que se puede obtener mediante sembrado. En este caso el sembrado provoca la disminución del tamaño del cristal por un factor de tres.
Si la cristalización de la zeolita se puede inducir mediante un sembrado, y
si depende de los pequeños núcleos de iones con agua, ¿por qué no intentar alterar
este mecanismo? ¿Por qué no cambiar "los moldes"?
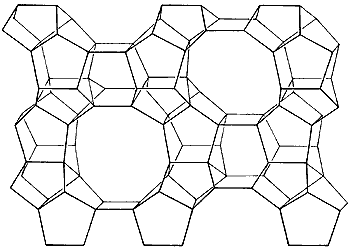
Figura 17. Estructura de una zeolita ZSM-5.
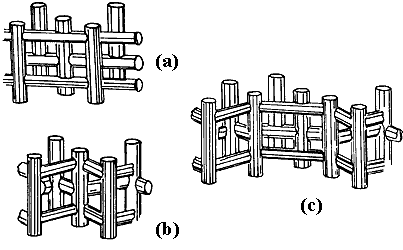
Figura 18. Esquema de la estructura porosa de zeolitas pentasil: (a) ZSM-11; (b) variante intermedia; (c) ZSM-5
Desde luego, es de esperarse que si el molde varía, también lo haga el sólido obtenido. Eso es precisamente lo que hace unos años llevó a cabo Barrer, seguido posteriormente por otros laboratorios como los de la Compañía Mobil. La síntesis se efectuó usando macromoléculas orgánicas como el TPA o el TBA (tetrapropilamonio y tetrabutilamonio). La originalidad de este trabajo consistió en utilizar esas enormes moléculas para que alrededor de ellas se ordenaran los tetraedros de silicio y aluminio. Una vez conseguida la cristalización se eliminan las moléculas orgánicas y sólo queda la zeolita, o sea un esqueleto compuesto de tetraedros de silicio y aluminio cuya porosidad se debe a la estructura del TPA o TBA.
La "receta" para sintetizar este tipo de zeolitas no difiere mucho de las síntesis convencionales de zeolitas, salvo que el componente alcalino que promueve el proceso de polimerización del gel es una base* aminada* orgánica (hidróxido de tetrapropilamonio, por ejemplo, introducido en solución). Las condiciones típicas de cristalización requieren temperaturas entre 150 y 200°C y tiempos de 1 a 7 días.
De hecho, este descubrimiento dio origen a toda una familia de zeolitas designadas con las siglas ZSM, también se le suele llamar pentasil. En la figura 17 se muestra la estructura de la zeolita ZSM-5 (obtenida con TPA). En la figura 18 comparamos la estructura de la zeolita ZSM-5 con la ZSM-11 (obtenida con TBA). Tienen un sistema de canales formados por anillos de 10 átomos. El tamaño de los poros está entre el de las zeolitas con anillos de 8 átomos (como la zeolita A o la erionita) y los anillos de 12 miembros como en las zeolitas faujasitas (X, Y). Dependiendo de cómo se dispongan en el espacio las capas constituidas por la estructura típica pentasil, se obtienen sistemas de canales variables como los de la figura 18.
Entre la ZSM-5 y la ZSM-11, que son las dos estructuras extremas, existe un número infinito de variantes. Como se muestra esquemáticamente en la figura 18, los dos conjuntos de canales (horizontales y verticales) de la ZSM-11 son rectos, mientras que en la ZSM-5 un conjunto de canales es recto y el otro senoidal. Invariablemente, los canales paralelos a las capas son rectos. Como es lógico, el análisis e identificación de semejantes estructuras son muy difíciles y en general, ambiguos.
Esperamos haber convencido al lector de que es posible variar el tamaño de las ventanas, de los poros, de las cavidades, alterar la composición, intercambiar cationes o modificar la hidratación de las zeolitas, en resumen, que se pueden crear materiales zeolíticos. Por lo tanto, dependiendo del uso que se le vaya a dar a la zeolita, el químico y el físico están en condiciones de proponer una zeolita adecuada, ya sea modificando las propiedades de las existentes, ya sea creando nuevas.
Estos trabajos, de gran repercusión tecnológica como veremos más adelante fueron,
de hecho, la prolongación lógica de líneas de investigación a largo término
tan académicas como la misma síntesis de cristales.
| GLOSARIO DEL CAPÍTULO II |
solución. Mezcla de dos sustancias, una de las cuales se disuelve en la otra; la sustancia disuelta se llama soluto y la otra solvente.
difracción de rayos X. Técnica utilizada para obtener información sobre la estructura y la composición de los materiales cristalinos.
gel. Sustancia obtenida al flocular una solución coloidal.
reacción química. Cambio en una sustancia o sustancias que produce otras con propiedades químicas diferentes.
polimerización. Unión de varias moléculas de un compuesto para formar grandes moléculas.
polímero. Se dice de una molécula cuya masa molecular es un múltiplo de la otra denominada monómero.
peso molecular. El peso molecular relativo de un compuesto es el peso de una molécula de ese compuesto en relación con el peso de un átomo de oxígeno, al cual, por convención, se le ha asignado el peso de 16.000 unidades de masa atómica.
promotor. Sustancia que, incorporada en pequeña cantidad a un catalizador, aumenta notablemente su actividad.
caolín. Silicato de aluminio puro proveniente de alteraciones de los feldespatos, los granitos, las arcillas blancas; es refractario.
base. Véase ácido y base en el glosario del Capítulo 1.
amina. Nombre químico de los compuestos que se obtienen sustituyendo el hidrógeno del amonio con radicales hidrocarbonados univalentes.