III. CRISTALES LÍQUIDOS
CON toda razón le habrá parecido contradictorio el título de este capítulo. En efecto, por una parte llamamos líquido a una sustancia que fluye y toma la forma del recipiente que la contiene; pero, por otra, a un cristal lo concebimos como sustancia sólida y rígida. De modo que, al menos intuitivamente, ¡un cristal es precisamente lo opuesto a un líquido! Y sin embargo existen sustancias reales, los cristales líquidos, que exhiben la dualidad sólido-líquido, es decir, que, simultáneamente, poseen propiedades de los líquidos, fluidez y viscosidad, y propiedades ópticas que se parecen de modo asombroso a las de los cristales como, por ejemplo, poder reflejar colores diferentes dependiendo del ángulo bajo el cual se les observe.
En los últimos treinta años se ha descubierto que estas sustancias ocupan un
lugar único en la naturaleza. Así, se sabe que los cristales líquidos desempeñan
un papel fundamental en los organismos vivos, pues el DNA forma diversas fases
líquido cristalinas; también se les utiliza para fabricar dispositivos electrónicos,
como los indicadores electro-ópticos que muestran letras y símbolos diversos
en las calculadoras de bolsillo o en las carátulas de los relojes electrónicos
modernos (Figura 20).

Figura 20. Indicador numérico electro-óptico fabricado con cristales líquidos.
También han permitido fabricar pantallas de TV extraordinariamente delgadas
y hacen posible el desarrollo de ventanas o cortinas que con sólo accionar un
interruptor se hacen transparentes o totalmente opacas (Figura 21).
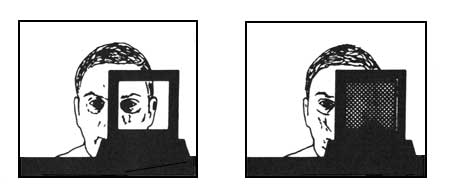
Figura 21. Ventana de cristal líquido con transparencia controlable.
Estos líquidos tan peculiares son también esenciales para fabricar nuevos materiales, entre ellos fibras de muy alta resistencia y son de gran utilidad en la recuperación del petróleo. Y la lista de las aplicaciones de estos líquidos exóticos continúa creciendo sin cesar... Pero antes de examinar con más detalle cuáles son las propiedades de los cristales líquidos que hacen posible estas aplicaciones, hagamos un poco de historia.
Los cristales líquidos fueron descubiertos hace más de cien años (1888) por el botánico austriaco F. Reinitzer, quien encontró que algunos compuestos orgánicos derivados del colesterol parecían tener dos puntos de fusión. Más específicamente, observó que al calentar los cristales de estas sustancias a 145° C, el sólido se transformaba en un líquido turbio; pero éste a su vez, se convertía en un líquido totalmente claro y transparente precisamente a 179° C. Reinitzer también realizó el proceso inverso y enfrió el líquido transparente observando que exactamente a las mismas temperaturas anteriores ocurrían las transformaciones opuestas. Como además los cambios observados iban acompañados de absorción o emisión de calor, dependiendo de si la temperatura aumentaba o disminuía y, asimismo, como el volumen del sistema cambiaba en forma abrupta, Reinitzer concluyó que la sustancia en realidad exhibía dos cambios o transiciones de fase sucesivas. Al poco tiempo de estas primeras observaciones (1889), el cristalógrafo alemán F. Lehmann descubrió que el líquido turbio intermedio entre los cristales y el líquido transparente poseía propiedades ópticas y una estructura molecular muy parecida a la de un cristal sólido, y acuñó el nombre de cristal líquido. Aun sin darse plena cuenta, lo que en realidad habían descubierto era un nuevo estado de la materia: las fases intermedias o mesofases.
Sin embargo, a pesar de que inicialmente los cristales líquidos despertaron gran interés y fueron muy estudiados durante el primer tercio de este siglo, pronto fueron relegados a un rincón de la física y cayeron rápidamente en el olvido subsistiendo sólo como curiosidad de laboratorio. Diversos factores contribuyeron a esta pérdida de interés, uno de ellos fue el prejuicio, fuertemente arraigado en el hombre desde la remota antigüedad, según el cual las tres nociones: gas, líquido y sólido describen todas las posibles fases de la materia. Esta actitud, aún no superada en los años treinta de este siglo, conlleva naturalmente un rechazo a la dualidad sólido-líquido exhibida por los cristales líquidos. En consecuencia no es de extrañar que la aparente ambigüedad en el punto de fusión descubierta por Reinitzer se atribuyera únicamente a la presencia de "impurezas" en el sistema bajo estudio.
Otro factor preponderante fue el gran desarrollo logrado en el segundo tercio de este siglo en otros campos de la ciencia como la física de semiconductores, la química de polímeros, la física atómica o el espectacular desarrollo de la electrónica. Todos estos avances y la entonces falta de aplicaciones prácticas de los cristales líquidos, frenaron y eclipsaron su desarrollo. Pero, paradójicamente, los mismos avances y, de manera especial el proceso de miniaturización de los dispositivos electrónicos, produjeron el renacimiento y auge que los cristales líquidos tienen en nuestros días. En efecto, en este afán de miniaturización la electrónica pasó de los bulbos a los transistores, después a los microcircuitos y finalmente a los circuitos integrados actuales.
Este proceso tuvo como consecuencia importantísima la disminución de las potencias consumidas y, por tanto, la reducción de las fuentes de alimentación energética en aparatos e indicadores electrónicos. Sin embargo, ocurrió algo muy lógico pero que no se había anticipado: al reducir tanto las dimensiones de los dispositivos electrónicos ¡casi se perdió la comunicación con ellos mismos! Cada vez era más difícil transmitir —a bajo costo— la información al hombre, pues los diodos semiconductores emisores de luz consumen grandes corrientes eléctricas y los cinescopios de televisión son demasiado grandes. Faltaba, pues, un puente de comunicación entre lo muy pequeño y el mundo macroscópico. Es entonces, a principios de los años sesenta, cuando los cristales líquidos son recordados y comienza su resurgimiento hasta convertirse en uno de los campos más activos en la investigación científica interdisciplinaria con enormes posibilidades de aplicación tecnológicas.
Pero, se preguntará el lector, ¿qué propiedades físicas son las que hacen tan especiales a los cristales líquidos? y, sobre todo, ¿es posible entender estas propiedades en términos de las nociones más familiares o intuitivas que tenemos de los líquidos ordinarios o los cristales? Para contestar estas preguntas es necesario examinar brevemente las características de la estructura e interacción de las moléculas de un cristal líquido.
Un cristal líquido fluye, se escurre y toma la forma del recipiente que lo contiene, de la misma manera que lo hace un líquido ordinario como, por ejemplo, el agua. Pero a diferencia de ésta, cuyas moléculas son relativamente simples y prácticamente esféricas, las moléculas de un cristal líquido son, por lo general, o muy alargadas en forma de barra o aplanadas en forma de disco (Figura 22).
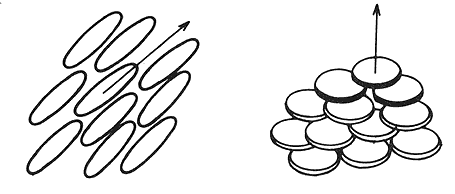
Figura 22. Las moléculas de cristal líquido tienen forma de barras o discos.
Esta asimetría molecular tiene una consecuencia muy importante, los átomos dentro de la molécula se sitúan preferentemente a lo largo del eje de la molécula o bien en el plano definido por la molécula misma, dando lugar a una estructura molecular complicada, según se ilustra en la figura 23.
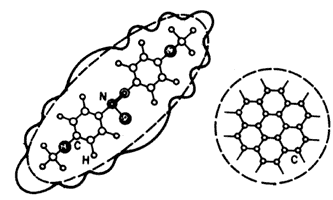
Figura 23. Nubes electrónicas: los enlaces entre los átomos producen una distribución de carga complicada en las moléculas.
Ahora bien, recordemos que cada átomo consta de un núcleo con carga eléctrica positiva rodeado por una nube de electrones con carga eléctrica negativa que compensa exactamente la del núcleo, de manera que los átomos, y por tanto las moléculas, son eléctricamente neutros. Esta disposición de los núcleos y nubes electrónicas produce una distribución de carga bastante compleja dentro de la molécula (Figura 24).
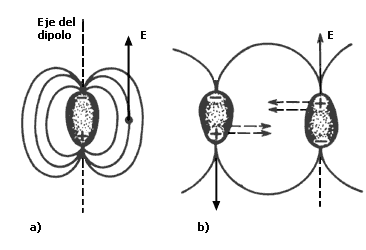
Figura 24. (a) Líneas de fuerza del campo eléctrico de un dipolo, (b) fuerzas de atracción entre dipolos.
Pero esta configuración no es estática, sino que cambia cuando dos moléculas se acercan entre sí. En efecto, cuando esto ocurre, las nubes electrónicas son las primeras en entrar en contacto y se repelen por tener cargas del mismo signo, de modo que a distancias comparables con las dimensiones moleculares mismas, las fuerzas intermoleculares son repulsivas y tienden a alejar a las nubes electrónicas y en consecuencia a las moléculas. Pero esta repulsión también produce el desplazamiento relativo de las nubes electrónicas con respecto a sus núcleos. Como esto ocurre en cada átomo, en las moléculas alargadas el efecto neto podemos describirlo imaginando que la presencia de una molécula de cristal líquido produce una distorsión en la distribución de carga eléctrica de la otra molécula, de modo que la carga positiva neta de los núcleos queda separada una cierta distancia de una carga negativa de igual magnitud. Como es sabido, a esta configuración de carga se le llama un dipolo eléctrico y a la línea que une ambas cargas se le llama eje del dipolo, que coincide entonces con el eje largo de la molécula. Así que podemos concluir que una molécula de cristal líquido induce la formación de dipolos eléctricos en las moléculas vecinas. Debe señalarse, sin embargo, que es más fácil que la nube electrónica se desplace con respecto al núcleo positivo a lo largo del eje de la molécula que transversalmente a él —a lo largo del eje corto— aunque esto último también es posible dependiendo de la estructura molecular. Ahora debemos averiguar a qué conduce esta formación de dipolos en todo el cristal líquido.
Sabemos que cada configuración de cargas eléctricas crea un campo eléctrico E en el espacio que la rodea. La estructura espacial específica de cada campo, es decir, cómo varia su magnitud con la posición y cuál es su dirección en cada punto, es una propiedad de cada configuración de carga, pero es precisamente a través de este campo como cada configuración ejerce fuerzas sobre otras cargas eléctricas. En el caso del dipolo eléctrico la estructura de este campo está representada por las líneas de fuerza que se muestran en la figura 24 (a) y sus propiedades son tales que, si en la región ocupada por este campo se coloca otro dipolo, las fuerzas que el campo del primero produce fuerza a que los dipolos se orienten como se muestra en la figura 24 (b). Es decir, la mayor parte de los átomos de una molécula trata de situarse al lado de los átomos de otra, de modo que las cargas del mismo signo se sitúen lo más cerca unas de otras. El resultado neto es que así se genera una fuerza atractiva entre los dipolos. Entonces, cuando dos moléculas de un cristal líquido se encuentran separadas a distancias mayores que sus dimensiones, las moléculas se atraen. Es claro que de acuerdo con este modelo simplificado de la interacción entre moléculas se sigue que debe existir una distancia entre ellas para la cual las fuerzas atractivas y repulsivas se equilibren y, en consecuencia, la configuración relativa de las moléculas sea la más estable y la más favorable desde el punto de vista energético. Por lo tanto es de esperarse que las moléculas de cristal líquido tiendan a adoptar esta configuración manteniendo sus ejes dipolares o planos característicos paralelos entre sí. Concluimos entonces que, debido a la estructura de sus moléculas y en especial debido a la asimetría de las mismas, un cristal líquido adopta configuraciones altamente ordenadas. Aunque el mecanismo de interacción molecular que hemos descrito es básicamente el mismo que genera el orden en los cristales sólidos. No debe olvidarse una diferencia esencial entre ambos sistemas: en todo momento los cristales líquidos permanecen en estado líquido, lo cual implica que los centros de masa de sus moléculas no forman una red periódica sino que fluyen manteniendo el orden en la orientación común de sus ejes moleculares.
De acuerdo con el tipo de arreglos moleculares que pueden formar, Friedel (1922) clasificó los cristales líquidos en tres grandes clases: nemáticos, esmécticos y colestéricos. La fase nemática exhibe orden en la orientación de sus moléculas y al mismo tiempo desorden en la posición de sus centros de masa. Las moléculas pueden moverse lateralmente, girar alrededor del eje común o deslizarse paralelamente a él (Figura 25).
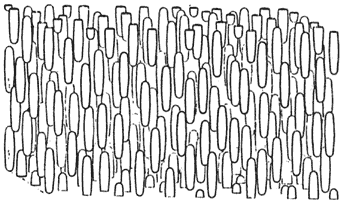
Figura 25. La fase nemática exhibe orden de orientación, pero desorden en la posición de los centros de masa moleculares.
Podríamos comparar este arreglo molecular con el de los cerillos dentro de una caja: aunque pueden moverse, la presencia de los demás impone restricciones a estos movimientos y tiende a mantenerlos paralelos entre sí. De este modo, respecto a la posición de sus centros de masa, un nemático se comporta como un líquido ordinario y sus moléculas se mueven caóticamente. En cambio difiere totalmente de un líquido ordinario en que sus moléculas se orientan y al moverse mantienen sus ejes paralelos a una dirección común. Es preciso señalar que, por supuesto, este orden nunca es perfecto, sólo ocurre a temperaturas moderadas cuando las variaciones térmicas no son tan intensas como para destruir totalmente este orden de orientación. Recordemos que ya desde las primeras observaciones de Reinitzer sabemos que al calentar un cristal líquido éste se convierte en un líquido ordinario. También es importante mencionar que, además de la temperatura, otras propiedades, como la densidad, son de gran importancia para determinar el grado de orden o el tipo de fase líquido cristalina que puede formarse. En efecto, cuando el número de moléculas por unidad de volumen es elevado, o sea, cuando la densidad es grande, las moléculas están más cerca unas de otras y las interacciones repulsivas entre ellas son más intensas, lo cual favorece la aparición de orden tanto de orientación como de posición en el cristal líquido. Sin embargo, estas fluctuaciones térmicas producen defectos en la orientación los cuales dan lugar a estructuras microscópicas en forma de hilo que flotan en el nemático o que se adhieren a la superficie del recipiente. Precisamente esta característica fue el origen del nombre nemático que en griego significa hilo.
En contraste con los nemáticos, que son la fase más desordenada de los cristales líquidos, los esmécticos constituyen la fase más ordenada. Tienden a organizarse en capas planas paralelas entre sí, como las hojas de un libro pero con sus ejes moleculares perpendiculares a estos planos y paralelos entre sí. Éste es, por ejemplo, el arreglo de las moléculas en las capas superficiales de una pompa de jabón y es el que le proporciona la cohesión necesaria para formarse. De hecho, esméctico se deriva del vocablo griego que designa una sustancia de propiedades similares al jabón. Como en los nemáticos, las moléculas de esméctico también pueden girar alrededor de la dirección de orientación común pero no pueden hacerlo fuera de la capa en que se encuentran. En cada plano las moléculas pueden acomodarse en filas con diferentes grados de orden de posición de sus centros de masa. En el caso más ordenado se produce un arreglo regular muy parecido al de la red de un sólido, en el que hay orden y repetición en cada dirección (Figura 26).
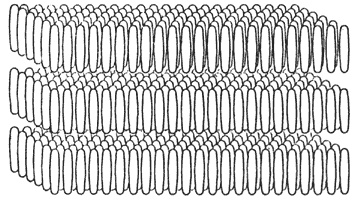
Figura 26. Cristal líquido esméctico con orden de orientación de los ejes moleculares y orden en la posición de sus centros de masa.
En cambio, en el arreglo más desordenado los centros de masa moleculares se mueven caóticamente en cada plano, de modo que en este caso el esméctico es nemático por planos (Figura 27). Debe enfatizarse, sin embargo, que en cualquier caso el esméctico es siempre fluido y las diferentes capas se deslizan, en mayor o menor grado, unas sobre otras.

Figura 27. Capas de esméctico en las que no existe orden de posición. Se comportan como nemáticas en cada plano.
La tercera clase de cristales líquidos posee una estructura molecular característica de muchos compuestos que contienen colesterol y por esta razón se le llama colestérica. Como en los esmécticos, las moléculas de colestérico también pueden acomodarse en capas superpuestas, pero con una diferencia crucial: los ejes moleculares se orientan en una dirección paralela al plano mismo de las capas. Más aún, esta dirección cambia ligeramente de capa a capa debido a la peculiar estructura molecular de los colestéricos, y en consecuencia el eje de orientación, al pasar de un plano a otro, describe una trayectoria en forma de hélice, como se indica en la figura 28.
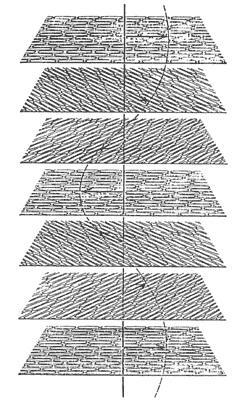
Figura 28. La dirección de orientación molecular en cada plano de colestérico describe una trayectoria helicoidal (línea discontinua).
Hemos visto cómo la arquitectura molecular de los cristales líquidos favorece, a temperaturas y densidades moderadas, la aparición de una dirección especial a lo largo de la cual se orientan las moléculas alargadas y perpendicularmente a ella en las moléculas en forma de disco. La peculiaridad de este tipo de materiales es que la existencia de una dirección preferida afecta el comportamiento de los rayos luminosos en el material cambiando su intensidad, color y dirección de propagación. Por esta razón a esta dirección especial se le llama el eje óptico del material y es la causa de muchos fenómenos ópticos importantes. Es necesario subrayar aquí que la existencia del eje óptico es un fenómeno colectivo que se da en forma espontánea en los cristales líquidos. Así, por ejemplo, si un rayo de luz blanca incide sobre el cristal líquido formando un ángulo con el eje óptico puede transformarse en luz de color al transmitirse a través del líquido pues la velocidad de la luz en el fluido depende de la dirección de propagación respecto al eje óptico. Pero, además de este cambio en el color, también puede ocurrir que el rayo saliente se divida en dos rayos luminosos cuyas intensidades relativas varíen dependiendo de la dirección del rayo incidente con el eje óptico. A este fenómeno se le llama birrefringencia.
Por otra parte, es bien conocido que los cristales sólidos con ejes ópticos
se usan en múltiples aplicaciones tecnológicas en las que es necesario dirigir
los rayos luminosos en forma rápida y precisa. Una aplicación muy conocida es
la de los polaroides o polarizadores, que sólo transmiten algunos de los rayos
luminosos que inciden sobre ellos y que se usan ampliamente en la fotografía
en colores o para fabricar lentes que protejan los ojos de la luz deslumbradora
del Sol. Para entender mejor la función de un polarizador recordemos que cada
onda electromagnética emitida por un sistema particular de cargas en movimiento,
consta de un campo eléctrico E y un campo magnético H que oscilan transversalmente
a la dirección de propagación de la onda (Figura 29). Aunque en cada onda el
campo eléctrico está orientado de modo preciso, en un rayo de luz compuesto
de muchas ondas emitidas por diferentes sistemas de cargas a diferentes tiempos,
no hay en general una dirección —"polarización"— bien determinada del
campo eléctrico total. Cuando esto ocurre se dice que la luz es natural o no
polarizada.
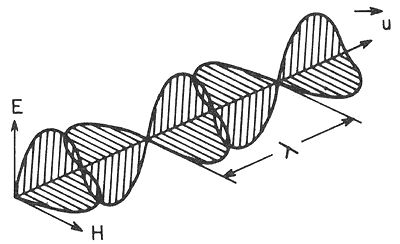
Figura 29. Onda electromagnética propagándose en la dirección de u. l es la longitud de onda.
Los polarizadores permiten, precisamente, convertir la luz natural en polarizada al eliminar del rayo de luz todas aquellas ondas cuya polarización no sea la requerida. Ya que los cristales líquidos poseen eje óptico no es de extrañar que también exhiban muchos de estos fenómenos, los cuales son totalmente insólitos en los líquidos ordinarios. Sin embargo, a diferencia de los cristales sólidos los cristales líquidos presentan una ventaja enorme: debido a la relativa debilidad de las fuerzas de interacción molecular, la orientación del eje óptico se puede variar con mayor facilidad. Existen diversos métodos para "manejar" el eje óptico de un cristal líquido, todos ellos basados en la enorme capacidad de estos sistemas para responder a la acción de campos externos.
El primer fenómeno en el que se observó que el eje óptico cambia de dirección bajo la acción de un campo eléctrico es el ahora llamado efecto Freederiks (1943), descubierto por el físico ruso del mismo nombre. Este fenómeno se observa con mayor facilidad en un nemático y, como veremos, constituye la base física del funcionamiento de los indicadores electro-ópticos de las carátulas de relojes y calculadoras electrónicas modernas. Si un campo eléctrico externo actúa sobre un nemático, interacciona con los dipolos de sus moléculas y las hace girar de manera tal que su eje largo tiende a colocarse paralelamente al campo aplicado o en dirección perpendicular a él, dependiendo de que el momento dipolar de la molécula esté dirigido en la dirección de su eje largo o corto, respectivamente. Pero ya hemos visto que en un nemático todas las moléculas mantienen una misma orientación debido a las características de su interacción mutua; así que si una molécula de nemático se reorienta bajo la acción de un campo externo, las demás se reorientan también en la misma dirección. Por lo tanto, basta con aplicar un campo eléctrico pequeño para producir una reorientación de todo el eje óptico del nemático.
Un indicador electro-óptico consta básicamente de una celda diminuta con los siguientes elementos: una capa muy delgada (0.01-0.1 mm) de cristal líquido, por lo general un nemático, colocado entre dos placas de vidrio cada una de las cuales está unida a un polarizador. Estas placas se pulen de manera tal que la cohesión entre las moléculas y las placas sólidas sea máxima, lo cual se logra produciendo surcos en las placas de aproximadamente las dimensiones de una molécula de nemático. Así se consigue que las moléculas que están en contacto con las placas se alineen con la dirección de pulimento y, por las características de las interacciones moleculares, todas las moléculas en el espesor de la capa se alinean exactamente en la misma dirección. Si bajo estas condiciones una placa se gira noventa grados respecto a la otra —debido a que a grandes distancias de las placas el influjo del vidrio sobre las moléculas de nemático es menor que cerca de las superficies sólidas— las moléculas, y por lo tanto el eje óptico del cristal líquido, se reorientan adquiriendo la configuración torcida que se muestra en la figura 30.
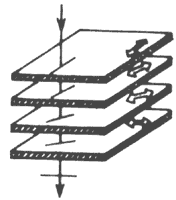
Figura 30. Geometría torcida producida al girar las placas de vidrio 90°.
Si entonces se ilumina la celda con luz natural, ésta se polariza y al penetrar en la celda su polarización sigue la configuración torcida del eje óptico, de modo que al salir por la placa inferior también habrá girado noventa grados. Pero como el eje del polarizador inferior tiene precisamente esa dirección, la luz atravesará el segundo polarizador. Entonces, si debajo del polarizador inferior se coloca un espejo, la luz podrá reflejarse nuevamente al interior de la celda, atravesarla en sentido inverso y salir de ella hasta llegar a los ojos de un observador que verá a la celda perfectamente clara y transparente. Este proceso se ilustra en la parte izquierda de la figura 31.
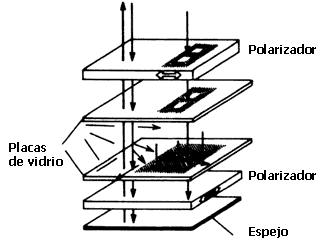
Figura 31. Elementos de una celda de un indicador electro-óptico.
Para poder formar cualquier cifra, letra o palabra en el indicador, es preciso colocar dos electrodos entre las placas de vidrio de manera que, al conectarlos a una pila, se produzca un campo eléctrico en el nemático. Al efecto, el electrodo inferior se construye de una sola pieza, mientras que el superior consta de muchos electrodos más pequeños. Así, por ejemplo, para formar cualquier cifra entre cero y nueve sólo se requieren siete segmentos, cada uno de los cuales puede conectarse o desconectarse a un circuito eléctrico de acuerdo a las señales que produzca un generador diminuto cuyo funcionamiento lo controla un programa especial. De esta manera es posible producir un campo eléctrico únicamente sobre ciertas regiones de la celda. En la parte derecha de la figura 31 se ilustra la situación en que ha sido cerrado el circuito de manera que los segmentos del electrodo superior que conforman el número ocho se activen. De acuerdo con el efecto Freederiks, el campo eléctrico en esta región de la celda tiende a alinear las moléculas destruyendo la configuración torcida que prevalecía en ausencia de campo. Entonces, la luz polarizada que sale del primer polarizador se transmite, por debajo de los segmentos de electrodo asociados a la cifra ocho, por toda la capa de nemático sin cambiar su polarización. Pero al llegar al segundo polarizador, cuya dirección de polarización es perpendicular a la polarización de la luz, no podrá atravesarlo y entonces o se absorbe en el líquido o se desvía en cualquiera otra dirección. Como esta luz no llega al espejo, tampoco alcanzará al observador y éste verá oscuros los segmentos de la cifra ocho. El resultado final será que el observador verá un ocho oscuro sobre un fondo claro (Figura 32).
Figura 32. Imagen típica de un indicador digital electro-óptico.
Éste es el principio físico del funcionamiento de la gran mayoría de los indicadores digitales usados en calculadoras de bolsillo, videograbadoras, tableros de diversos aparatos medidores o cuadrantes de sintonía. Es importante señalar que los procesos comprendidos en los dispositivos que acabamos de describir, ocurren rápidamente, por lo común en una diezmilésima o cienmilésima de segundo; así, en una fracción pequeña de tiempo se puede mostrar en la pantalla toda una sucesión de cifras o símbolos diversos. Más aún, como las dimensiones de la celda son tan pequeñas, los problemas usuales asociados con el manejo de los líquidos no se presentan y las potencias consumidas en los circuitos de la misma son muy pequeños; por ejemplo, una pila de 1.5 voltios basta para generar toda la energía requerida.
En las páginas anteriores hemos presentado un esbozo de cómo son los cristales líquidos; resulta evidente que es éste un campo interdisciplinario de gran importancia, tanto científica como tecnológica. Podemos mencionar que actualmente ya están a la venta televisores miniatura a colores, con pantallas de gran definición, fabricados con cristales líquidos. A juzgar por los logros y aplicaciones espectaculares de los cristales líquidos obtenidos en los últimos años, no cabe duda que el futuro nos deparará sorpresas cada vez mayores y, al mismo tiempo, nos brindará nuevos retos para comprender las extraordinarias propiedades de estas fases intermedias de la materia.