II. LA ELECTRICIDAD HASTA EL AÑO 1800
DESDE tiempos inmemoriales el hombre se dio cuenta de que después de frotar con paño un tipo de resina llamada ámbar, ésta adquiría la capacidad de atraer algunos objetos ligeros, como trozos de papel. La historia registra a Tales de Mileto, filósofo y matemático griego, que vivió hace unos 2 600 años, como el primero que hizo experimentos de esta naturaleza, aunque es bastante probable que desde antes se conociese este tipo de fenómeno. En griego, ámbar se dice elektron y de esta palabra se deriva electricidad. Durante muchos siglos este tipo de experiencias no fueron sino meras curiosidades.
Hacia principios del siglo XVIII se inició la investigación detallada de los fenómenos eléctricos. Entre 1729 y 1736 dos científicos ingleses, Stephen Gray (1696-1736) y Jean Desaguliers (1683-1744) dieron a conocer los resultados de una serie de experimentos eléctricos muy cuidadosos. Encontraron que si unían por medio de un alambre metálico un tubo de vidrio previamente frotado con un trozo de corcho, éste se electrificaba. Comprobaron que el corcho se electrificaba ya que al acercarle trozos de papel éstos eran atraídos por él. Este fenómeno persistía aun si el vidrio y el corcho se separaban a distancias de 300 metros. Si en lugar de efectuar la unión con un alambre metálico empleaban un hilo de seda, el corcho no se electrificaba. Además descubrieron que si la línea de transmisión hacía contacto con el suelo, o sea con la tierra, el corcho dejaba de electrificarse.
Con todos estos experimentos llegaron a la conclusión de que la electrificación era un efecto que se presentaba en la superficie de los cuerpos, en donde aparecía lo que llamaron una "virtud" o "fluido" eléctrico al que en la actualidad se le llama carga eléctrica. Encontraron que la carga eléctrica podía moverse libremente de un cuerpo a otro a través de ciertos materiales que llamaron conductores (el cuerpo humano, los metales, el aire húmedo, etc.). También existen materiales que no conducen electricidad, a los que se llama aisladores o no-conductores (la madera, la seda, la cerámica, etcétera).
Un científico francés, François du Fay (1698-1739), hizo otro tipo de experimentos que reportó entre 1733 y 1734. Frotó con tela de seda dos tubos de vidrio iguales. Al acercar los tubos vio que siempre se repelían. Así concluyó que dos materiales idénticos se repelan cuando se electrifican en formas idénticas. Como cada uno de los tubos adquiere el mismo tipo de carga se puede afirmar que cargas iguales se repelen.
El mismo François du Fay hizo muchos otros experimentos con diferentes materiales y llegó a la conclusión de que existen dos tipos de electricidad; a una la llamó vitrosa (la que aparece cuando se frota con seda el vidrio) y a la otra resinosa (la que aparece cuando se frota al hule con piel).
Durante la siguiente década, Benjamín Franklin (1706-1790)) realizó estos mismos descubrimientos en Estados Unidos, sin conocer los trabajos del francés. Según él, el vidrio electrificado había adquirido un exceso de fluido (carga) eléctrico, y le llamó a este estado positivo. Al estado de la seda con la que frotó el vidrio lo llamó negativo, pues consideraba que había tenido una deficiencia de fluido (carga) eléctrico. Esta terminología de Franklin es la que se utiliza hasta hoy en día, aunque no se acepten las ideas con que la concibió este científico.
En resumen, existen en la naturaleza dos tipos de cargas eléctricas: positiva y negativa. Además, se puede concluir de una multitud de resultados experimentales que dos cargas eléctricas del mismo tipo (negativa-negativa o positiva-positiva) se repelen, mientras que dos cargas de tipos distintos (positiva-negativa) se atraen.
No fue sino hasta fines del siglo XVIII, en 1785, que el ingeniero
militar francés Charles Auguste Coulomb (l736-1806) pudo medir con bastante
precisión las características de las fuerzas entre partículas eléctricamente
cargadas. Para ello utilizó un péndulo de torsión (Figura 1) que consiste en
una barra AB que está sujeta por medio de un alambre vertical. Cuando
uno de los extremos experimenta una fuerza, la barra gira y hace que el alambre
se tuerza. Midiendo el ángulo que gira el alambre se puede determinar la magnitud
de la fuerza que experimentó el extremo de la barra. Coulomb colocó en el extremo
A de su péndulo una carga y acercó otra carga C. Cambiando los
valores de las cargas y manteniendo la distancia entre A y C fija,
encontró que mientras más grande es cada una de las cargas, mayor es la magnitud
de la fuerza entre ellas (ya sea de atracción si las cargas son opuestas, o
de repulsión si son iguales). De hecho, si una de las cargas aumenta al doble,
la fuerza aumenta al doble, si la carga aumenta al triple, la fuerza aumenta
al triple y así sucesivamente. Además, mientras más separadas estén las cargas,
menor será la fuerza. Así si la distancia entre A y C aumenta
al doble, la fuerza disminuye a la cuarta parte; si la distancia aumenta al
triple, la fuerza disminuye a la novena parte, etc. Este conjunto de resultados
recibe el nombre de ley de Coulomb.
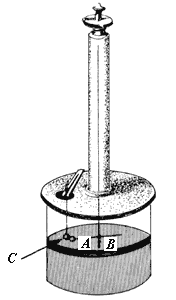
Figura 1. Aparato diseñado por Coulomb para medir la fuerza entre cargas eléctricas.
Regresemos al año de 1663, cuando Otto von Guericke (1602-1686) de Magdeburgo, Alemania, construyó el primer generador de electricidad. Este aparato producía cargas eléctricas por medio de fricción. Sobre un armazón de madera Von Guericke montó una esfera de azufre sobre un eje. Mientras con una mano hacía girar la esfera, con la otra la presionaba. Así obtenía cargas eléctricas sobre la esfera, que atraían diversos objetos cercanos. El funcionamiento de esta máquina estaba basado en el experimento arriba descrito en que se frotaba una sustancia con otra. El famoso científico inglés Isaac Newton (1642-1727) propuso usar una esfera de vidrio en lugar de una de azufre. Al transcurrir los años se diseñaron diferentes variantes, gracias a lo cual se construyeron máquinas cada vez con mayor capacidad de producir carga eléctrica.
Así, en las primeras décadas del siglo XVIII ya existían máquinas que producían cargas eléctricas por medio de fricción. Funcionaban esencialmente a base de discos que se hacían girar por medio de manivelas. Al girar se friccionaban con otra superficie y se cargaban, de la misma forma en que un trozo de vidrio se carga al frotarlo con un paño. Estas máquinas producían cantidades respetables de carga eléctrica y al acercarlas a otras superficies se producían chispas. Era muy frecuente encontrar estas máquinas en salones de juegos, pues hacían que los cabellos de las señoras se pusieran de punta al ser atraídos por las cargas generadas.
Hacia 1746 Pieter van Musschenbroek, en Leiden, Holanda, construyó el primer dispositivo para almacenar cargas eléctricas. Se trataba de una botella de vidrio que estaba recubierta, tanto en sus paredes interiores como exteriores, de una capa muy delgada de estaño. En esta famosa botella de Leiden se pudieron almacenar considerables cantidades de carga eléctrica, producidas por las máquinas de fricción. Posteriormente se diseñaron otros dispositivos más prácticos y cómodos para almacenar carga eléctrica, a los cuales se llamó condensadores.
Hacia mediados del siglo XVIII, mientras efectuaba algunos experimentos, Benjamín Franklin se dio cuenta de que durante las tormentas había efectos eléctricos en la atmósfera, y descubrió que los rayos eran descargas eléctricas que partían de las nubes. Franklin logró juntar cargas eléctricas de la atmósfera por medio de varillas muy picudas. A la larga, esto dio lugar a la invención del pararrayos, que consistía en una varilla metálica picuda conectada a la tierra; las cargas eléctricas del rayo eran atraídas a la varilla y conducidas a la tierra. Con esto se evitaba que un rayo cayera sobre una casa, pues era conducido a tierra sin causar ningún daño. Posiblemente ésta fue la primera aplicación práctica de la investigación científica de la electricidad.
Por otro lado, hacia la última parte del siglo XVIII un gran número
de personas empleó animales para estudiar las descargas eléctricas y utilizó
como fuentes máquinas generadoras y botellas de Leiden. Una de estas personas
fue Luigi Galvani (1737-1798), profesor de anatomía en la Universidad de Bolonia,
Italia. Sus discípulos se dieron cuenta de que cuando se sacaban chispas de
un generador y se tocaban simultáneamente las patas de una rana con un bisturí,
éstas se contraían. Galvani estudió con más detalle este curioso fenómeno. En
primer lugar, unió una extremidad de la rana a un pararrayos y la otra la fijó
a tierra por medio de un alambre metálico. Descubrió que los músculos se estremecían
cuando había tormenta, pues las cargas que recogía el pararrayos se transportaban
a través del músculo hasta la tierra. La conexión la realizó de la siguiente
manera: en un extremo de la pata conectó un alambre de cobre, mientras que en
el otro extremo conectó uno de hierro (Figura 2). En cierto momento, y de manera
accidental, juntó los alambres y se dio cuenta de que la pata se contraía. De
sus experiencias anteriores sabía que esta contracción ocurría solamente cuando
una carga eléctrica pasaba por la pata, pero ¡no había conectado ningún extremo
a ninguna fuente de carga eléctrica! Así llegó a la conclusión de que si se
formaba un circuito cerrado entre dos metales que pasara por la pata, se generaba
una corriente eléctrica que circulaba por el circuito. Sin embargo, Galvani
no estaba en lo cierto, ya que creyó que la fuente de la electricidad estaba
en lo que llamó "electricidad animal". Galvani se dedicó a hacer experimentos
con diferentes animales creyendo que había descubierto y confirmado la veracidad
de la electricidad animal. Con el tiempo se comprobó que sus hipótesis no eran
correctas.
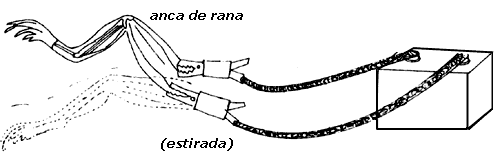
Figura 2. Si los metales hierro y cobre se unen, el anca de la rana se contrae debido al paso de una corriente eléctrica.
Alejandro Volta (1745-1827), profesor de la Universidad de Pavia, Italia, se enteró de los experimentos de Galvani y los volvió a hacer, usando lo que llamó ranas "galvanizadas". Sin embargo, no aceptó la explicación de Galvani. Volta se dio cuenta de que para lograr el efecto descubierto por Galvani se necesitaba cobre, hierro y el líquido del tejido muscular. Hizo una serie de experimentos muy cuidadosos, utilizando alambres de diferentes materiales; así descubrió que si usaba estaño y cobre lograba una corriente relativamente fuerte, mientras que si usaba hierro y plata el efecto era poco intenso. Siguiendo esta línea de pensamiento dejó de usar ranas y puso su propia lengua entre los metales, logrando el mismo efecto; en seguida probó con diferentes líquidos entre los metales y siempre encontró el mismo efecto. El caso más satisfactorio fue cuando usó placas de zinc y cobre en un ácido líquido (Figura 3). De esta manera llegó a la conclusión de que el efecto descubierto por Galvani no tenía nada que ver con la "electricidad animal" sino que se debía a una acción química entre el líquido, llamado electrolito, y los dos metales. Es así como Volta construyó lo que posteriormente se llamó una pila voltaica, que fue el primer dispositivo electroquímico que sirvió como fuente de electricidad.
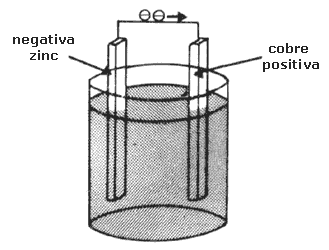
Figura 3. Esquema de una de las primeras baterías eléctricas de Volta.
Entre los extremos de los metales, fuera del electrolito, se genera una diferencia de potencial, o voltaje, que puede dar lugar a una corriente eléctrica. En la pila de la figura 3 el zinc adquiere carga negativa, mientras que el cobre adquiere cargas positivas. Al zinc se le llama cátodo y el cobre recibe el nombre de ánodo. Así se tiene una fuente de electricidad distinta a la generada por fricción. Con este medio químico para obtener electricidad se abrieron nuevas posibilidades de aplicación práctica y experimental.
La explicación de las reacciones químicas que ocurren en la pila o celda voltaica se dio muchos años después, ya que en la época de Volta la química apenas empezaba a desarrollarse como ciencia moderna. Solamente diremos que, por un lado, el zinc adquiere un exceso de electrones, mientras que por el otro, el ácido con el cobre da lugar a cargas eléctricas positivas. Al unir el cobre con el zinc por medio de un alambre conductor, los electrones del zinc se mueven a través del alambre, atraídos por las cargas del cobre y al llegar a ellas se les unen formando hidrógeno.
Desde entonces se han construido diferentes tipos de pilas o baterías. Un avance importante fue la pila con el electrolito sólido, o sea, la llamada pila seca, como las que usamos hoy en día en los aparatos eléctricos portátiles.
El descubrimiento de Volta se expandió como reguero de pólvora. Muy pronto en muchos países europeos se construyeron pilas voltaicas de diferentes tipos, que fueron un acicate para los estudios de las propiedades y efectos electroquímicos, térmicos, magnéticos, etc., de la electricidad.
Volta recibió en vida muchos premios y agasajos. En 1881 el Congreso Internacional de Electricistas decidió honrarlo dando su nombre a la unidad de diferencia de potencial: el volt, a la que se suele también llamar de manera más familiar, voltaje.
La posibilidad práctica de construir pilas voltaicas produjo una revolución en el estudio de la electricidad. Hemos de mencionar que en muchos laboratorios era muy poco factible construir las máquinas de electricidad por fricción, ya que eran bastante caras; sin embargo, las pilas eran relativamente baratas. Permitieron el avance de la ciencia química ya que estaban al alcance de muchos laboratorios; de otra manera no se hubieran podido realizar muchas investigaciones científicas. Gran parte de los primeros descubrimientos electroquímicos fueron hechos precisamente con pilas voltaicas. Poco después de haber recibido una carta de Volta en la que explicaba cómo construir una pila, William Nicholson (1753-1825) y Anthony Carlisle (1768- 1840) construyeron en Londres uno de estos dispositivos, y con el fin de conseguir una mejor conexión eléctrica, conectaron cada una de las terminales de la pila a un recipiente con agua. Se dieron cuenta de que en una de las terminales aparecía hidrógeno y en la otra, oxígeno. Fue así como descubrieron el fenómeno de la electrólisis, en el que, por medio de una corriente eléctrica, se separan los átomos que componen la molécula del agua. Humphry Davy (1778-1829), también en Inglaterra, descompuso por medio de la electrólisis otras sustancias, y así descubrió los metales sodio y potasio al descomponer electroquímicamente diferentes sales minerales, como la potasa cáustica, la soda fundida, etc. También obtuvo electroquímicamente los elementos bario, calcio, magnesio y estroncio. Poco después Faraday descubrió, también con las pilas voltaicas, las leyes de la electrólisis.