PARADA TÉCNICA
EVALUACIÓN DE LA TEORÍA DEL FLOGISTO. LA GRANDEZA DE LAVOISIER VA MÁS ALLÁ DE SU EXPLICACIÓN DE LA COMBUSTIÓN.
LA TEORÍA del flogisto ocupó las mentes de los científicos por más de 150 años
y fue en la historia del desarrollo del concepto de elemento la barrera por
vencer para el establecimiento definitivo de la química como ciencia. Es uno
de los casos en que lo aparentemente razonable es estéril, como el concepto
de movimiento de Aristóteles en mecánica o el geocentrismo en astronomía.
Diversos autores han tratado con benevolencia la teoría del flogisto con el argumento de que "fue la primera generalización en la química que correlacionó de una manera sencilla y comprensiva gran número de fenómenos químicos y algunas relaciones existentes entre una variedad enorme de substancias". Sin embargo, es difícil ver cómo el ficticio flogisto pudo haber facilitado nada fungiendo como factor unificador o fundamento. Otros han señalado también que, dentro del marco de la teoría flogística, muchos experimentos se llevaron a cabo que difícilmente se les hubiera ocurrido hacer a los investigadores de haber imperado un marco teórico diferente. Pero también se puede argüir que se llevaron a cabo muchos experimentos importantes bajo los sistemas teóricos precedentes, y se puede sostener que el surgimiento de la química como ciencia fue notablemente tardío y que el retraso fue debido a la intrusión de la teoría del flogisto, que hizo la transición de la química de Boyle y Mayow a la de Lavoisier más difícil en vez de más fácil. Se forzó esta teoría a una finalidad de explicación total, hasta convertirla en un verdadero camaleón. Así, por ejemplo, el hecho de que los cuerpos cambien de color con diferentes grados de calentamiento, se explicaba como debido a que contenían diferentes cantidades de flogisto, pero no se daban números que representaran la cantidad de esa substancia, números que todo el mundo pudiera en principio calcular o medir. La historia del flogisto ejemplifica que, en ciencia, si bien una teoría es mejor mientras mayor sea el número de fenómenos que explica, será ociosa, inútil y hasta contraproducente, mientras no lo haga de manera cuantitativa y auto consistente.
Ha sido más provechoso, incomparablemente, para el progreso de nuestro conocimiento de la Naturaleza, el enunciar la ley de la conservación de la masa en las reacciones químicas, aunque no explique muchas cosas de las reacciones mismas, que enunciar la hipótesis del flogisto, y esto a pesar de que la ley de conservación de la masa en las reacciones químicas no es exacta en principio, como lo establece la física moderna, que requiere que sea la masa-energía la magnitud física que se conserve en un sistema aislado. Pero ocurre que el calor absorbido o cedido, aun en la más violenta de las reacciones químicas, una explosión de dinamita, por ejemplo, no representa en variación de masa total, ni siquiera un milésimo de miligramo por tonelada de reactantes, por lo que en las operaciones del laboratorio de química, en las operaciones industriales y en los procesos biológicos, la pérdida o ganancia de masa asociable a la energía cedida al entorno o ganada de él por el sistema químico, es experimentalmente indetectable. Así, en química clásica se consideran las leyes de conservación de la masa y de la energía como leyes que se cumplen separadamente.
El trabajo de Lavoisier había traído un orden y una sistematización a la química que nunca antes había conocido, sin embargo la nomenclatura de las substancias seguía en la mayor confusión. Se continuaban usando los términos alquímicos, y era para los aprendices de química un esfuerzo brutal de memoria aprender los nombres de un número cada vez mayor de substancias con las cuales tenían que tratar. En 1782, Guyton de Morveau publicó un trabajo sobre formas de sistematizar la nomenclatura química. Lavoisier; naturalmente, se interesó y se unió a Morveau en este objetivo; a ellos se unieron Berthollet y Fourcroy. Sus resultados aparecieron en el libro titulado Méthode de nomenclature chimique, en 1787. Este volumen contiene las reglas para nombrar a los compuestos químicos que prácticamente son las mismas que se usan hasta nuestros días. La teoría de Lavoisier estaba completa, con un lenguaje adecuado a ella, aunque haya sido en los años siguientes cuando se dedicó al estudio de la respiración de los animales. Sin embargo, la mayoría del mundo científico, alejado del grupo de sus más allegados, todavía perdía el tiempo luchando con las discrepancias de la teoría del flogisto. En vista de ello, Lavoisier se determinó a preparar un texto de química basado en las nuevas ideas, que rompiera bruscamente con los textos tradicionales de química y tal que las futuras generaciones de químicos encontraran en él un buen cimiento para construir. En 1789, publicó su Traité elémentaire de chimie, que junto con los Principia constituye el punto de partida de la ciencia moderna. En este libro, Lavoisier describe con considerable detalle la base experimental de su rechazo del flogisto y de su nueva teoría de la combustión. Su punto de vista es esencialmente el de un científico moderno. En él enuncia con toda claridad su idea de la conservación de la masa e ilustra abundantemente la manera de aplicarla en química; presenta "una tabla de substancias simples, que pueden ser consideradas los elementos de los cuerpos". Admitió que ésta era un lista empírica, sujeta a revisión a medida que se descubrieran nuevos hechos. Constituye la primera tabla de los verdaderos elementos químicos. La traducción del Traité a las lenguas más usadas siguió rápidamente a su publicación. En nuestro país se realizó la primera traducción al español, en el mundo, del primer tomo, que apareció a finales de 1797. La importancia del Traité no puede exagerarse; con la notable excepción de Priestley, todos los químicos importantes se convirtieron a la nueva teoría y la química entró a un siglo de progreso asombroso.
Pero ¿y la constitución de la materia? Me dirá el lector, ¿qué pasó con los átomos? ¡Ah, para allá vamos, no se me ha olvidado!
Una vez que se captaron dos ideas, la de conservación de la masa y la de elemento químico, el investigador francés José Luis Proust (1754-l826) pudo por experimentación propia, nueva, y por verificación de resultados de otros investigadores, hallar un hecho que expresó de la siguiente manera, "un compuesto es un ente privilegiado al cual la Naturaleza asigna una proporción fija de sus elementos constituyentes; es en resumen una substancia que la Naturaleza nunca crea, aun cuando sea por mediación del hombre, más que con la balanza en la mano [...] Reconozcamos que las propiedades de los verdaderos compuestos son invariables como lo es la proporción de sus constituyentes. De polo Norte a polo Sur, los compuestos se encuentran idénticos en estos dos respectos. Su apariencia podrá variar; debido a la manera de agregación, pero sus propiedades químicas, nunca. Hasta ahora no se han observado diferencias entre los óxidos de hierro del Sur y los del Norte. El cinabrio de Japón está constituido en la misma proporción que el de España. La plata no se oxida o muriatiza en forma diferente, en el muriático del Perú que en el de Siberia [...] Si encontramos imposible hacer una onza de ácido nítrico, de un óxido, de un sulfuro, o una gota de agua, con proporciones diferentes entre sus constituyentes, de aquellas que la Naturaleza les ha asignado desde la eternidad, debemos reconocer que existe una balanza, la cual regula incluso en nuestros laboratorios las proporciones de los constituyentes en los compuestos".
En resumidas cuentas, cada vez que dos o más elementos se combinan para formar un compuesto, lo hacen en una proporción en peso, definida, fija.
Imaginemos que hacemos el siguiente experimento: pesamos varias muestras de 10 g de plomo cada una, el plomo es un metal lustroso, gris plateado; mezclamos cada una de ellas con una cantidad diferente de azufre, un polvo vítreo amarillo, digamos desde medio gramo, a tres gramos. Con calor llevamos las distintas muestras a que reaccionen en crisol de platino. Cuando la reacción ha terminado, notamos la aparición de un polvo negro, el sulfuro de plomo. En algunas de las muestras notamos que ha sobrado azufre y en otras que ha sobrado plomo.
Procedemos a separar el azufre en aquellas muestras que presentan un sobrante de azufre, agitando la muestra en disulfuro de carbono, un líquido en el que se disuelve el azufre pero no el plomo ni el sulfuro de plomo. Una vez separado el azufre, se seca el sulfuro de plomo y se pesa. El resultado será de 11.56 g. Si a esto restamos los 10 g de plomo que empleamos, obtenemos que se combinaron sólo 1.56 g de azufre, en todos los casos en los que sobró azufre. Y en todos ellos el porcentaje en peso es 86.5% de plomo y 13.5% de azufre. El cociente del peso de plomo al de azufre resulta ser 6.41.
En las muestras donde vemos que sobró plomo, con un pincel separamos el metal del polvo negro, pesamos el metal sobrante, restamos de 10 g, con lo que conocemos el peso de plomo que se combinó. Conocemos también el peso de azufre empleado en cada una de estas muestras y hallamos que el porcentaje de plomo es 86.5% y el de azufre es 3.5%, en todas. De modo que en el sulfuro de plomo, el porcentaje en peso de plomo es al de azufre como 6.41 es a 1.0 siempre, independientemente de cómo se halla preparado. 6.41/1.0 es la proporción fija en el sulfuro de plomo.
Si calentamos 45 g de óxido de mercurio, un polvo rojo (el calx de mercurio,
el mercurium calcinatum per se) en un matraz de cuello largo, vemos que
se forman 41.5 g de mercurio, un líquido plateado, y se escapa el oxígeno. De
la resta 45.0-41.5 obtenemos que se hallaban combinados 3.5 g de oxígeno
en el óxido de mercurio. El porcentaje en peso de mercurio es de 92.2% y el
de oxígeno 7.8%, y la proporción fija de mercurio a oxígeno es de 11.82/1.0.
Supóngase ahora que se calientan 15 g de mercurio con 1.0 g de aire, mezcla
que supondremos consta de 21% de oxígeno y 79% de nitrógeno. Cuando la reacción
se haya completado, ¿qué substancias y qué masas de cada una estarán presentes?1![]()
Vale la pena subrayar la diferencia clave entre mezcla homogénea o solución y un compuesto. Una mezcla, por ejemplo, de oxígeno con hidrógeno se puede preparar con la proporción en peso de hidrógeno a oxígeno que nos plazca. Puedo fabricar bronce con una variación casi continua de proporciones en peso de cobre a estaño. Las mezclas son pues de composición variable. No así los compuestos químicos. La proporción en peso de los elementos que los constituyen es fija. Si quiero preparar agua como lo hizo Cavendish, sin que sobre ni hidrógeno ni oxígeno, debo partir de una mezcla cuya proporción en peso de oxígeno a hidrógeno sea de 8/1. Ahora bien, ¿por qué? ¿Cuál es la razón física?
Es verdad que existen dos clases de agua, cada una con su proporción fija en peso de oxígeno a hidrógeno, que la hace ser ella misma, con su densidad, su punto de congelación, su índice de refracción, etc., peculiares, el agua común, 8/1 y la llamada agua oxigenada, 16/1. El asunto es que no existen ni pueden existir aguas con proporciones intermedias arbitrarias entre estas dos. ¿Por qué?
Dados dos elementos, ocurre que se pueden combinar de maneras diferentes para dar lugar a diferentes compuestos, pero cada vez que se obtiene uno cualquiera de ellos, identificado mediante sus propiedades, se encuentra que cumple siempre con la misma proporción constante. Por ejemplo, la combinación de carbono con oxígeno puede dar monóxido de carbono, gas muy tóxico que no enturbia el agua de cal, o bióxido de carbono que sí la enturbia, no es venenoso y es más denso. El primero tiene una proporción fija en peso de oxígeno a carbono de 4/3, y el segundo, de 8/3. Otra vez, no existen ni pueden existir óxidos de carbono con proporciones arbitrarias entre esas dos. ¿Por qué?
Que en un compuesto sus elementos componentes se encontraran siempre en una
proporción constante, no fue fácil de aceptar. Los experimentales, debido por
una parte a los errores inherentes a toda medición, entonces grandes, y por
otra, debido a que cuando dos elementos pueden dar lugar a varios compuestos
no lo hacen en forma excluyente, sino simultánea (por ejemplo, cuando arde carbón,
se forman los dos gases mencionados al mismo tiempo), creían en la posibilidad
de que, dentro de límites moderados, la composición podía variar; esto dio lugar
a hablar, por ejemplo durante todo el siglo XIX, de aguas mejores
unas que otras, o ya a finales del siglo XX, hay personas en el
Tercer Mundo que piensan que una aspirina (ácido acetilsalicílico) norteamericana
es mejor que una nacional.
La ley de la conservación de la masa y la ley de las proporciones constantes de Proust, son leyes macroscópicas, empíricas.
¿Cuál es su explicación en términos de la constitución de la materia? ¿Cuál es su razón física de ser? La respuesta, elegantísima, la dio Juan Dalton en 1808.
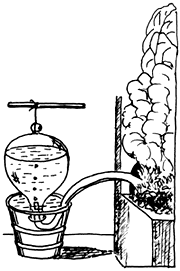
Figura 27. Cuba de Hales.
![[Inicio]](../img/begin.gif)