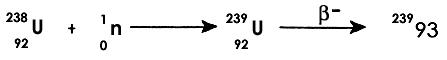
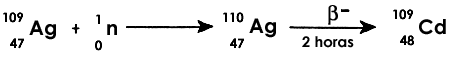V. LA FISIÓN NUCLEAR: OTTO HAHN Y LA ESCUELA ALEMANA
| PEDRO-BOSCH GIRAL |
"HOY que vamos de picada añoramos el momento cuando íbamos en
ascenso", le hace decir Carlos Fuentes al narrador de El prisionero de Las
Lomas. ¡Cuántas veces, cada uno de nosotros se ha lamentado del mismo modo!
Y sin embargo, nuestra crisis resulta menor si se la compara con los acontecimientos
que se produjeron en Alemania durante la vida de Otto Hahn. Por eso, en más
de un aspecto, para los que nos ha tocado vivir en "tiempo de austeridad", la
vida de Otto Hahn es ejemplar.
Hahn nació el 8 de marzo de 1879 en Francfort del Main y murió el 28 de julio de 1968 en Gotinga, Alemania. O sea que en su juventud disfrutó la prosperidad alemana de la posguerra del conflicto franco-prusiano, pero a los 35 años tuvo que enfrentarse con la primera Guerra Mundial y a los sesenta con la segunda.
Hahn vivió cambios sociales y políticos tan radicales como los que simultáneamente se produjeron en el campo de la física y de la química. Comprobó cómo de la mecánica newtoniana hubo que pasar a la relativista y, en el campo de la radiactividad, supo del descubrimiento del radio en 1896 por Henri Becquerel (1852-1908, premio Nobel de física en 1903) y del uso rutinario de las centrales nucleares en los sesentas.
Otto Hahn "quemó las naves" en más de una ocasión para lanzarse a lo desconocido. Y tenía a quién parecerse: su padre, de origen campesino, que pudo haber seguido la tradición agrícola de la familia, prefirió hacerse vidriero comprando su propia tienda y estableciéndose en Francfort. Su promoción de artesano a hombre de negocios coincidió con la bonanza que se produjo en Alemania después de la Guerra Franco-Prusiana (1870-1871). Los Hahn se convirtieron, entonces, en una respetable familia de la clase media que insistía en vivir austeramente. Sin embargo, esta prosperidad económica se veía nublada por la mala salud del pequeño Otto, que le duró hasta los catorce años.
En el colegio y durante el bachillerato, Otto Hahn fue un estudiante común y corriente a quien le interesaba la química. Esta vocación se confirmó cuando asistió a una serie de conferencias para adultos sobre el tema. Igual que su padre, no quiso seguir los caminos trillados: Otto se enfrentó a los deseos familiares, que querían verlo arquitecto, e ingresó a la Universidad de Marburgo en 1897 en la carrera de química. Su vida de estudiante transcurrió más en las cervecerías que frente al profesor de matemáticas o de física, según él mismo lo relata. Se dice que de aquel entonces le vino el gusto por el tabaco. A menudo se "iba de pinta" para asistir a conferencias de arte o de filosofía, y, desde luego, los encuentros románticos no faltaron.
Así y todo, en 1901 obtuvo el doctorado y después de pasar un año en la infantería volvió a Marburgo. Hahn consiguió entonces empleo de asistente de su profesor principal, Theodor Zincke. No está por demás subrayar que estos empleos eran muy disputados ya que se les consideraba trampolín obligado para ingresar a la industria. En efecto, la recomendación de un profesor determinaba la obtención de una plaza en las compañías químicas alemanas que, en aquella época, eran las más poderosas y avanzadas. A Hahn le ofrecieron un contrato que requería del dominio de un idioma extranjero. Por eso, con su propio dinero, se fue a Inglaterra en septiembre de 1904. Como Zincke no quería que permaneciese inactivo, le consiguió un lugar en Londres, en el University College con sir William Ramsay (1852-1916, premio Nobel de química en 1904), famoso por haber descubierto varios gases inertes.
Ramsay, en esa época, se interesaba en la radiactividad y contaba con la colaboración de Frederick Soddy (1852-1916, premio Nobel de química en 1904) que había trabajado con E. Rutherford. Sin embargo, como sucede frecuentemente, a Ramsay le faltaban ayudantes. Sin pensarlo dos veces le extendió a su joven visitante unos 100 gramos de bario para que de ellos extrajera los pocos miligramos de radio que contenían. El método a seguir era el de Marie Curie. Desde luego Hahn, que era químico orgánico, le explicó que desconocía el tema. Ramsay replicó que tendría entonces la ventaja de abordarlo sin ideas preconcebidas y que, además, preparando un compuesto orgánico (lo cual alimentaría notablemente la cantidad total de material estudiado) podría calcular el peso atómico a partir de los pesos moleculares. Así intentarían confirmar la determinación de Curie. El método inicialmente usado por los Curie para separar elementos radiactivos y determinar sus propiedades químicas consistía en poner en solución la sustancia radiactiva con otros cuerpos y usar varios agentes precipitadores. Se probaba, entonces, si el precipitado o la solución o ambos eran radiactivos. Suponiendo que ambos lo fuesen, se trataba entonces cada parte de un modo análogo, y se repetía el proceso hasta que una parte de los productos no fuese radiactiva y la otra parte presentara un decaimiento exponencial con la vida media característica. Los Curie aislaron así el radio (1898) a partir de la pechblenda mineral.
En el juego como en el amor, se habla de "la suerte de los principiantes" y de los "bandazos de la fortuna". En la vida de Hahn el primer bandazo fue aceptar llevar a cabo esa extracción, cambiándose de la química orgánica a la radiactividad, y la suerte de principiante fue la de enfrentarse con un material que contenía un alto porcentaje de torio además del uranio. Otto Hahn siguió la técnica de separación al pie de la letra y descubrió un nuevo radioelemento: el radiotorio, que de hecho era un isótopo del torio, pero en aquel entonces la existencia de los isótopos de los elementos todavía no se conocía.
El mismo Hahn cuenta:
El resultado final de mi trabajo fue, por lo tanto,
no la preparación de un estado puro, de quizás 9 mg de radio, sino el
descubrimiento de un nuevo "radioelemento" que producía la emanación
del torio pero que era más fuertemente radiactivo que el torio conocido.
Llamé a la sustancia radiotorio. ¿Cómo vino a dar esta sustancia a la
muestra de radio? La explicación es que la muestra no se extrajo de
una veta de uranio puro, sino de una veta llamada torianita, que existe
en Ceilán (hoy Sri-Lanka) y que contiene además de uranio un alto porcentaje
de torio. Hablando estrictamente, el descubrimiento del radiotorio fue
sólo un asunto de suerte. |
Entusiasmado Otto Hahn, junto con otro joven alemán, Otto Sackur, se enfrentó con un tema entonces muy polémico: ¿cuál era la diferencia entre el actinio reportado por A. L. Debierne (1874-1849) y el emanio de F. O. Giesel (1852-1927?) Los dos jóvenes investigadores demostraron que eran idénticos. En detalle, sucedió lo siguiente.
Debierne, que trabajaba con los Curie, encontró, entre los hidróxidos utilizados en el tratamiento de la pechblenda, un nuevo elemento al que llamó actinio. Su vida media era sólo de unos cuantos segundos.
Simultánea e independientemente Giesel descubrió, al tratar de preparar radio a partir de pechblenda para la Fábrica de Quinina de Brunswick, un elemento también de vida muy corta, al que llamó emanio.
Las propiedades químicas del actinio de Debierne y del emanio de Giesel, tal y como las describieron los dos descubridores, eran diferentes, por lo tanto, parecía que se trataba de elementos distintos. Ramsay consiguió muestras de ambas sustancias y se las entregó a Sacktir y a Hahn quienes determinaron con precisión la vida media de cada uno. Resultaron ser ambas de 3.9 s; por lo tanto, el actinio y el emanio tenían que ser el mismo elemento. Se decidió retener el nombre de actionio, ya que el artículo de Debierne precedió el de Giesel. Sin embargo, sabemos que éste entendía mejor las propiedades (muy parecidas a las del lantano, por cierto) de este elemento.
En vista de los éxitos obtenidos, Hahn decidió no corregir el rumbo y dedicarse a la radioquímica. Con el apoyo de Ramsay, que lo estimaba mucho y que estaba convencido de que tales dotes para la investigación se perderían en la industria, consiguió una plaza en el Instituto de Química de la Universidad de Berlín, dirigido por Emil Fischer (1852-1919, premio Nobel de química en 1902). Antes de ocuparla, decidió pasarse unos cuantos meses en Montreal con Ernest Rutherford (1871-1937, premio Nobel de química en 1908) para especializarse de lleno en el estudio de las desintegraciones radiactivas.
En septiembre de 1905, a los 26 años, O. Hahn cruzó el Atlántico para incorporarse a la Universidad McGill en Montreal.
Figura V.1. Los elementos radiactivos liberan tres clases de radiaciones que se pueden separar mediante un campo eléctrico.
¡Cuál no fue su sorpresa al comprobar que se le recibía con cierta reserva! No creían en la veracidad de sus descubrimientos porque B. B. Boltwood (1870-1927), un buen amigo de Rutherford y sobresaliente radioquímico de Yale, había trabajado con el radiotorio descubierto por Hahn y había determinado que: "la substancia viene a ser un nuevo compuesto de ThX y de estupidez". Sin embargo, Hahn supo demostrar que el radiotorio existía y además logró hacerse amigo de todos sus nuevos colegas, incluyendo al mismo Boltwood.
Hahn escribió:
El ambiente en el instituto de Rutherford era de
lo más estimulante. Rutherford todavía no se había vuelto mundialmente
famoso como para atraer muchos alumnos[...] el único forastero, además
de mí, era el doctor Max Levin de Gotinga, y él también estaba estudiando
radiactividad. Después fue profesor en Gotinga pero, más adelante, por
razones extrañas, tuvo que ocuparse de la fábrica de relojes de su padre.
|
En una ocasión la revista inglesa Nature quiso publicar una fotografía de Rutherford, al que le importaba muy poco la apariencia externa. Sin embargo, al público inglés no se le podía presentar un retrato en el cual no se viesen los puños albeantes de la camisa asomando bajo las mangas de la chaqueta. Fue Otto Hahn el que le prestó a Rutherford sus puños postizos (puños que, como el cuello, se ponían y se quitaban a las camisas para poderlos lavar y almidonar por separado) para que el neozelandés posara luciendo impecable. Otto Hahn presumía de que al menos sus puños habían sido inmortalizados por Nature en 1906, mismo año en el que el que pasó a formar parte de la Universidad de Berlín, ya "transmutado" de químico orgánico a radioquímico.
Hahn se incorporó en 1906 al instituto dirigido por Fischer. De recién llegado, para proseguir sus investigaciones, estableció una relación, provechosa para ambas partes, con "Knofler y compañía", que eran los productores de preparaciones de torio. En Canadá, Hahn había encontrado que la vida media del radiotorio era de dos años, pero Boltwood (¡otra vez Boltwood!) argumentaba, con base en sus resultados, que debía ser menor. Hahn probó, estudiando muestras preparadas, varios años antes, que la actividad disminuía al principio y luego aumentaba gradualmente. Es decir, que debía existir un radioelemento entre el torio y el radiotorio. Otto Hahn consiguió separarlo en 1907 y lo llamó mesotorio. Como químicamente no es fácil separarlo del radio, material escaso en Alemania, y como la demanda de radio crecía, Knofler y Compañía decidieron vender, con mucho éxito por cierto, el mesotorio de gran actividad, al que se conoció como radio alemán.
Otto Hahn nos cuenta:
Un día Emil Fischer me mandó llamar para que le
procurara información sobre la radiación del mesotorio a un profesor
del Charité-Hospital de Berlín que quería usarlo para irradiar cultivos
de tubérculos. El viejo Geheimrat me recibió amablemente y entonces
empezó a describir los experimentos que había llevado a cabo con "semitorio".
Cuando repliqué, con toda la modestia debida, que el nombre correcto
era mesotorio, me dio una amistosa palmada en la espalda y dijo: "¡Créame
joven colega, la sustancia se llama semitorio!" Recordando la mala impresión
que causé en el Congreso de Bunsen, esta vez, con recién estrenada modestia,
tuve buen cuidado de no corregir su error. |
Con la misma modestia recuerda:
Todos mis intentos de separar uno del otro los dos
"elementos", radio, y mesotorio, fallaron. Resultaba tan imposible como
separar el radiotorio del torio. El parecido químico entre las sustancias
era evidentemente mayor que el que hay, por ejemplo, entre las tierras
raras; nadie aún había pensado, sin embargo, en la posible existencia
de los isótopos. |
Al año de su regreso a Alemania, Otto Hahn ya era privatdozent (profesor auxiliar) y en 1910 profesor. Muy pronto se hizo amigo de sus colegas físicos, entre ellos Walther Nernst (1864-1941) y de compañeros más jóvenes como Max von Laue (1879-1960), Adolf von Baeyer (1835-1917), Gustav Hertz (1887-1975) y James Franck (1882-1964), todos ellos premios Nobel entre 1905 y 1925.
Esto no quiere decir que aun en un medio tan privilegiado intelectualmente no existiesen los "valores establecidos". Por ejemplo en 1907, durante un congreso, su amigo Max Levin tuvo que sugerirle a Otto Hahn que fuese más prudente en algunas de sus intervenciones, pues acababa de oír a un profesor de la vieja guardia decirle a otro: "Oh, es uno de esos berlineses britanizados", refiriéndose a Hahn. Fue a partir de este incidente cuando Hahn decidió "volverse modesto", tal y como lo probó en su entrevista con el Geheimrat que referimos arriba. Hasta Emil Fischer era uno de los que difícilmente aceptaban que se pudiese detectar, por métodos radiactivos y por sus propiedades químicas, cantidades muy por debajo de lo que se puede pesar. En la conferencia inaugural del curso dictado por Otto Hahn en 1907, Fischer declaró que para ciertas sustancias la prueba más fina era la del olfato, y difícilmente se encontraría otra más sensible. Esta actitud conservadora y tradicionalista fue característica de los químicos, mientras que los físicos se mostraron más avanzados, entre ellos la austriaca Lise Meitner (1878-1968).
A Berlín llegó de Viena Lise Meitner en el otoño de 1907 para
efectuar un trabajo teórico bajo la dirección de Max Planck (1858-1947, premio Nobel de física en 1918) y para llevar a cabo algunos
estudios experimentales sobre la radiactividad. Así empezó una
colaboración fructífera entre Hahn y Meitner, que tenían la misma
edad. Trabajaron bajo el mismo techo durante 31 años. Su
colaboración se vio interrumpida porque Meitner tuvo que escapar
de Alemania, huyendo de la persecución política y racial. Pero
volvamos al año 1907, Hahn nos cuenta:
En aquellos días no se permitía a las mujeres trabajar
en el Instituto Fischer. Cuando le planteé la colaboración a Emil Fischer,
le otorgó un permiso a la señorita Meitner para que trabajase conmigo
en la carpintería de la planta baja del instituto (Otto Hahn se refiere,
aquí, al local en donde estaba instalado su laboratorio, y que había
sido una carpintería), en donde se llevaban a cabo las medidas de radiactividad:
le solicitó, sin embargo, que no entrase a los cuartos de estudio del
piso superior ya que sentaría un mal precedente |
También por aquellos días Hahn disponía, en su laboratorio, de una colección casi completa de radioelementos. Él y Lise Meitner decidieron observar las radiaciones beta, es decir, los electrones emitidos por los materiales radiactivos. Comprobaron que varios elementos, al contrario de lo que se creía, eran emisores de radiaciones beta cuando decaían.
Cuando el nuevo Instituto de Química (Institut für Chemie) de la Sociedad Kaiser Wilhelm abrió sus puertas en Berlín-Dahlem a finales de 1912, a Hahn lo nombraron jefe de un departamento de radiación pequeño pero independiente, del cual, desde luego Meitner formaba parte. Como este laboratorio era nuevo, no estaba contaminado, lo cual les permitió estudiar substancias de radiactividad tan débil como el rubidio y el potasio. Se interesaron entonces en fechar rocas gracias a dichos elementos. Con los años este laboratorio se dividió en dos grandes departamentos, uno abocado a la radioquímica, dirigido por Hahn, y el otro a la física nuclear, dirigido por Meitner. Recuerda Otto Hahn:
Después de mudarnos de nuestro territorio contaminado
del Instituto de Química al recién levantado Instituto de Química de
la Sociedad Kaiser Wilhelm (1913), pudimos hacer trabajo experimental
con los elementos débilmente activos, potasio y rubidio. Muchos años
después estas investigaciones llevaron a lo que se llamo "método del
estroncio" para determinar la edad geológica. |
|
Método de estroncio |
|
Los elementos radiactivos naturales son, sobre todo, isótopos de los elementos con número atómico mayor de 80, es decir, que en la tabla periódica se encuentran más allá del mercurio (Hg). Estos elementos radiactivos se prestan a numerosos métodos de fechado (o medida de antigüedad) de muestras geológicas o arqueológicas. En un sistema aislado, la ley según la cual decrece el número total de átomos del padre (N) y aumenta el número de átomos del hijo (D) está dada por: No=N+D, en donde No es el número inicial de átomos del padre. Además, se sabe que como el padre decae el número de átomos del padre es función del tiempo (t): Ln N=-l t + Ln No. o sea N=Noe-lt en donde l = Ln2 /t1/2 No se debe confundir t, que es el tiempo que se desea determinar, y t1/2 que es la vida media del elemento inicial. Así, el tiempo transcurrido desde el origen del sistema es: t = (1 / l) Ln (1 + D / N ) porque N = ( N+D ) e-lt Por lo tanto t se puede deducir a partir de l y de la abundancia relativa del átomo padre y del átomo hijo. La desintegración del 87Rb en 87Sr es la filiación más importante en la medida de muestras geológicas. El rubidio natural (Rb) es una mezcla de los isótopos 85Rb (72.15%) y 87Rb (27.85%). El contenido de estroncio, "común y corriente" en el 87Sr (no radiactivo) es de 7.02%. El periodo (o sea l) del 87Rb, que es de 4.7 x 1010, años nos permite hacer las siguientes aproximaciones: N ~ No ( 1- l t) D = No - N = No l t t = (No - N) / l No ~ D / l No que es una ecuación sencilla, pero que necesita de una determinación muy precisa del contenido de estroncio 87Sr no radiactivo en la muestra. Este método es efectivo en el caso de las micas, por ejemplo. En general el estroncio se extrae por vía química y el contenido de Sr se determina por espectrometría de masas. |
Éstos fueron también los años en los que se hicieron los avances más importantes en la teoría de la radioquímica. Fajans y Soddy, independientemente, concluyeron en 1913 que cada grupo de especies inseparables (como el radiotorio y el torio) correspondían a un solo elemento químico, o sea que se debían clasificar en el mismo sitio de la tabla periódica. Por eso Soddy propuso designar a las especies de un grupo como isótopos, del griego iso, mismo, igual, y topos, lugar. Es decir, que en cada casilla de la tabla periódica se debe incluir a todos los átomos que tengan el mismo número de protones (número atómico) aunque su masa sea diferente (o sea, aunque tengan diferente número de neutrones), tal y como lo explicamos anteriormente.
Como otros radioquímicos, Hahn ya estaba familiarizado con hechos como la imposibilidad de separar el mesotorio del radio o el radiotorio del torio. Pero las generalizaciones necesarias para explicar estos rompecabezas no eran su fuerte. Hahn era, ante todo, un excelente experimentador.
Sintiendo que su vida ya estaba encarrilada, Hahn se casó con Edith Junghans en 1913, más la fatalidad quiso que, un año después, estallara la primera Guerra Mundial y que tuviese que incorporarse a un regimiento. En 1915, a los treinta y seis años con grado de sargento, participaba activamente en la guerra química, bajo la dirección científica de Fritz Haber (1868-1934 premio Nobel de química en 1918). Así, se vio envuelto en el desarrollo, prueba, manufactura y uso de nuevas armas, y vivió el conflicto en el frente occidental durante el otoño de 1914. Cuando se encontraba en Bruselas en enero de 1915 se le ordenó que llamara a Fritz Haber, que entonces se encontraba también en Bélgica cumpliendo con una misión para el Ministerio de la Guerra.
Haber le explicó que la guerra se había visto paralizada en las trincheras y que hacían falta nuevas armas para romper el estancamiento. Anteriormente se habían probado irritantes químicos con el propósito de hacer inhabitables las trincheras. Sin embargo Walter Nernst había tenido poco éxito y el propio Haber dio por terminado el trabajo en diciembre de 1915 cuando una explosión en su laboratorio mató a Otto Sackur. Cuando Hahn visitó a Haber un mes después, ya no se trataba de sacar al enemigo de las trincheras sino de matarlo, y por eso se investigaban las posibilidades bélicas del cloro.
A Hahn, ahora teniente, y a algunos de sus colegas (James Franck, Gustav Hertz, Wilhelm Westphal y Erwin Madelung) los concentró el ejército en una nueva unidad: el Regimiento 36 donde se les entrenó en los usos de los gases venenosos, la defensa contra ellos y la meteorología. En un par de meses ya estaba Hahn de regreso en Flandes como miembro de un regimiento de infantería: era el experto en gases. Una vez instalados los cilindros de gas a lo largo del frente, se planeó el ataque en repetidas ocasiones. Había que programarlo con 24 horas de adelanto para poder trasladar las unidades de la retaguardia hasta el frente pero, en todas las ocasiones, condiciones climáticas adversas, obligaron a cancelar la operación. El Alto Mando decidió entonces mover los cilindros a Yprès, Bélgica donde los vientos solían ser favorables. En abril de 1915 se liberó el gas de 5 000 cilindros distribuidos en un frente de más de 6 km y se formó una nube de 640 a 915 m de espesor que fue a dar a las líneas francesas afectándolas gravemente. Casi una división se asfixió, más de 15 000 hombres resultaron afectados y un tercio de ellos murió. Este suceso se suele considerar como el inicio de las guerras químicas "científicamente" organizadas.
Ni la guerra química, ni ningún tipo de destrucción iban con el carácter de Hahn, tan preocupado por los problemas morales. En su autobiografía escribió:
Como resultado de trabajar con sustancias tan tóxicas
nuestras mentes se nublaron tanto que perdimos todo escrúpulo. En cualquier
forma, para entonces nuestros enemigos habían copiado nuestros métodos
y, como se perfeccionaron rápidamente en este tipo de guerra, nos convertimos
paulatinamente en receptores del ataque y fuimos dejando de ser los
agresores. Otro factor que se debe considerar es que nosotros, como
observadores del frente, pocas veces vimos los efectos directos de nuestras
armas. En general, todo lo que sabíamos era que el enemigo había abandonado
las posiciones que se habían bombardeado con granadas de gas. |
En ambos lados del frente hubo combatientes a quienes participar
en la guerra con armas de gas no les provocó sentimientos de
culpa. Se invocó la necesidad de defenderse, y la reacción de los
aliados fue brutal. Cierta instalación de desarrollo e investigación
situada cerca de Washington, por ejemplo, sólo contaba con dos
edificios cuando EUA entró en la guerra mas, para la fecha del
Armisticio, había 50 edificios y trabajaban allí 1 200 científicos. Un
grupo de investigación dirigido por James Bryant Conant elaboró un
proceso para producir gas mostaza (mucho más mortífero que el de
los alemanes) cuando un grupo británico, encabezado por William
Pape, acababa de lograr lo mismo. Pero, volvamos a Hahn y a la
primera Guerra Mundial.
De esa época. Otto Hahn relata esta anécdota:
Durante la primera Guerra Mundial mi coronel me
presentó a un oficial superior con las palabras: "En la vida civil el
teniente Hahn es profesor y descubrió el mesotorio." El oficial contestó:
"Entiendo que el teniente Hahn es químico: ¿pero qué tiene que hacer
con animales antediluvianos? |
A pesar de tanta actividad, antes del armisticio Hahn tuvo la oportunidad de visitar su laboratorio en Berlín-Dahlem. Con Meitner, en 1917, descubrió el isótopo más estable del elemento 91, que llamaron protactinio (Fajans y Gohring, en 1913, habían descubierto este elemento, el 91, y lo habían bautizado brevium debido a su muy corta vida).
Como ya casi todos los elementos naturales habían sido descubiertos, los temas de investigación básica en radioquímica eran muy limitados. Hahn se dedicó durante los doce años siguientes a estudiar las aplicaciones de la radiactividad a los problemas químicos hasta que la radioquímica resurgió para transformarse en química nuclear con el gran acontecimiento de 1932: James Chadwick (1891-1974, premio Nobel de física en 1935) descubrió el neutrón. Solo dos años después, en 1934, Irène Curie (1897-1956) y Frédéric Joliot (1900-1958) (premios Nobel de física en 1935), pusieron en evidencia los tres primeros radioisótopos artificiales y un nuevo mecanismo de desintegración beta por emisión de electrones positivos, llamados positrones y definidos como partículas elementales de carga positiva y de la misma masa que el electrón negativo. ¡Es decir que los Joliot-Curie habían descubierto la radiactividad artificial! Es sorprendente que nadie pensara que el resultado de una desintegración nuclear debería ser un núcleo inestable, aunque durante 30 años se estuviese familiarizado con los núcleos inestables.
Otto Frisch, de quien hablaremos en detalle más adelante, comentó:
Después del descubrimiento hubo una especie de
estampida de borregos para repetir el experimento con las más obvias
variaciones (yo fui uno de los borregos). Sólo Fermi tuvo la inteligencia
de lanzarse en una dirección muy diferente y extremadamente fructífera.
|
Para ello, Fermi disponía del instrumental adecuado. Al enterarse del descubrimento de los Joliot-Curie, propuso un experimento para comprobar si con neutrones, se formaban núcleos radiactivos. La mayor parte de los investigadores encontraron que semejante experimento no tenía futuro, ya que se disponía de mucho menos neutrones que de partículas alfa (las partículas alfa no son más que núcleos de helio). Pero no se dieron cuenta de que a los neutrones como no tienen carga, no los frenan los electrones y no los repele el campo de Coulomb del núcleo, esto es, son más eficaces que las partículas alfa. Es más: el neutrón, al acercarse al núcleo, queda sujeto a las intensísimas fuerzas que existen entre los protones y los neutrones del núcleo.
Cuatro semanas después del descubrimiento de los Joliot-Curie, Fermi publicó los primeros resultados que probaban que varios elementos se vuelven radiactivos cuando se les bombardea con neutrones. Un mes más tarde ya anunciaba que el bombardeo del uranio producía una nueva radiactividad que parecía deberse a elementos transuránicos, o sea elementos con más de 92 protones y, por lo tanto, situados más allá del uranio en la tabla periódica.
Y como sucede muy a menudo, un resultado equivocado dio el empujón necesario. Este "descubrimiento" puso a Hahn y a Meitner en el camino de la fama. Ambos se sintieron desafiados ya que consideraban al protactinio su coto privado; fueron ellos, en efecto, los que nombraron al elemento y los que encontraron al único isótopo natural de protactinio que existe en cantidades pesables: el protactinio - 231 ( 3.3 x 104 años). Aún más, Hahn había descubierto con protactinio-234 el fenómeno del isomerisino nuclear, o sea la existencia de dos núcleos con el mismo número de protones y de neutrones pero con diferentes vidas medias: 1.17 m para el metaestable (m) y 6.75 horas para el estado base (g). Fue Lise Meitner quien se interesó de inmediato en las reacciones nucleares de Fermi y quien convenció a O. Hahn de reiniciar la colaboración interrumpida hacía 12 años. La idea era centrarse en los elementos transuránicos. En una primera nota sus observaciones estaban de acuerdo con la interpretación de Fermi, pero había que investigar qué eran todos esos "nuevos elementos", interpretar tantos resultados sorprendentes y entender el mecanismo por el cual se formaban.
Era la época en la que Leo Szilard bromeaba diciendo que si un hombre, de repente, hacía algo inesperado había una mujer detrás de él, pero que si un núcleo atómico hacía algo inesperado seguramente había un neutrón detrás de él. Lise Meitner escribió:
Encontré que estos experimentos eran tan fascinantes
que en cuanto aparecieron en Nuovo Cimiento y en Nature convencí
a Otto Hahn de colaborar directamente conmigo otra vez [...] para resolver
estos problemas. Me pareció muy sorprendente que el uranio diera lugar
a una cadena tan larga de emisores b consecutivos. |
Se trataba, pues, de un problema de física nuclear, así que ahora era Lise Meitner quien definía el problema y dirigía al grupo de Berlín. Sin embargo, la ayuda de Hahn era fundamental. La Meitner le confesó a Max von Laue "que no se llegaría a ningún sitio en este campo sólo con la física. Hacía falta la ayuda de un químico del calibre de Otto para tener éxito". Una vez más se comprueban las características de la ciencia moderna: el trabajo en equipo y la interdisciplinaridad. Sin embargo todo este trabajo se veía muy entorpecido por la situación política de Alemania. Hitler tomó el poder en 1933 y el Partido Nazi se convirtió en el único autorizado. Los primeros campos de concentración aparecieron en 1933.
En unos cuantos meses las universidades alemanas perdieron al 25% de sus físicos debido a las políticas raciales de Hitler. Entre ellos Einstein, Franck, Born, Otto Stern y muchos profesores jóvenes quienes aún no eran tan conocidos. Aunque Lise Meitner no escondía sus raíces judías, no fue despedida. Su primer impulso fue renunciar a su plaza pero sus amigos la convencieron de no hacerlo. Después lo vio claramente: "quedarse hubiese tenido el efecto de apoyar a Hitler."
En 1933 era difícil adivinar el futuro, así que permaneció en Berlín. Allí disponía de todo lo necesario para trabajar y mal que bien el instituto consiguió barajar sus cartas políticas con mucha cautela para esquivar las persecuciones raciales y políticas.
A mediados de 1935, el dúo Hahn-Meitner le pidió al joven Fritz Strassman, un experto químico analítico, que colaborara con ellos. Se formo así un equipo armonioso tanto desde el punto de vista científico (químico, físico, químico analítico) como político: Meitner, "no aria", Hahn, conocido por sus puntos de vista antinazi y Strassmann, el valiente joven que se negó a unirse al Partido Nazi o a cualquier organización afín, y que por lo tanto tenía todas las puertas cerradas fuera del Instituto.
No fue sino en marzo de 1938 (cuando se produjo la anexión de Austria por los nazis) que empezaron a propagarse rumores de que Lise Meitner (judía austriaca) podría perder su plaza y de que se le impediría salir de Alemania para proteger los secretos científicos. El 13 de julio de 1938, Meitner se escapo literalmente "de contrabando" con la ropa que traía puesta y unas cuantas monedas en el bolsillo. Logró llegar a Holanda gracias a sus amigos Dirk Coster y Adrian Fokker. Iba sin pasaporte ni papeles pero logró pasar después a Dinamarca y luego a Suecia, en donde Manne Siegbahn la acogió en el Instituto Nobel de Estocolmo.
HAHN Y STRASSMAN DESCUBRIDORES
En Francia, Irène Curie y su colaborador yugoslavo Pável Savitch lograron aislar, después de bombardear al uranio con neutrones, una sola substancia cuya vida media era de 3.5 horas. Lo consiguieron cubriendo sus muestras con una capa gruesa de bronce. Esta sustancia, por su comportamiento químico, parecía ser torio.
Hahn revisó el trabajo y concluyó que no era torio. Así se lo comunicó a los franceses, que en un artículo del verano de 1938 reconocieron que, en efecto, la problemática substancia no se comportaba como el actinio, añadiendo que se parecía mucho al lantano. Curie y Savitch escribieron textualmente "Se puede separar por fraccionamiento."
¡Qué cerca estaban de la fisión nuclear! El mismo Hahn nos dice:
de hecho su sustancia era sin lugar a dudas el
mismo lantano. Si la señora Joliot-Curie y Savitch lo hubiesen reconocido,
hubiesen estado a punto de descubrir la fisión. |
Nuevamente Hahn, esta vez con Fritz Strassmann y ya sin Meitner, puso manos a la obra y repitió este trabajo. Hahn y Strassmann descubrieron productos radiactivos que se comportaban en parte como el actinio, en parte como el radio. Determinaron cuidadosamente las propiedades de este "radio" y se dieron cuenta de que eran idénticas a las del bario. Hahn explica: "En breve, nuestro 'radio' artificial no se podía separar del bario ¡por la sencilla razón de que era bario!" Otto Frisch cuenta:
Fue entonces cuando yo aparezco, porque L. Meitner
se sentía sola en Suecia y, como sobrino devoto, fui a visitarla en
Navidad. Allí, en un pequeño hotel, en Kungalv, cerca de Goteborg, la
encontré desayunando y meditando sobre una carta de Hahn. Me mostré
escéptico sobre el contenido —que el bario se formaba por bombardeo
del uranio con neutrones— pero ella siguió dándole vueltas. Caminamos
en la nieve, yo con esquís, ella a pie[...] y gradualmente la idea fue
tomando forma[. ..] era un proceso que se debía explicar en términos
de la idea de Bohr, o sea que el núcleo era como una gota líquida; semejante
gota puede elongarse y dividirse. Pensé en la manera como la carga eléctrica
del núcleo hubiese disminuido la tensión superficial y vi que sería
cero para Z = 100 y seguramente muy pequeña para el uranio[...]. En
el primer artículo utilicé la palabra "fisión", que me sugirió el biólogo
norteamericano William A. Arnold, a quien le pregunté cómo se llamaba
la división de una célula. |
[Hahn nos lo cuenta así:]
En enero de 1939 publicamos un resumen de estos
experimentos que se separan de todos los experimentos previos en física
nuclear. Al interpretar los experimentos fuimos muy cautelosos, en parte
porque la serie de pruebas todavía no estaba totalmente terminada —duraron
varias semanas. Pero nuestra cautela no se debía a desconfianza en nuestros
resultados. En efecto, yo había comprobado nuestra conclusión, ya que
habíamos identificado como lantano un producto de decaimiento de uno
de nuestros isótopos de radio, lo cual significaba que el padre debía
ser radio y no bario. Nuestra excesiva cautela se debía, sobre todo,
al hecho de que, como químicos, no nos atrevíamos a anunciar un descubrimiento
revolucionario en física. Sin embargo, hablamos de "estallido" del uranio,
así llamamos al sorprendente proceso que había producido bario, muy
abajo en la tabla periódica[...]. Inmediatamente después de aparecer
nuestro artículo, Meitner y su sobrino Otto Frisch, independientemente,
salieron con su histórica publicación demostrando cómo el modelo atómico
de Niels Bohr podía explicar el rompimiento de un átomo pesado en núcleos
de tamaño medio. |
El papel de Hahn, en tan trascendental descubrimiento, fue aceptar los hechos
experimentales. En función de sus medidas afirmó que obtenía lantano y propuso
"el estallido" del núcleo, supo, además, convencer a su entorno (al revés de
I. Noddack, como veremos más adelante) mediante argumentos irrebatibles que
sacudieron los conocimientos de su época. Cuando Otto Frisch regresó a Copenhague
le contó a Bohr las conclusiones a que había llegado. Bohr estaba entonces a
punto de embarcarse hacia Estados Unidos, más se entusiasmó exclamando: "Pero
qué tontos hemos sido. Esto es maravilloso y justo como debe ser." Y lo instó
a publicar cuanto antes el resultado. Bohr, en el mismo barco, hizo parte de
los cálculos necesarios para probar que era el isótopo 235 del uranio el que
se fisionaba al bombardearlo con neutrones lentos.
|
La fisión |
|
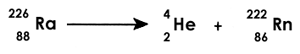
Esta operación consiste en provocar el estallido del núcleo de un átomo pesado, obteniendo fragmentos de masa mediana. Un isótopo del uranio, el 238U92 se presta a este proceso y una de las reacciones que se producen al bombardearlo con neutrones lentos se formula así:
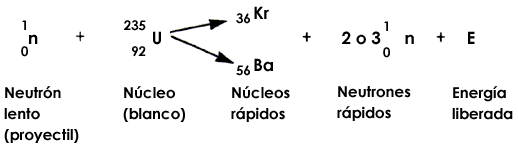
Esta reacción se conoce como fisión; consume un neutrón lento y libera, además de 2 ó 3 neutrones rápidos y energía, dos átomos de una masa media (kriptón y bario). Si se consigue disminuir la velocidad de estos neutrones rápidos, estos mismos neutrones son capaces de provocar 2 ó 3 nuevas reacciones etcétera. La energía E se puede calcular para la fisión individual tomando en cuenta las energías cinéticas del neutrón incidente, de los fragmentos Kr y Ba producidos de los neutrones expulsados y de la energía de la radiación g. También se puede hacer la suma de la energía de cohesión del núcleo inicial de U. La diferencia es entonces igual a E. La reacción de fisión contemplada aquí libera alrededor de 200 MeV. Esta energía es mucho mayor de la que se obtiene en los procesos de radiactividad natural (10 MeV). ¡Las reacciones químicas usadas, como la combustión del carbón, del hidrógeno, etc., proveen energías de unos cuantos electrón-volts solamente! Hay que hacer notar, además, que los 200 MeV no representan más que alrededor de 1/1000 de la masa del átomo de uranio que sufre la ruptura. En las bombas atómicas se deja que el mecanismo se multiplique y se dispone rápidamente de una energía colosal. En las pilas atómicas, al contrario, gracias a dispositivos moderadores, se le impide a la reacción en cadena degenerar en explosión y se controla en todo momento la potencia liberada por el reactor. El fenómeno de la fisión no debe confundirse con el de la fusión. |
No se debe dejar de mencionar aquí que, cuando Fermi estaba seguro de que el uranio, como otros núcleos pesados, se "tragaría" cualquier neutrón lento que se le acercara, Ida Noddack, una química alemana, apuntaba muy acertadamente que podían formarse elementos ligeros. Sin embargo Ida Noddack no propuso cómo se podrían formar dichos elementos ligeros y sus comentarios (publicados en una revista poco leída por los químicos y sencillamente no leída por los físicos) se tildaron de pedantería pura. Su artículo no tuvo ninguna trascendencia en el trabajo que vino después, como lo hemos visto en los párrafos anteriores. Ida Noddack dijo textualmente:
Es concebible que durante la irradiación de núcleos
pesados con neutrones, estos núcleos se desintegren en fragmentos mayores
que sean isótopos de elementos conocidos pero no necesariamente vecinos
de los elementos originalmente irradiados. |
A menudo esta frase se interpreta como la predicción de la fisión nuclear. Sin embargo, hay que insistir en que ni siquiera la Noddack consideró que su proposición fuera digna de probarse experimentalmente.
Strassmann dijo que había sido una coincidencia. Este menosprecio, sin duda, está influenciado por el dudoso e irreproducible descubrimiento del elemento natural 43 anunciado por Noddack. Cuando en cierta ocasión Ida Noddack se quejó de esta actitud, en una nota, Hahn y Strassmann prefirieron en el último momento no publicar una respuesta muy dura que ya habían redactado y le dejaron la ingrata misión a los editores de la revista. La relación entre el matrimonio Noddack y el dúo Hahn-Meitner fue muy tirante, ya que a las controversias científicas se sumaban las políticas.
Y aquí nos vemos obligados a hacer un paréntesis ya relatar lo que sucedía fuera de Berlín.
Aunque el grupo de Hahn consiguió mantenerse al margen del esfuerzo de guerra alemán, hubo otros grupos científicos pertenecientes a la escuela alemana que, colaborando con los aliados o con el eje, influyeron en el curso de la guerra. En Hamburgo, Paul Hartech, que había sido alumno de Rutherford, alertó al Ministerio de Guerra: "Nos tomamos la libertad de llamar su atención sobre el progreso más reciente en física nuclear. En nuestra opinión, permitirá tal vez producir un explosivo muchas veces más potente que cualquiera de los convencionales[. ..] La nación que se anticipe en su empleo tendrá una ventaja insalvable sobre las demás." ¿Palabras proféticas? Hoy sabemos que sí lo fueron y sin embargo los alemanes no consiguieron fabricar la bomba atómica. Una explicación de su fracaso, muy discutida al final de la guerra, radica en la reticencia de los físicos alemanes para fabricar una bomba en provecho de Hitler. En sus recuerdos, escritos después del conflicto, W. Heisenberg (1901-1976), el famoso teórico alemán, da la impresión de que tanto él como sus colegas no colaboraron en el proyecto con la diligencia de que eran capaces porque desaprobaban la idea de una bomba en manos del Fürher.
Sin embargo, la documentación confiscada a los alemanes después de la victoria demuestra que, al menos hasta 1942, los físicos alemanes se entregaron en cuerpo y alma al estudio del uranio. Quizás el motivo por el cual estos trabajos no desembocaron en el arma de la victoria fue la rivalidad entre físicos e ingenieros. En efecto, según los físicos, los ingenieros eran hombres prácticos y por lo mismo obtusos y sin imaginación. Los físicos, en cambio, se consideraban (¡y se consideran!) a sí mismos brillantes, ingeniosos, imaginativos, inventores [...] por lo tanto, sólo ellos debían construir los reactores imprescindibles para obtener el material atómico necesario para la bomba. El resultado fue que la guerra concluyó sin que Alemania tuviera un reactor operativo.
Y en cuanto a los reactores[...] hay que mencionar lo que sucedió en Francia: Joliot fue sometido a un interrogatorio para saber en dónde se encontraba el uranio y su agua pesada. Joliot "confesó" que el uranio había "sido evacuado" y el agua pesada embarcada en Burdeos, y les dio el nombre de un barco que había sido echado a pique.
Los alemanes se interesaron también en el ciclotrón —casi terminado— construido en los sótanos del Colegio de Francia, ya que no había ninguno en Alemania, y aunque W. Bothe (1891-1957) tratase de construir uno en su laboratorio de Heidelberg, pasarían años antes de que lo terminase. Los oficiales de la Wehrmacht decidieron adueñarse de la máquina de Joliot como botín de guerra y mandarla a Alemania.
En la primera conversación entre los alemanes y Joliot el intérprete resulto ser Wolfgang Gentner ¡El mismo joven que, siendo estudiante unos años antes en el laboratorio de Joliot, había revisado el contador Geiger cuando, por primera vez, Joliot detectó la radiactividad artificial! Según Gentner el reencuentro fue difícil para ambos. Sin embargo, Gentner consiguió entrevistarse en secreto, en uno de los cafés del Barrio Latino, con su antiguo profesor y pudo advertirle que el ciclotrón francés corría el riesgo de ir a parar a Alemania. Por lo tanto más valía, le sugirió Gentner, que se le propusiera a los invasores usarlo en la propia Francia. Joliot, con estos datos, supo conseguirlo.
En esa época, la política alemana consistía en tratar con cautela y respeto a los franceses eminentes con la esperanza, bien fundada por cierto, de que muchos colaborarían a la integración de su país en una Europa nazi. P. Laval, por ejemplo, quién dirigió el régimen de Vichy presidido por Petain en agosto de 1940, se lamentaba de que el agua pesada hubiese sido enviada a Gran Bretaña. Así que a finales de 1940 cuatro especialistas alemanes empezaron a trabajar en el ciclotrón dirigidos por Gentner. Este grupo tardó mucho en hacer funcionar el ciclotrón, en parte por la dificultad de conseguir las refacciones electrónicas y en parte también porque tuvieron qué modificarlo. De hecho, Gentner y sus colaboradores no querían trabajar para la guerra porque simpatizaban menos con sus compatriotas nazis que con sus anfitriones franceses. En más de una ocasión, como lo cuenta Joliot, avisaron a algunos de sus amigos franceses que la Gestapo los vigilaba.
Cuando Bothe aparecía en París, por una curiosa mala suerte, el ciclotrón no funcionaba. Era el jefe de talleres de Joliot el que de cuando en cuando cortaba el agua que servía para enfriar el aparato. Bothe entonces tenía que disculparse por "haber sobrecalentado" la máquina ¡Así, gracias a que un alemán (Gentner) supo separar los principios humanitarios del mundo de los intereses temporales de su propio país, los alemanes no consiguieron el ciclotrón!
El uranio belga y el agua pesada francesa proporcionaban a los aliados los ingredientes necesarios para la reacción en cadena. Pero recordemos que el uranio existe en la corteza terrestre en tres formas o isótopos. Dos son importantes, el 238U y el 255U , el fisionable es el 235U, pero aparece sólo en cantidades ínfimas, menos del 1% en el uranio tal y como se encuentra en la naturaleza. Nadie, en aquel entonces, tenía noción de cuánto 235U se requería para conseguir la "masa crítica". En aquella época se calculó que la carga imprescindible rayaba en 40 toneladas, o sea que el peso total de una bomba atómica sería demasiado grande para que la transportara un avión.
Fueron dos investigadores, alemán y el otro austríaco, refugiados en Gran Bretaña, Rudolph Peierls y Otto Frisch (otra vez el sobrino de L. Meitner) los que en un informe de sólo tres páginas propusieron que, en vez de intentar aumentar la cantidad de 235U era preferible extraer 235U del 238U. Las dos sustancias son químicamente similares y difieren sólo en el peso, digamos que como la nata y la leche. Los dos alemanes calcularon que 5 kg de 235U, al fisionarse, liberarían una energía igual a la de varios millones de toneladas de dinamita.
Este Memorandum de Frisch-Peierls, transmitido por los británicos a los estadounidenses, se convirtió en la base del proyecto Manhattan, cuyas consecuencias todos conocemos.
Aunque en Alemania se formó un grupo que debía estudiar los desarrollos militares, como lo discutimos antes, para tranquilidad de Hahn se le permitió seguir con su propia investigación. En efecto, Hahn no se interesó en la enorme liberación de energía que caracteriza a la fisión nuclear, en cambió le dedicó todo su empeño al estudio de los fragmentos obtenidos en el proceso. Por lo tanto, no participó en el proyecto del reactor y de la bomba atómica alemanes.
Al terminar la guerra, así como a otros científicos alemanes, se le obligó a instalarse en Inglaterra. Aunque ya tenía sesenta y seis años, todavía era un hombre vigoroso; había sido alpinista y ahora corría todos los días. Fue en la Gran Bretaña en donde se enteró de la explosión de las bombas atómicas en Hiroshima y Nagasaki. Es fácil entender su angustia, apenas compensada por el premio Nobel de química que se le otorgó en 1945.
Cuando pudo, al fin, volver a Alemania a principios de 1946, lo eligieron presidente
de la antigua Sociedad Kaiser Wilhelm, rebautizada por sugerencia de las potencias
de ocupación como Sociedad Max Planck para el avance de la ciencia. Otto Hahn
se convirtió en una figura pública muy respetada, era amigo de Theodor Heus
(1884-1963, primer presidente de la RFA) y militó enérgicamente
en contra del desarrollo y de las pruebas de las armas nucleares. Entre otros,
firmó la Declaración de Mainau (1955) de los laureados Nobel, resaltando el
peligro del mal uso de la energía atómica. Figuró entre los dieciocho científicos
alemanes eminentes que protestaron públicamente contra la adquisición de armas
nucleares por Alemania en 1957.
Simultáneamente se le honraba en todas partes. En 1966, por ejemplo, Meitner; Strassmann y él compartieron el prestigioso premio Enrico Fermi. Este periodo de su vida se vio oscurecido por la perdida de su hijo único, Hanno, y de su nuera, que se mataron en un accidente automovilístico en 1960. La señora Hahn nunca se recuperó de tan triste noticia.
Otto Hahn murió en Gotinga el 28 de julio de 1968 a consecuencia de una caída, y su mujer sólo le sobrevivió dos semanas.
Severo Ochoa (1905- , premio Nobel de medicina en 1959) en entrevista publicada en Ciencia y Desarrollo, afirma que la investigación necesita de un "caldo de cultivo" o sea de un ambiente y de unas facilidades que, como lo hemos destacado en este texto, se dieron en la Alemania de principios de siglo.
Aunque hoy éstas son las verdades del barquero, conviene recordar lo que hace más de un siglo Louis Pasteur (1822-1895), que tenía 57 años cuando nació Otto Hahn, escribió en un folleto dirigido a los franceses:
Os suplico que os intereséis por esos sagrados
edificios significativamente llamados laboratorios. Solicitad que sean
multiplicados y completados. Son los templos del futuro, de las riquezas
y del bienestar. |
Otto Hahn descubrió la fisión nuclear porque, además de su propio talento, disponía del laboratorio adecuado, porque estaba rodeado de científicos brillantes y porque podía comunicarse y discutir sus resultados con los investigadores del mundo entero. Y él, que vivió dos guerras, quizás hubiera podido decir lo que Carlos Fuentes escribe en El prisionero de las Lomas: "la información es la base del poder, pero la condición es saber emplearla, o, llegado el caso, no emplearla: el silencio también es poder."
I. Asimov, Historia de la energía nuclear, Alianza Editorial, El libro de bolsillo, Madrid, 1985.
M. E. Brandan, Armas y explosiones nucleares: la humanidad en
peligro, La Ciencia desde México, SEP-FCE-CONACYT, núm. 61,
1988.
S. Bulbulian, La radiactividad, La Ciencia desde México, SEP-FCE-
CONACYT, núm. 42, 1987.
H.O. Denschlag, "The discovery of nuclear fission 50 years ago, a few remarks", J. of Radioanalytical and Nuclear Chemistry, Articles, 142, 5, 1990.
H. García Fernández, La bomba y sus hombres, Editorial Alhambra, 1987.
J. Hachette y J. Hytril, Dictionnary of Scientific Biography, C.C. Gillespie (editor), vol. IV, Charles Scrinbner's Sons, Nueva York.
O. Hahn, New atoms, progress and some memories, Elsevier Publishing Company, 1950.
O. Hahn, "The discovery of fission", Scientific American, p. 76, feb.,1958.
G. Hermann, Five decades ago: from the "transuranics " to nuclear fission, Angew. Chem. Int. Ed., Inglaterra, 29, 481, 1900.
A. Mondragón, "La física nuclear" en La física contemporánea 2. La
ciencias del siglo XX, UNAM, Guillermo Aguilar (comp.), México,1983.
Nobel Lectures (Physics), Incluye discursos y las biografías de los
laureados 1922-1941. Publicada por la Fundación Nobel en 1965,
Elsevier Publishing Company, Amsterdam, Londres, Nueva York,
1965.
P. Pringle y J. Spigelman, Los barones nucleares, Planeta, Colección Al filo del tiempo, 1984.
J. Rickards, Las radiaciones: reto y realidades, La Ciencia desde
México, SEP-FCE-CONACYT, núm. 8, 1986.
W.R. Shea, Otto Hahn and the rise of nuclear physics, D. Reideel Publishing Company, Dordrecht, Boston, Lancaster, 1983.
R.L. Sime, "Belated recognition: Lise Meitner's role in the discovery of fission", J. of Radioanalytical and nuclear Chemistry articles, 142, 13, 1990.
S. Weart, La grande aventure des atomistes français, Fayard, París, 1980.
![[Inicio]](../img/begin.gif)
![[Anterior]](../img/prevsec.gif)

![[Siguiente]](../img/nextsec.gif)
![[FNT 30]](../img/pio109.gif)
![[FNT 32]](../img/pio111b.gif)
![[FNT 33]](../img/pio112c.gif)
![[FNT 34]](../img/pio113a.gif)